
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Биологическая роль
|
|
|
|
1. ТПФ участвует в реакциях декарбоксилирования α-кетокислот;
2. ТПФ участвует в расщеплении и синтезе α-оксикислот (например, кетосахаров), т.е. в реакциях синтеза и расщепления углерод-углеродных связей, находящихся в непосредственной близости к карбонильной группе.
Тиамин-зависимые ферменты – пируватдекарбоксилаза и транскетолаза.
Авитаминоз и гиповитаминоз.
Болезнь бери-бери, нарушения функций пищеварительного тракта, изменения психики, изменения деятельности сердечно-сосудистой деятельности, развитие отрицательного азотистого баланса и т.д.
Источники: растительные продукты, мясо, рыба, молоко, бобовые растения – фасоль, горох, соя и др.
Суточная потребность: 1,2-2,2 мг.
Витамин В2 (рибофлавин, витамин роста)
Кроме самого рибофлавина в природных источниках содержатся его коферментные производные: флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД). Эти коферментные формы витамина В2 количественно преобладают в большинстве животных и растительных тканей, а также в клетках микроорганизмов.
В зависимости от источника получения витамин В2 называли по разному: лактофлавин (из молока), гепафлавин (из печени), вердофлавин (из растений), овофлавин (из яичного белка).
Химическая структура: в основе молекулы рибофлавина лежит гетероциклическое соединение – изоаллоксазин (сочетание бензольного, пиразинового и пиримидинового колец), к которому в положении 9 присоединен пятиатомный спирт рибитол. Химический синтез рибофлавина осуществлен в 1935 г. Р.Куном.
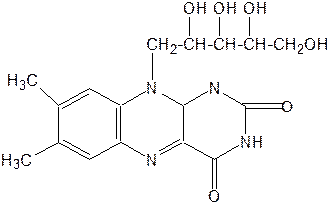
 | ||||
Рибофлавин
Растворы витамина В2 имеют оранжево-желтую окраску и характеризуются желто-зеленой флюоресценцией.
Желтый цвет присущ окисленной форме препарата. Рибофлавин в восстановленной форме – бесцветен.
В2 хорошо растворим в воде, устойчив в кислых растворах,легко разрушается в нейтральных и щелочных растворах. В2 чувствителен к видимому и УФ-излучению, легко подвергается обратимому восстановлению, присоединяя Н2 по месту двойной связи и превращаясь в бесцветную лейкоформу. Это свойство витамина В2 легко окисляться и восстанавливаться лежит в основе его биологического действия в клеточном метаболизме.
Авитаминоз и гиповитаминоз: остановка роста, выпадение волос, воспалительные процессы слизистой оболочки языка, губ и т.д. Кроме того, общая мышечная слабость и слабость сердечной мышцы; помутнение хрусталика (катаракта).
Биологическая роль:
1. Входит в состав флавиновых коферментов ФАД, ФМН, которые являются простетическими группами флавопротеинов;
2. Участвует в составе ферментов при прямом окислении исходного субстрата с участием О2, т.е. дегидрировании. К коферментам этой группы относятся оксидазы L- и D-аминокислот;
3. В составе флавопротеинов осуществляют перенос электронов от восстановленных пиридиновых коферментов.
Источники: дрожжи, хлеб (мука грубого помола), семена злаковых, яйца, молоко, мясо, свежие овощи, молоко (в свободном состоянии), печень и почки (в составе ФАД и ФМН).
Суточная потребность: 1,7мг.
Витамин В6 (пиридоксин, антидермический)
Открыт в 1934 г. П. Дьерди. Впервые выделен из дрожжей и печени.
Химическая структура. Витамин В6 является производным 3-оксипиридина. Термином «витамин В6» по рекомендации Международной комиссии по номенклатуре биологической химии, обозначают все три производных 3-оксипиридина, обладающих одинаковой витаминной активностью: пиридоксин (пиридоксол), пиридоксаль и пиридоксамин.
 | 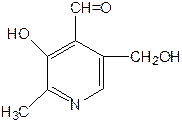 | 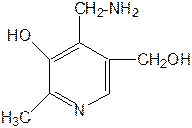 | |||
пиридоксин пиридоксаль пиридоксамин
В6 хорошо растворим в воде и этаноле. Водные растворы весьма устойчивы по отношению к кислотам и щелочам, но чувствительны к свету в нейтральной зоне рН.
Авитаминозы гиповитаминоз. У человека недостаточность витамина В6 проявляется в угнетении выработки эритроцитов, дерматите, воспалительных процессах кожи, замедлении роста животных, нарушении обмена триптофана.
Биологическая роль. Все три производные 3-оксипиридина наделены витаминными свойствами, коферментные функции выполняют только фосфорилированные производные пиридоксаля и пиридоксамина:
 | 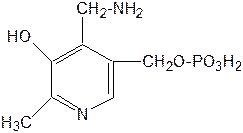 | ||
пиридоксаминфосфат пиридоксальфосфат
Пиридоксаминфосфат как кофермент функционирует в реакциях превращения карбонильных соединений, например в реакциях образования 3,6-дтдезоксигексоз,входящих в антигены, локализованные на поверхности бактериальных клеток.
Биохимические функции пиридоксальфосфата:
1. транспортная – участие в процессе активного переноса некоторых аминокислот через клеточные мембраны;
2. каталитическая – участие в качестве кофермента в широком круге ферментативных реакций (переаминирование, декарбоксилирование, рацемизация аминокислот и др.);
3. функция регулятора скорости оборота пиридоксалевых ферментов – удлинение времени полураспада в тканях некоторых пиридоксальных апоферментов при их насыщении пиридоксальфосфатом,повышающим устойчивость апоферментов к тепловой денатурации и действию специфических протеиназ.
При недостаточности витамина В6 наблюдаются нарушения метаболизма аминокислот.
Источники: в продуктах растительного и животного происхождения (хлеб, горох, фасоль, картофель, мясо, печень и т.д.). Он также синтезируется микрофлорой кишечника!
Суточная потребность: около 2 мг.
Витамин В12 (кобаламин,антианемический)
Кобаламины – групповое название соединений, обладающих В12-витаминной активностью.
Химическая структура. Центральной частью молекулы витамина В12 является циклическая корриновая система, напоминающая по структуре порфирины (отличаются от них тем, что два пиррольных кольца плотно сконденсированы друг с другом, а не соединены через метиленовый мостик). Под плоскостью корринового кольца, в центре которого находится Со, находится присоединенный к кобальту остаток 5-дезоксиаденозина.
Авитаминоз и гиповитаминоз. Недостаток витамина В12 приводит к развитию злокачественной анемии, нарушению деятельности ЦУНС и резкому снижению кислотности желудочного сока.
Для активного процесса всасывания витамина В13 в тонком кишечнике обязательным условием является наличие в желудочном соке внутреннего фактора Касла (особого белка – гастромукопротеина), который специфически связывает витамин В12 в особый сложный комплекс и в таком виде всасывается в кишечнике.
Биологическая роль. Выявлены ферментные системы в состав которых в виде простетической группы входят кобаломидные коферменты
Химические реакции, в которых витамин В12 принимает участие как кофермент, условно делят на две группы. К первой группе относятся реакции трансметилирования, в которых метилкобаламин выполняет роль промежуточного переносчика метильной группы (реакции синтеза метионина и ацетата).
Вторая группа реакций при участии В12-коферментов заключается в переносе водорода в реакциях изомеризации.
Источники: мясо, говяжья печень, почки, рыба, молоко, яйца. Главным местом накопления витамина В12 в организме человека является печень, в которой содержится до нескольких мг витамина.
Витамин В12 является единственным витамином, синтез которого осуществляется исключительно микроорганизмами.
Синтезируется кишечной микрофлорой!
Суточная потребность 0,003 мг.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 1579; Нарушение авторских прав?; Мы поможем в написании вашей работы!