
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Зарождение идеи квантованности мира
|
|
|
|
Для выхода из противоречия М.Планк предположил, что энергию электромагнитных колебаний нельзя делить до бесконечности. Для каждой частоты колебаний 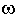 существует минимально возможная порция (квант) энергии
существует минимально возможная порция (квант) энергии  E =
E = 
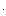
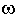 , где
, где  - постоянная Планка. Меньше этого кванта не существует порций энергии с данной частотой колебаний. Несмотря на крайне непривычные для физиков выводы, которые последовали за этим предположением, ученый мир вынужден был признать справедливость квантования, так как этот закон с колоссальной точностью выполнялся на опыте, устраняя парадокс Рэлея-Джинса. Это событие считается концом классического периода естествознания.
- постоянная Планка. Меньше этого кванта не существует порций энергии с данной частотой колебаний. Несмотря на крайне непривычные для физиков выводы, которые последовали за этим предположением, ученый мир вынужден был признать справедливость квантования, так как этот закон с колоссальной точностью выполнялся на опыте, устраняя парадокс Рэлея-Джинса. Это событие считается концом классического периода естествознания.
В числе прочего идея квантования энергии подтверждалась и тем фактом, что спектр любого светового излучения вовсе не являлся непрерывным, а состоял из последовательности полос, каждая из которых соответствовала определенной частоте электромагнитных волн. Возник вопрос, почему атомы излучают свет не всех частот, а только определенных, как это предписывалось классическими законами? Почему электроны, вращаясь вокруг ядра, не излучают непрерывно энергию и в конечном итоге не падают на ядро?
Бор предположил, что электроны в атоме, как и электромагнитные колебания, также могут иметь только строго определенные энергии. Это привело к созданию квантовой модели атома, согласно которой электроны в атоме могут находиться только на определенных орбитах. Бор установил правила для нахождения этих допустимых орбит. «Упасть» на ядро электрон просто не «имеет права» так как должен перейти с допустимой орбиты в недопустимое состояние. Каждой орбите соответствует своя энергия. Излучить энергию электрон может только в том случае, если ближе к ядру находится свободная допустимая орбита, на которую может перескочить электрон. На орбите с наименьшей возможной энергией электрон может находиться неограниченно долго. Но он может перескочить и на более высокую освободившуюся орбиту, если поглотит квант энергии (фотон). Никогда на одной орбите не могут находиться два электрона с одинаковым набором квантовых чисел (принцип Паули).
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 477; Нарушение авторских прав?; Мы поможем в написании вашей работы!