
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Многоатомные спирты
|
|
|
|
Простейшие представители многоатомных спиртов – этиленгликоль и глицерин:
СН2 – СН2 СН2 – СН – СН2
ê ê | | |
ОН ОН ОН ОН OH
этиленгликоль глицерин
(этандиол) (пропантриол)
Физические свойства. Этиленгликоль и глицерин – вязкие жидкости, сладкие на вкус, хорошо растворимые в воде. Многоатомные спирты имеют большее количество полярных гидроксильных групп, участвующих в образовании водородных связей, поэтому их Т. кип. значительно выше, чем одноатомных спиртов:
| вещество | Т. кип. | вещество | Т. кип. |
| CH3−СH2−OH | 78º | CH3−CH2−CH2−OH | 97º |
| CH2−CH2 | | OH OH | 197º | CH2−CH−CH2 | | | OH OH OH | 290º |
Химические свойства многоатомных спиртов сходны со свойствами одноатомных спиртов. В реакциях может участвовать либо одна, либо несколько гидроксильных групп. Однако −I-эффект дополнительных гидроксильных групп делает атомы водорода OH-групп более подвижными, поэтому многоатомные спирты, в отличие от одноатомных, реагируют с щелочами, образуя соли:
 HO−CH2−CH2−OH + 2 NaOH NaO−CH2−CH2−ONa + 2 H2O
HO−CH2−CH2−OH + 2 NaOH NaO−CH2−CH2−ONa + 2 H2O
полный гликолят натрия
СН2− СН− CH2 СН2−СН−CH2
 | | | + NaOH | | | + H2O
| | | + NaOH | | | + H2O
ОН ОН OH OH ONa OH
моноглицерат натрия
Особенно легко идет замещение атома водорода гидроксильной группы на ионы тяжелых металлов в результате образования комплексов. Осадок гидроксида меди растворяется в глицерине с получением ярко-синего раствора комплексного соединения глицерата меди:



 2−
2−

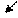 CH2−OH СН2– О O – CH2 2 K+
CH2−OH СН2– О O – CH2 2 K+

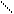 | | Cu |
| | Cu |
 2 CH−OH + Cu(OH)2 + 2 KOH СН2– О O – CH2 + 4 H2O
2 CH−OH + Cu(OH)2 + 2 KOH СН2– О O – CH2 + 4 H2O
| | |
CH2−OH CH2−OH HO−CH2
 |  |
глицерат меди
Реакция с гидроксидом меди используется при качественном определении многоатомных спиртов, имеющих ОН-группы у соседних атомов углерода.
Этиленгликоль получают окислением этилена в водном растворе перманганата калия:
KMnO4
 СH2 = CH2 + H2O HO−СH2−CH2−OH
СH2 = CH2 + H2O HO−СH2−CH2−OH
Глицерин ранее получали гидролизом растительных или животных жиров. В настоящее время его получают из пропилена:
Cl2, hν HOCl H2O


 CH2=CH−CH3 CH2=CH−CH2Cl CH2−CH−CH2Cl CH2−CH−CH2
CH2=CH−CH3 CH2=CH−CH2Cl CH2−CH−CH2Cl CH2−CH−CH2
| | | | |
OH Cl OH OH OH
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 549; Нарушение авторских прав?; Мы поможем в написании вашей работы!