
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тепловая теорема нернста. Сопоставление тепловых эффектов и изменения энергии Гиббса в реакциях, происходящих в конденсированных системах при различных температурах
Сопоставление тепловых эффектов и изменения энергии Гиббса в реакциях, происходящих в конденсированных системах при различных температурах, показывает, что в области низких температур при приближении к абсолютному нулю значения тепловых эффектов и изменения энергии Гиббса сближаются. Тепловая теорема является постулатом, утверждающим, что это сближение продолжается и при дальнейшем понижении температуры, причем при абсолютном нуле и вблизи него кривые соприкасаются и общая для них касательная параллельна оси температур.
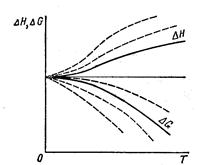
Математически ΔG = ΔH
lim│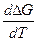 │T→0 = lim│
│T→0 = lim│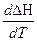 │T→0 = 0
│T→0 = 0
Из тепловой теоремы вытекает ряд следствий
(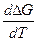 )p = -ΔS при Т → 0
)p = -ΔS при Т → 0
lim[ΔS]T→0 = 0 [ΔS]T=0 = 0
т.е. вблизи абсолютного нуля все реакции, совершающиеся в конденсированных системах,не сопровождаются изменением энтропии.
Второе следствие получим, применяя условие
(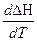 )p = ΔC
)p = ΔC
lim[ΔC]T→0 = 0 [ΔC]T=0 = 0
т.е. вблизи абсолютного нуля изменение теплоемкости твердых реагирующих веществ бесконечно мало отличается от нуля. Можно показать, что при очень низких температурах не только ΔS и ΔС твердых тел стремятся к нулю, но и многие другие свойства тел (объем, давление насыщенного пара и др.) изменяются с температурой так, что их производные по температуре стремятся к нулю. Этим объясняется принцип недостижимости абсолютного нуля (называемый также третьим законом термодинамики),согласно которому никакие процессы не могут снизить температуру до абсолютного нуля.
1.24 РАСЧЕТ ХИМИЧЕСКОГО РАВНОВЕСИЯ С ПОМОЩЬЮ
СТАНДАРТНЫХТЕРМОДИНАМИЧЕСКИХ ВЕЛИЧИН
В настоящее время известны стандартные теплоты образования и энтропии более 7500 простых веществ и соединений. С помощью этих табличных данных можно вычислить термодинамические параметры многих десятков тысяч реакций, в том числе предполагаемых и не изученных экспериментально. В методе расчета, основанном на использовании стандартных термодинамических величин, используются два исходных уравнения
ΔG0T = ΔH0T – TΔS0T
lnK0P = - ΔG0T /RT
Если нет никаких предварительных сведений о положении равновесия при интересующей нас температуре, расчет ΔG и Кр полезно производить в две стадии. В первой стадии вычисляют изменение энергии Гиббса при Т = 298К и для стандартных условий.
Для расчета ΔН0298 и ΔS0298 используют уравнения
ΔH0298 = (nΔH0298,f)кон - (nΔH0298f)нач
ΔS0298 = (nS0298)кон - (nS0298)нач
По величине и знаку  ΔG0298 судят о возможности получения желаемых веществ из взятых исходных в стандартных условиях.
ΔG0298 судят о возможности получения желаемых веществ из взятых исходных в стандартных условиях.
Не следует думать, что реакция неосуществима вообще, если по расчету получится сравнительно небольшая величина ΔG0298.Реакция невозможна только в стандартных условиях, но, вероятно, может протекать при иных температурах и давлении, при непрерывном удалении продуктов реакции из зоны реакции.
Точный расчет (вторая стадия) покажет - при каком сочетании указанных факторов величина энергии Гиббса станет отрицательной и как она должна быть изменена дальше, чтобы выход продуктов реакции сделался достаточно большим. В качестве ориентировочного критерия, определяющего целесообразность второго этапа расчетов, рекомендуется величина ΔG0298 = 418кдж/моль
На второй стадии расчета переходят от значения ΔG0298 к значению ΔG0т при других температурах.
Для этого необходимо вычислить ΔH0т и ΔS0т при заданной Т.
ΔH0т = ΔН0298 + 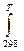 ΔСрdT
ΔСрdT
ΔS0т = ΔS0298 + 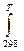 ΔСр
ΔСр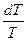
ΔG0т = ΔH0298 – TΔS0298 + 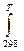 ΔCpdT - T
ΔCpdT - T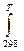 ΔCp
ΔCp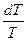
Если пренебречь влиянием изменения теплоемкости, т. е. ΔСр = 0,то решение уравнения будет грубо приближенным
ΔG0т = ΔH0298 – TΔS0298
Данное приближение (первое приближение Улиха) необходимо для быстрой оценки возможности протекания реакции при интересующей температуре.
При выполнении точного расчета подставляется зависимость
ΔСр = f(T) ΔCр = Δа + ΔвТ + ΔсТ2 + Δс1 Т-2
Проведя интегрирование, получим
ΔG0 т = ΔH0298 – TΔS 0298 - T{Δa(ln +
+  - 1) +
- 1) +
+ 
 (T - 2×298 +
(T - 2×298 +  ) +
) + 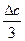 (Т2 - 3×2982 +
(Т2 - 3×2982 +  ) - Dс1(-
) - Dс1(-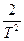
+ 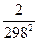 +
+ 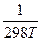 )}.
)}.
DG0T = DH0298 - T×DS0298 – T(DaM0 + DbM1 + DcM2 + Dc1M-2.
Коэффициенты М0,М1,М2, М-2 рассчитаны для разных температур, их значения можно найти в справочнике.
Этот метод расчета называется методом Темкина – Шварцмана.
|
Дата добавления: 2014-01-07; Просмотров: 440; Нарушение авторских прав?; Мы поможем в написании вашей работы!