
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Моносахариди
|
|
|
|
Структура молекул. Моносахариди – це сполуки, що містять одночасно гідроксильні групи (-он) та альдегідну (–СОН) або кетонну (=С=О) групу. Перші називають альдозами, другі – кетозами.
Моносахариди утворюються в результаті окислення багатоатомних спиртів. При окисленні первинної спиртової групи (–СН2ОН) утворюються альдози, а при окисленні вторинної спиртової групи (–СНОН) – кетози. Утворення найпростіших моносахаридів – тріоз: гліцеринового альдегіду і дигідроксиацетону можна розглянути на прикладі окислення (дегідрування) триатомного спирту гліцерину.
При окисленні шестиатомного спирту сорбіту, що міститься у багатьох плодах, утворюються гексози – глюкоза або фруктоза.
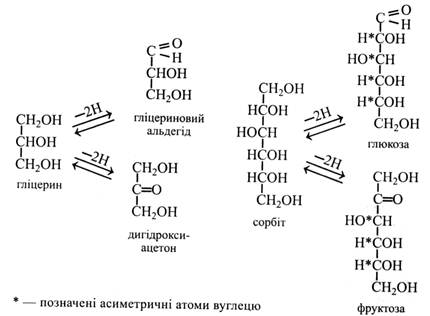
У назвах альдоз використовується суфікс «-оза» (глюкоза, галактоза, рибоза, ксилоза), а у назвах кетоз – суфікс «-улоза» (рибулоза, ксилулоза, седогептулоза).
Значний внесок у вивчення будови і перетворення вуглеводів, особливо моносахаридів, зробив великий німецький вчений-хімік Еміль Фішер. Ним також були запропоновані лінійні формули моносахаридів.
Глюкоза, фруктоза та інші моносахариди містять асиметричні атоми вуглецю, у яких усі 4 валентності заміщені різними атомами і групами. Це визначає їхню оптичну активність, тобто здатність в розчині обертати площину поляризації праворуч (+) або ліворуч (–), а також наявність стереоізомерів, що розрізняються за своїми фізичними і хімічними властивостями.
Кількість стереоізомерів даного моносахариду дорівнює 2n, де n – число асиметричних атомів вуглецю в молекулі. Глюкоза має 4 асиметричні атоми і 24=16 стереоізомерів, а фруктоза – 3 симетричні атоми і 23=8 стереоізомерів.
Серед стереоізомерів моносахаридів більш відомі D і L, або, як часто говорять, моносахариди можуть мати D- і L-конфігурацію. При визначенні конфігурації того чи іншого моносахариду як стандарт використовують гліцериновий альдегід, що містить тільки один асиметричний атом вуглецю і, отже, має тільки одну пару стереоізомерів – D i L.

Гліцериновий альдегід може існувати в трьох формах: у вигляді право- і лівообертальних D- та L-стереоізомерів та у вигляді суміші їх рівних кількостей. Така суміш називається рацемічною, вона позбавлена оптичної активності.
Моносахариди, у яких розташування –Н і –ОН біля найближчого до первинної спиртової групи вуглецевого атому таке ж саме, у D-гліцеринового альдегіду, мають D-конфігурацію, а ті, у яких –Н і –ОН розташовані біля того ж вуглецевого атому, як у L-гліцеринового альдегіду, відносять до L-стереоізомерів. Інакше кажучи, для визначення конфігурації даного моносахариду розглядають розташування –Н і –ОН біля асиметричного атому вуглецю, найбільш віддаленого від карбонільної групи =С=О або –СОН. Звичайно цей вуглецевий атом є найближчим до первинної спиртової групи. Якщо вуглецевий ланцюг цукру зображений зверху вниз і карбонільна група розташована вгорі, то у D-стереоізомерів група –ОН біля останнього асиметричного атома знаходиться праворуч, а у L-стереоізомерів – ліворуч.
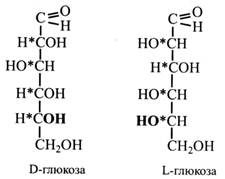
D i L-стереоізомери відносяться один до одного, як предмет і його дзеркальне відображення. Тому в L-глюкози –Н і –ОН біля всіх асиметричних вуглецевих атомів мають протилежне D-глюкозі розташування, а місце групи –ОН біля 5-го вуглецевого атому є лише ознакою для класифікації стереоізомерів.
У рослинах містяться і засвоюються в основному D-форми цукрів. L-форми зустрічаються дуже рідко. Тому далі ми будемо позначати лише L-форми, маючи на увазі, що всім іншим моносахаридам притаманна D-конфігурація.
На перших етапах вивчення моносахаридів їхні відомі властивості добре пояснювалися формулами Фішера. Пізніше виявилися нові ознаки цукрів, які вже не можна було пояснити цими формулами. Наприклад, було показано, що моносахариди не завжди виявляють альдегідні властивості (не дають реакції з фуксинсульфітною кислотою, не утворюють бісульфітної сполуки з NaHSO3). При розчиненні моносахаридів спостерігалася зміна питомого обертання, яке лише через деякий час досягало постійної величини.
Це явище назвали мутаротацією. Крім того, виявилося, що один із гідроксилів молекули моносахариду відрізняється більш високою реакційною активністю.
Для пояснення цих і ряду інших особливостей московський професор-хімік М. А. Коллі у 1870 р. запропонував гіпотезу, відповідно до якої моносахариди існують не тільки в альдо- і кето-, але й у циклічній формі. Це припущення у 1883 р. підтвердив і розвинув німецький хімік Б. Толленс. Згідно з його гіпотезою, моносахариди існують не тільки у формі альдо- і кетоспиртів, а й у вигляді циклічних напівацеталей. Напівацеталі утворюються в результаті реакції альдегідів зі спиртами.
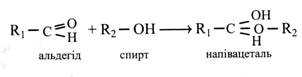
Подібна реакція між альдо- або кетогрупою і гідроксилом спиртової групи може відбуватися й усередині молекули моносахариду, в результаті чого утворюються циклічні напівацеталі.
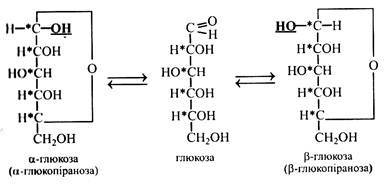
І наведених формул циклічних напівацеталей глюкози видно, що у них немає альдегідної групи, це пояснює відсутність альдегідних властивостей. До того ж у циклічних форм з'являється ще один асиметричний атом вуглецю, це приводить до виникнення ще однієї пари стереоізомерів, які позначають α і β.
Встановлення між цими стереоізомерами рівноважного стану пояснює мутаротація. Новий гідроксил, що з'явився при циклізації у молекулі цукру, назвали напівацетальним, а пізніше глікозидним. Цей гідроксил і виявився найбільш реакційноздатним. При написанні формули моносахариду зверху вниз у α-стереоізомерів напівацетальний гідроксил розташовується праворуч, а у β-стереоізомерів – ліворуч.

Наведені вище циклічні формули моносахаридів є похідними гетероциклічних сполук – шестичленною пірану і п’ятичленного фурану – піранози і фуранози (глюкопіраноза, фруктофураноза). В. Хеуорс запропонував зображати циклічні моносахариди у вигляді перспективних формул.
У цих формулах товстими лініями зображують зв'язки між вуглецевими атомами, які на площині потрапляють на передній план.
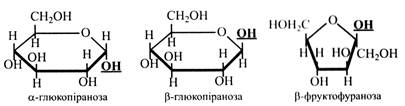
Атомів вуглецю в кільці перспективних формул зазвичай не пишуть. α-Форми і β-форми розрізняються за положенням –ОН (напівацетального гідроксилу) відносно площини кільця. У α-стереоізомерів -ОН розташовується під площиною кільця, а у β-ізомерів – над площиною.
У живих організмах молекули моносахаридів завжди мають циклічну форму, у такому ж вигляді залишки цукрів входять до складу полісахаридів. У твердому стані цукри також мають циклічну будову. Тільки в розчині з'являються, крім циклічних, ще і нециклічні форми молекул. При цьому останніх у розчині мало – до 1 %.
У природі серед циклічних форм цукрів в основному зустрічаються піранози, фураноз дуже мало (фруктоза, рибоза).
Хімічні властивості
Моносахариди легко окислюються з утворенням кислот. Причому окислення може відбуватися як у кислому, так і в лужному середовищі. У цукрів легше за все окислюється альдегідна група.
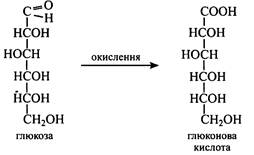
У лужному середовищі моносахариди можуть окислюватися оксидами металів (міді, вісмуту, срібла). При цьому цукор окислюється до кислоти, а оксиди металів відновлюються. Оксид міді (II), відновлюючись, утворює оксид міді (І). Ця реакція використовується для кількісного визначення цукрів за кількістю оксиду міді (І).
При взаємодії цукрів з оксидами вісмуту і срібла останні відновлюються до вільних металів. Реакція «срібного дзеркала» використовується для сріблення ялинкових прикрас, колб, посудин Дюара та термосів.

Однак так, як написано, реакція з оксидом міді (II) йти не може, бо СuО – нерозчинний у воді порошок. У зв'язку з цим для реакції беруть сіль двовалентної міді – СuSO4. Оскільки окислювання цукрів відбувається в лужному середовищі, до розчину СuSO4 необхідно додати луг.
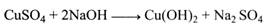
Але й у цьому разі виникає перешкода: Сu(ОН)2 являє собою драглеподібний осад і не може далі реагувати з цукром. Для подальшого ходу реакції необхідно утримувати катіони двовалентної міді в лужному середовищі в розчині. Для цього до лужного розчину міді додають сегнетову сіль (К, Na-виннокислий), яка зв'язує іони міді й утримує їх у лужному середовищі в розчині.

Цей розчин синього кольору, що містить СuSO4, NaОН і сегнетову сіль, називають фелінговою рідиною і використовують для кількісного визначення цукрів. Фелінгову рідину нагрівають із розчином цукру. При цьому випадає червоний осад Сu2O, кількість якого відповідає кількості цукру.
Фелінгову рідину відновлюють цукри, що мають вільний напівацетальний (глікозидний) гідроксил. Це усі моносахариди і деякі олігосахариди. Їх називають відновними цукрами на відміну від тих, що не містять вільного напівацетального (глікозидного) гідроксилу і не здатні відновлювати фелінгову рідину.
При відновленні моносахариди утворюють відповідні багатоатомні спирти. Так, при відновленні глюкози і фруктози утворюється шестиатомний спирт – сорбіт.
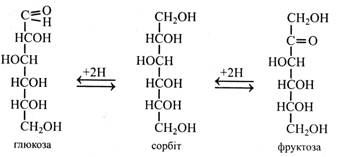
У рослинах кислоти і спирти утворюються з моносахаридів ферментативним шляхом.
Моносахариди можуть взаємодіяти з кислотами, утворюючи складні ефіри. Особливо велике значення в живих клітинах мають складні ефіри цукрів і фосфорної кислоти – сахарофосфати.
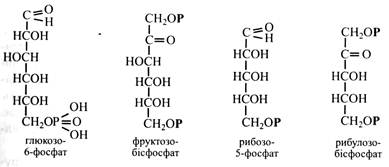
Сахарофосфати є активованими формами моносахаридів, оскільки містять багатий на енергію фосфорноефірний зв'язок. Тому вони легко вступають у біохімічні реакції. По суті, весь вуглеводний обмін у рослинах – це реакції між сахарофосфатами або з неодмінною їхньою участю.
Важливою властивістю цукрів є їхня здатність утворювати глікозиди. Це відбувається в результаті реакції напівацетального (глікозидного) гідроксилу з будь-якою сполукою, частіше невуглеводної природи (агліконом), α- і β-стереоізомери утворюють, відповідно, α- і β-глікозиди, які відрізняються за хімічними властивостями і на які діють різні ферменти. У рослинах частіше зустрічаються β-глікозиди.
Одними з найпростіших глікозидів є метилглікозиди.
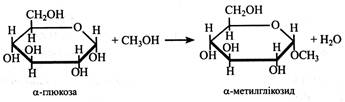
Глікозиди дуже поширені в рослинах. Їх агліконами можуть бути різні речовини (спирти, кислоти, фенольні сполуки). Цукри, що входять до складу глікозидів, дуже різноманітні й часто у вільному стані не зустрічаються. Глікозиди нерідко мають гіркий смак і специфічний аромат.
У рослинах петрушки міститься глікозид апіїн, у листках і насінні хрестоцвітих – глікозид синігрин, що надає специфічного запаху та гіркого смаку гірчиці. Відома ароматична речовина ванілін є агліконом глікозиду кори ванільного дерева. У насінні рослин із родини розових є глікозид амігдалін, що містить в агліконі залишок синільної кислоти. Саме цей глікозид надає запаху гіркого мигдалю кісточкам персиків, абрикосів, слив, вишень тощо.
Деякі глікозиди застосовуються у медицині, наприклад, група серцевих глікозидів. Вони позитивно впливають на роботу серцевого м'яза. Серцевих глікозидів багато, наприклад у наперстянці.
Характеристика окремих моносахаридів
Моносахариди – білі кристалічні речовини, добре розчинні у воді, які мають більш-менш солодкий смак. Вони дуже поширені в природі, особливо їх багато в рослинах. Моносахариди в рослинах знаходяться у вільному стані, у вигляді фосфорних ефірів, вони входять до складу полісахаридів та інших сполук (глікозидів, гліколіпідів, глікопротеїдів).
Моносахариди класифікують за числом вуглецевих атомів у ланцюжку (С3-С9) на тріози, тетрози, пентози, гексози, гептози, октози і нанози.
Тріози. До них належать найпростіші моносахариди – гліцериновий альдегід і дигідроксиацетон.
У вільному стані вони не зустрічаються, а у вигляді фосфорних ефірів (ФГА і ФДА) є важливими проміжними сполуками обміну вуглеводів (фотосинтез, дихання, бродіння).
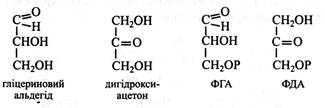
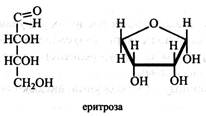
Тетрози. Найбільш поширена у рослинах тетроза – еритроза, що має фуранозну форму й у вигляді фосфорного ефіру бере участь в обміні вуглеводів.
Пентози. Рослини характеризуються високим вмістом пентоз. При нагріванні з розбавленою Н2SO4 або НС1 пентози утворюють леткий гетероциклічний альдегід фурфурол, що з НС1 і аніліном дає інтенсивне червоне забарвлення. Ця реакція служить для якісного і кількісного визначення пентоз. Серед пентоз найбільш відомими є ксилоза, арабіноза і рибоза.
Ксилоза. Її ще називають деревним цукром. Вона входить до складу полісахаридів (геміцелюлози, гумі, слизи). Ксилозу одержують шляхом гідролізу деревини, соломи, висівок, бавовняного і соняшникового лушпиння. На розчинах гідролізної ксилози вирощують мікроорганізми Torula і Manilia, що дають багатий білком корм худобі. Ксилозу також використовують у кондитерській промисловості. Для цього її одержують гідролізом кукурудзяних качанів, які містять до 12 % цього цукру.
Ксилоза входить до складу глікозидів, а у вигляді фосфорних ефірів бере участь в обміні вуглеводів. Вона не зброджується дріжджами і не засвоюється людським організмом.
У рослинах в обміні вуглеводів бере участь ізомер ксилози – ксилулоза у вигляді фосфорного ефіру.

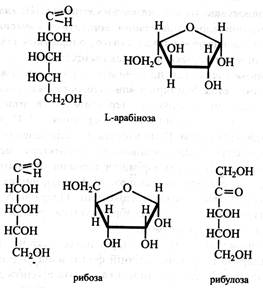
L-арабіноза знаходиться в рослинах у фуранозній формі та входить до складу полісахаридів (геміцелюлози, гумі, слизи). Арабінозу одержують шляхом кислотного гідролізу вишневого клею або бурячного жому. Дріжджі арабінозу не зброджують, людський організм її не засвоює.
Рибоза відіграє дуже важливу роль у живих організмах. Вона входить до складу РНК, нуклеотидів, вітамінів, коферментів. її фосфорні ефіри беруть участь в обміні вуглеводів. Зустрічається рибоза у фуранозній формі. Ізомер рибози, її кетоформа – рибулоза у вигляді фосфорного ефіру бере участь в обміні вуглеводів, а її подвійний ефір – рибулозобісфосфат є акцептором СО2 при фотосинтезі.
Гексози, поряд з пентозами, найбільш поширені моносахариди у рослинах. Це глюкоза, фруктоза, галактоза, маноза.
Глюкоза (декстроза, або виноградний цукор) – найпоширеніший у природі моносахарид. У вільному стані глюкоза міститься в зелених частинах рослин, у насінні, ягодах, фруктах, складає половину від загальної кількості цукрів нектару і меду. Глюкоза входить до складу олігосахаридів (сахароза, мальтоза, рафіноза), багатьох вищих полісахаридів (крохмаль, глікоген, целюлоза, ліхенін), глікопротеїдів, деяких ліпоїдів, багатьох глікозидів. Фосфорні ефіри глюкози беруть участь у метаболізмі вуглеводів. Глюкоза зброджується дріжджами і добре засвоюється тваринним організмом. Кут питомого обертання глюкози +52,5°.
Глюкозу одержують шляхом гідролізу крохмалю, частіше кукурудзяного або рисового. Глюкозу широко застосовують: вона є частиною нашої їжі (фрукти, мед), використовується у харчовій промисловості та медицині. Так, глюкоза складає велику частку патоки, що застосовується в кондитерській промисловості. З неї в промислових масштабах синтезують вітамін С. На глюкозі, яку одержують при гідролізі деревини, вирощують кормові дріжджі. Крім того, зброджуючи таку глюкозу, одержують гідролізний спирт, який використовують для технічних цілей.
Фруктоза (левулоза, плодовий цукор) – найважливіший представник кетоз. У природі вона зустрічається у фуранозній формі в основному у вигляді β-стереоізомера. Обертає площину поляризації вліво, кут питомого обертання -–92,4°. Фруктоза є найсолодшим цукром. Вона міститься у всіх зелених частинах рослин, у плодах, складає половину цукрів нектару і меду. її фосфорні ефіри беруть участь в обміні вуглеводів. Фруктоза входить до складу олігосахаридів (сахароза, рафіноза), вищих полісахаридів (інулін), глікопротеїдів, глікозидів. Одержують фруктозу шляхом гідролізу інуліну. Вона зброджується дріжджами і засвоюється тваринним організмом.
Галактоза у вільному стані в рослинах зустрічається вкрай рідко. Наприклад, у кристалічній формі вона виділяється на плодах плюща. Головним чином галактоза входить до складу олігосахаридів (лактоза, рафіноза), вищих полісахаридів (геміцелюлози, гумі, слизи), глікопротеїдів, глікозидів. Зброджується дріжджами.

Маноза у вільному стані майже не зустрічається. Звичайно вона входить до складу вищих полісахаридів (геміцелюлози, гумі, слизи), глікопротеїдів, глікозидів. Зброджується дріжджами.
Гептози. У рослинах поширена в основному одна гептоза – седогептулоза.

Седогептулоза в певних кількостях міститься в рослинах з родини товстянкових. Вперше її одержали з очитка (Sedum), звідси й назва. Фосфорні ефіри седогептулози беруть участь у перетворенні вуглеводів. Дріжджі седогептулозу не зброджують.
Октози і нанози. Ці моносахариди знайдені головним чином у плодах авокадо. Всі вони є кетозами. Прикладом октоз може бути гліцероманооктулоза, а наноз – еритрогулонанулоза.
Моносахариди з розгалуженим ланцюгом. Зазвичай моносахариди мають нерозгалужений ланцюг. Розгалужені цукри зустрічаються вкрай рідко і, як правило, у зв'язаному стані.
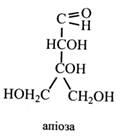
Апіоза – моносахарид, що входить до вкладу глікозиду апіїну, який міститься в рослині петрушки.
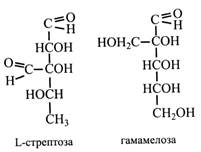
L-стрептоза має в розгалуженні альдегідну групу. Вона входить до складу антибіотика стрептоміцину. Ще однією особливістю стрептози є відсутність кисню в 5-го вуглецевого атома, тобто вона являє собою дезоксицукор.
Гамамелоза у бічному ланцюжку має первинну спиртову групу. Вона входить до складу ряду дубильних речовин.
Дезоксицукри. У рослинах зустрічаються моносахариди, у яких при одному, рідше при двох, вуглецевих атомах відсутній кисень. Це дезоксицукри.
L-рамноза міститься в багатьох глікозидах, у гумі, слизах, у пектинових речовинах. У вільному стані рамноза зустрічається в листках сумаху.
Фукоза знайдена у водоростях (фукус, ламінарія), а також у глікозидах та деяких геміцелюлозах.

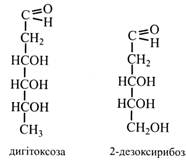
Дигітоксоза – двічі дезоксицукор, що міститься у глікозидах (наперстянка).
Дезоксирибоза у формі фосфорного ефіру входить до складу дезоксирибонуклеотидів ДНК.
Аміноцукри – це моносахариди, що містять аміногрупу. Наприклад, глюкозамін, галактозамін, у яких біля 2-го вуглецевого атома замість гідроксильної міститься аміногрупа.
У природі аміноцукри зустрічаються зазвичай у складі полісахаридів (хітин), глікопротеїдів, глікозидів. Вони мають сильно виражені основні властивості та можуть утворювати солі. У рослинах глюкозамін та інші аміносахариди знаходяться в основному у вигляді N-ацетильних похідних, тобто в аміногрупі один водень заміщений ацетильним залишком.
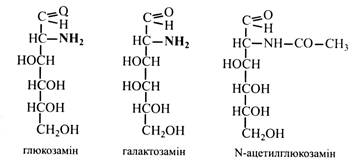
Деякі похідні моносахаридів
До них належать кислоти та багатоатомні спирти, що утворюються з моносахаридів, мають деякі спільні з ними властивості та беруть участь у їх метаболізмі.
Кислоти виникають при окисленні моносахаридів. Залежно від того, яка група в молекулі цукру окислюється, утворюються кислоти трьох типів:
1. При окисленні альдегідної групи до карбоксильної утворюються альбомові кислоти: з глюкози – глюконова, з галактози – галактонова, з рибози – рибонова тощо.
2. При одночасному окисленні альдегідної та первинної спиртової груп утворюються дикарбонові кислоти, що називаються альдаровими: з глюкози – глюкарова, з галактози – галактарова тощо.
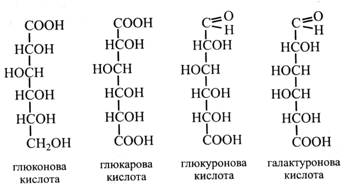
3. При окисленні тільки первинної спиртової групи утворюються альдокислоти – урокові кислоти: з глюкози – глюкуронова, з галактози – галактуронова, з манози – мануронова тощо.
Усі ці кислоти легко утворюються в рослинах і беруть участь у вуглеводному обміні, входять до складу деяких полісахаридів (геміцелюлози, гумі, слизи), глікопротеїдів, глікозидів.
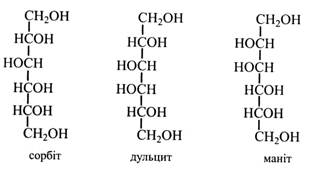
Багатоатомні спирти утворюються в рослинах шляхом відновлення моносахаридів, їх альдо- або кетогруп. Найбільш поширені в рослинах сорбіт, маніт, дульцит (галактит).
Сорбіт виникає при відновленні глюкози і фруктози. Він дуже поширений у рослинах. Багато його в плодах – фруктах і ягодах (яблука, груші, сливи, вишні, абрикоси, персики). Особливо багато сорбіту в плодах горобини – до 7 %, звідки його було вперше виділено.
Маніт утворюється при відновленні манози або фруктози. Його багато в овочах і плодах (морква, цибуля, оливки, ананаси), у грибах (до 11 %), у водоростях (5-20 %). Звичайно маніт одержують із морської капусти (бура водорость). Він виділяється на корі деяких дерев у вигляді «манни» (олива, деякі види ясена, тамарикса).
Дульцит (галактит) утворюється при відновленні галактози. Він міститься в багатьох рослинах і у виділеннях на корі та листках деяких дерев. Наприклад, «мадагаскарська манна» являє собою майже чистий дульцит.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 5534; Нарушение авторских прав?; Мы поможем в написании вашей работы!