
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Экологическая биотехнология
|
|
|
|
Традиционные биотехнологические процессы, основанные на брожении, дополняются новыми эффективными процессами получения белков, аминокислот, антибиотиков, ферментов, витаминов, органических кислот и др. Наступила эра новейшей биотехнологии, связанная с получением вакцин, гормонов, интерферонов и др.
Важнейшими задачами, стоящими перед биотехнологией сегодня, являются: повышение продуктивности сельскохозяйственных растительных культур и животных, создание новых пород культивируемых в сельском хозяйстве видов, защита окружающей среды и утилизация отходов, создание новых экологически чистых процессов преобразования энергии и получения минеральных ресурсов. Характеризуя перспективы и роль биотехнологии в человеческом обществе, уместно прибегнуть к высказыванию на одном из Симпозиумов по биотехнологии японского профессора К. Сакагучи, который говорил следующее: «... ищите все, что пожелаете, у микроорганизмов, и они не подведут вас... Изучение и применение в промышленности культур клеток млекопитающих и растений, иммобилизация не только одноклеточных, но и клеток многоклеточных организмов, развитие энзимологии, генетической инженерии, вмешательство в сложный и недостаточно изученный наследственный аппарат растений и животных все больше расширят области применения существующих направлений биотехнологии и создадут
принципиально новые направления».
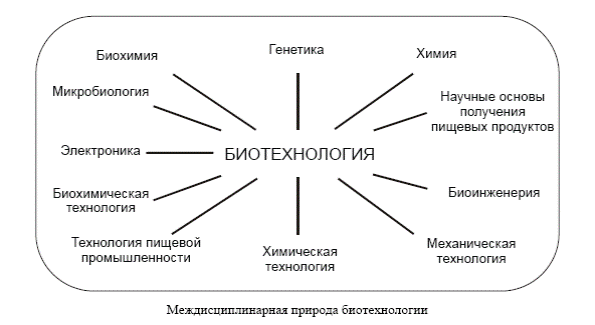
В современной биотехнологии в соответствии со спецификой сфер ее применения целесообразно выделить в качестве самостоятельных ряд разделов следующие:
•Промышленная микробиология;
•Медицинская биотехнология;
•Технологическая биоэнергетика,
•Сельскохозяйственная биотехнология;
•Биогидрометаллургия;
•Инженерная энзимология;
•Клеточная и генетическая инженерия;
Перспективность и эффективность применения биотехнологических процессов в различных сферах человеческой деятельности, от получения пищи и напитков до воспроизводства экологически чистых энергоносителей и новых материалов обусловлена их компактностью и одновременно крупномасштабностью, высоким уровнем механизации и производительности труда. Биологические технологии находятся в настоящее время в фазе бурного развития, но уровень их развития во многом определяется научно-техническим потенциалом страны.
Важнейшей задачей любого биотехнологического процесса является разработка и оптимизация научно-обоснованной технологии и аппаратуры для него. При организации биотехнологических производств частично был заимствован опыт развитой к тому времени химической технологии. Однако биотехнологические процессы имеют существенное отличие от химических в силу того, что в биотехнологии используют более сложную организацию материи – биологическую. Каждый биологический объект (клетка, фермент и т. д.) – это автономная саморегулирующаяся система.
Природа биологических процессов сложна и далеко не выяснена окончательно. Для микробных популяций, например, характерна существенная гетерогенность по ряду признаков – возраст, физиологическая активность, устойчивость к воздействию неблагоприятных факторов среды. Они также подвержены случайным мутациям, частота которых составляет от 10-4 до 10-8. Гетерогенность также может быть обусловлена наличием поверхностей раздела фаз и неоднородностью условий среды. В общем виде любой биотехнологический процесс включает три основные стадии: предферментационную, ферментационную и постферментационную. Принципиальная схема реализации биотехнологических процессов в общем виде может быть представлена блок-схемой, в которой сделана попытка охватить все варианты ферментационных процессов.


На предферментационной стадии осуществляют хранение и подготовку культуры продуцента (инокулята), получение и подготовку питательных субстратов и сред, ферментационной аппаратуры, технологической и рециркулируемой воды и воздуха. Поддержание и подготовка чистой культуры является очень важным моментом предферментационной стадии, так как продуцент, его физиолого-биохимические характеристики
и свойства определяют эффективность всего биотехнологического процесса. В отделении чистой культуры осуществляют хранение производственных штаммов и обеспечивают их реактивацию и наработку инокулята в количествах, требуемых для начала процесса. При выращивании посевных доз инокулята применяют принцип масштабирования, то есть проводят последовательное наращивание биомассы продуцента в колбах, бутылях, далее в серии последовательных ферментеров. Каждый последующий этап данного процесса отличается по объему от предыдущего обычно на порядок. Полученный инокулят по стерильной посевной линии направляется далее в аппарат, в котором реализуется ферментационная стадия. Приготовление питательных сред осуществляется в специальных реакторах, оборудованных мешалками. В зависимости от растворимости и совместимости компонентов сред могут быть применены отдельные реакторы. Технология приготовления сред значительно усложняется, если в их состав входят нерастворимые компоненты. В различных биотехнологических процессах применяются различные по происхождению и количествам субстраты, поэтому процесс их приготовления варьирует. Поэтому дозирование питательных компонентов подбирается и осуществляется индивидуально на каждом производстве в соответствии с Технологическим регламентом конкретного процесса. В качестве дозирующего оборудования при этом применяются весовые и объемные устройства, используемые в пищевой и химической промышленности. Транспорт веществ осуществляется насосами, ленточными и шнековыми транспортерами. Сыпучие компоненты подают в ферментеры с помощью вакуумных насосов. Часто применяют принцип предварительных смесей, то есть соли предварительно растворяют и затем транспортируют по трубопроводам, дозируя их подачу по объему. В силу исключительного разнообразия биотехнологических процессов и применяемых для их реализации сред, методов и аппаратуры рассмотрение данных элементов далее будет связано с конкретными биотехнологическими производствами.
Стадия ферментации является основной стадией в биотехнологическом процессе, так как в ее ходе происходит взаимодействие продуцента с субстратом и образование целевых продуктов (биомасс, эндо- и экзопродуктов). Эта стадия осуществляется в биохимическом реакторе (ферментере) и может быть организована в зависимости от особенностей используемого продуцента и требований к типу и качеству конечного продукта различными способами. Ферментация может проходить в строго асептических условиях и без соблюдения правил стерильности (так называемая «незащищенная» ферментация); на жидких и на твердых средах; анаэробно и аэробно. Аэробная ферментация, в свою очередь, может протекать поверхностно или глубинно (во всей толще питательной среды). Культивирование биологических объектов может осуществляться в периодическом и проточном режимах, полунепрерывно с подпиткой
субстратом. При периодическом способе культивирования ферментер заполняется исходной питательной средой и инокулятом микроорганизмов. В течение определенного периода времени в аппарате происходит взаимодействие микроорганизмов и субстрат сопровождающееся образованием в культуре продукта (Х + S → P). Биохимические превращения в этом аппарате продолжаются от десятков часов до нескольких суток. Регуляция условий внутри ферментера важнейшая задача периодического культивирования микроорганизмов. В ходе периодической ферментации выращиваемая культура проходит ряд последовательных стадий: лаг-фазу, экспоненциальную, замедления роста,стационарную и отмирания. При этом происходят существенные изменения физиологического состояния биообъекта, а также ряда параметров среды. Целевые продукты образуются в экспоненциальной (первичные метаболиты – ферменты, аминокислоты, витамины) и стационарной (вторичные метаболиты – антибиотики) фазах, поэтому в зависимости от целей биотехнологического процесса в современных промышленных процессах применяют принцип дифференцированных режимов культивирования. В результате этого создаются условия для максимальной продукции того или иного целевого продукта. Периодически ферментер опорожняют, производят выделение и очистку продукта, и начинается новый цикл. Непрерывный процесс культивирования микроорганизмов обладает существенными преимуществами перед периодическим. Непрерывная ферментация осуществляется в условиях установившегося режима, когда микробная популяция и ее продукты наиболее однородны. Применение непрерывных процессов ферментации создает условия для эффективного регулирования и управления процессами биосинтеза. Системы непрерывной ферментации могут быть организованы по принципу полного вытеснения или полного смешения. Первый пример – так называемая тубулярная культура. Процесс ферментации осуществляется в длинной трубе, в которую с одного конца непрерывно поступают питательные компоненты и инокулят, а с другой с той же скоростью вытекает культуральная жидкость. Данная система проточной ферментации является гетерогенной. При непрерывной ферментации в ферментах полного смешения (гомогенно-проточный способ) во всей массе ферментационного аппарата создаются одинаковые условия. Применение таких систем ферментации позволяет эффективно управлять отдельными стадиями, а также всем биотехнологическим процессом и стабилизировать продуцент в практически любом, требуемом экспериментатору или биотехнологу состоянии. Управление подобными установками осуществляется двумя способами. Турбидостатный способ базируется на измерении мутности выходящего потока. Измерение мутности микробной суспензии, вызванное ростом клеток, является мерой скорости роста, с которой микроорганизмы выходят из биореактора. Это позволяет регулировать скорость поступления в ферментер свежей питательной среды. Второй метод контроля, – хемостатный, проще. Управление процессом в хемостате осуществляется измерением не выходящего, а входящего потока. При этом концентрацию одного из компонентов питательной среды (углерод, кислород, азот), поступающего в ферментер, устанавливают на таком уровне, при котором другие питательные компоненты находятся в избытке, то есть лимитирующая концентрация задающегося биогенного элемента ограничивает скорость размножения клеток в культуре. Обеспечение процесса ферментации, с точки зрения инженерной реализации, сводится к дозированному поступлению в ферментер потоков(инокулята, воздуха (или газовых смесей), питательных биогенов, пеногасителей) и отвода из него тепла, отработанного воздуха, культуральной жидкости, а также измерению и стабилизации основных параметров процесса на уровне, требуемом для оптимального развития продуцента и образования целевого продукта. В ходе ферментации образуются сложные смеси, содержащие клетки, внеклеточные метаболиты, остаточные концентрации исходного субстрата. При этом целевые продукты, как правило, находятся в этой смеси в небольших концентрациях, а многие из них легко разрушаются. Все это накладывает существенные ограничения на методы выделения и сушки биологических препаратов.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 4843; Нарушение авторских прав?; Мы поможем в написании вашей работы!