
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Квантовые свойства света и строение атома
|
|
|
|
Лекция 4
1. Квантовые свойства света. Тепловое излучение тел, его характеристики. Черное тело. Закон Кирхофа. Формула Планка. Закон Стефана-Больцмана. Закон Вина.
2. Использование излучения тела человека в диагностике. Понятие термографии и тепловидения.
3. Строение атома (ядерная модель). Недостатки Резерфордовской модели атома. Спектры излучения разреженных газов. Спектральный анализ, его использование в медицине.
4. Дискретность энергетических состояний атома. Постулаты Бора.
5. Квантовая теория строения атома водорода по Бору.
1. Квантовые свойства света. Тепловое излучение тел, его законы.
Из всего многообразия электромагнитных излучений, видимых и невидимых человеческим глазом, можно выделить одно, которое присуще всем телам. Это излучение нагретых тел, или тепловое излучение. Оно возникает при любых температурах выше 0К, поэтому испускается всеми телами. В зависимости от температуры тела изменяются интенсивность излучения и спектральный состав.
Среднюю мощность излучения за время, значительно большее периода световых колебаний, принимают за поток излучения Ф.
Поток излучения, испускаемый 1м2 поверхности, называется энергетической светимостью. Она выражается в Вт/м2.
Энергетическая светимость, соответствующая интервалу длин волн от 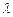 до
до 
 (1)
(1)
Где  -cпектральная плотность энергетической светимости тела, равная отношению энергетической светимости узкого участка спектра к ширине этого участка.
-cпектральная плотность энергетической светимости тела, равная отношению энергетической светимости узкого участка спектра к ширине этого участка.
Зависимость спектральной плотности энергетической светимости от длины волны называют спектром излучения тела.
Способность тела поглощать энергию излучения характеризуется коэффициентом поглощения, равным отношению потока излучения, поглощенного данным телом, к потоку излучения, упавшего на него:
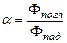 (2)
(2)
Монохроматический коэффициент поглощения определяется как
 (3)
(3)
Тело коэффициент поглощения, которого равен единице для всех частот, называют абсолютно черным.
Абсолютно черного тела в природе нет, но существуют их подобия: замкнутая непрерывная полость с малым отверстием, глазок мартеновской печи, сажа и т.д.
Луч, попавший в отверстие многократно отразившись от стенок, почти полностью будет поглощен.

Тело, коэффициент которого меньше единицы и не зависит от длины волны света, падающего на него называют серым.
Тело человека иногда считают серым, имеющим коэффициент поглощения ≈0,9 в инфракрасной части спектра.
Закон Кирхгофа: при одинаковой температуре отношение спектральной плотности энергетической светимости к монохроматическому коэффициенту поглощения одинаково для любых тел, в том числе и для черных:
 (4)
(4)
Где  -спектральная плотность энергетической светимости абсолютно черного тела.
-спектральная плотность энергетической светимости абсолютно черного тела.
Излучение абсолютно черного тела имеет сплошной спектр. Существует максимум спектральной плотности энергетической светимости, который с повышением температуры смещается в сторону коротких волн. Энергетическая светимость абсолютно черного тела Re можно найти как площадь, ограниченную крикой и осью абсцисс, или
 (5)
(5)
Энергетическая светимость увеличивается по мере нагревания абсолютно черного тела. Зависимость спектральной плотности энергетической светимости абсолютно черного тела от температуры описывается формулой Планка, который высказал гипотезу о квантовом характере излучения и поглощения энергии:
 (6)
(6)
Где h-постоянная Планка, k-постоянная Больцмана, T-абсолютная температура, 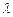 -длина волны излучения, с –скорость света в вакууме.
-длина волны излучения, с –скорость света в вакууме.
Закон Стефана-Больцмана: энергетическая светимость абсолютно черного тела пропорциональна четвертой степени его абсолютной температуры:
 (7)
(7)
 -постоянная Стефана-Больцмана
-постоянная Стефана-Больцмана
Закон смещения Вина: длина волны, соответствующая максимуму излучения абсолютно черного тела обратно пропорциональна его абсолютной температуре:
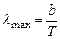 (8)
(8)
Где b-постоянная Вина.

Термография- это регистрация излучения различных участков поверхности тела с целью диагностической интерпретации. Определение температуры осуществляется жидкокристаллическими индикаторами, оптические свойства которых очень чувствительны к небольшим изменениям температуры. Другой метод основан на применении тепловизоров, в которых используются чувствительные приемники инфракрасного излучения.
В основе термографии лежит явление увеличения интенсивности ИК –излучения над патологическими очагами. Обычно это проявляется появлением «горячей зоны».
Термографическая диагностика не оказывает никакого внешнего воздействия или неудобства для пациента и позволяет «увидеть» аномалии тепловой картины на коже пациента, которые характерны для многих заболеваний и физических расстройств.
Примеры решения задач
1. При регистрации излучения тела человека в области горячей зоны было обнаружено локальное повышение температуры на 1º по сравнению с температурой здоровой ткани, которая составляла 36ºС. На сколько при этом сместился максимум спектральной плотности энергетической светимости?
Решение
В соответствии с законом Вина 
 . Изменение длины волны излучения
. Изменение длины волны излучения
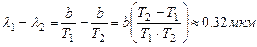
2. Приемник тепловизора может зарегистрировать изменение энергетической светимости поверхности объекта в 0,3%. Способен ли он зарегистрировать изменение температуры поверхности ладони на 1º?. Температуру ладони принять равной 30ºС.
Решение
Полная лучесипускательная способность или энергетическая светимость теплового излучения в соответствии с законом Стефана-Больцмана прямо пропорциональна его абсолютной температуре: 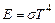 .Для двух значений температур запишем:
.Для двух значений температур запишем:
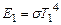 ;
; 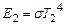
Из приведенных выражений можно найти относительное изменение энергетической светимости:
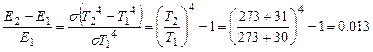
Что соответствует изменению указанной величина на 1,3%. Т.о., чувствительность приемника тепловизора достаточна для регистрации подобных изменений температуры.
3. Строение атома.
В 1911г. Резерфорд предложил ядерную модель атома, согласно которой весь положительный заряд и почти вся масса (>99,94%) атома сосредоточены в атомном ядре, размер которого ничтожно мал (~10-13см) по сравнению с размером атома 10-8см. Вокруг ядра по замкнутым (эллиптическим) орбитам движутся электроны, образуя электронную оболочку атома. Заряд ядра равен по абсолютной величине суммарному заряду электронов.
Предположение о вращении электронов вокруг ядра Резерфорд сделал в связи с тем, что согласно теореме Ирншоу, атом в виде статической системы не может быть устойчивым.
Предположение о наличии в центре атома одного массивного, но весьма малого ядра, Резерфорд доказал экспериментально в опыте по рассеянию альфа-частиц.
Однако резерфордовская модель строения атома не укладывалась в рамки законов классической физики. Действительно, согласно законам классической электродинамики, электрон, вращаясь вокруг ядра (с ускорением) должен непрерывно излучать э/м волны, частота которых равна частоте вращения электрона. Теряя энергию, электрон должен постепенно приближаться к ядру, двигаясь по спирали, и в конце концов упасть на ядро. По мере приближения электрона к ядру частота вращения электрона, а также частота э/м излучения должны непрерывно изменяться. Следовательно, атом должен давать сплошной спектр излучения.
Т.о., с точки зрения классической физики атом оказывается неустойчивой системой, дающей сплошной спектр излучения. Между тем, и то, и другое противоречит опыту, так как атомы весьма устойчивы и имеют линейный спектр излучения.
Спектры излучения разреженных газов
Исследование спектров излучения разреженных газов показали, что каждому газу присущ вполне определенный линейчатый спектр, а спектральные линии можно распределить по группам (сериям). Линии, принадлежащие к одной серии, связанны между собой определенной закономерностью. Так например, в видимой части спектра излучения водорода Бальмер обнаружил серию линий, частота которых выражается эмпирической формулой
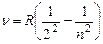 (9)
(9)
Где n=3,4,5.., R=3,29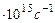 -постояннаяРидберга
-постояннаяРидберга


В ультрафиолетовой части спектра расположена серия Лаймана, частота линий которой определяется как
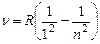 , где n=2.3.4…(10)
, где n=2.3.4…(10)
В инфракрасной области расположена серия Пашена:
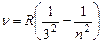 , где n=4,5,6…(11)
, где n=4,5,6…(11)
Различают три основных вида спектров: линейчатые- излучаются отдельными возбужденными атомами при переходе электронов на более низкие энергетические уровни;
Полосатые-излучаются возбужденными молекулами при переходе электронов в атомах и вследствие колебательных движений атомов в молекуле;
Сплошные-излучаются совокупностями многих взаимодействующих между собой молекулярных и атомных ионов. Основную роль играют хаотические движения частиц, обусловленных высокой температурой.
Спектральный анализ. Каждый химический элемент испускает (поглощает) свет с определенными длинами волн. Линейчатые спектры элементов получают путем фотографирования в спектрографах, в которых разложение света осуществляется с помощью дифракционной решетки. Линейчатый спектр «элемента»-это его своеобразный «отпечаток пальца», который позволяет безошибочно идентифицировать этот элемент на основе длин волн излучаемого (поглощаемого) света. Спекторграфические исследования являются одним из наиболее мощных методов химического анализа.
Качественный спектральный анализ-это сравнение полученных спектров с табличными для определения состава вещества.
Количественный спектральный анализ проводится путем фотометрирования (определения интенсивности) спектральных линий: яркость линий пропорциональна количеству данного элемента
Чувствительность спектрального анализа очень высока (~10-3-10-6%).
Спектральный анализ в медицине.
СА используется для диагностики микро- и макро-элементов. Он дает полные сведения о минеральном балансе за продолжительный период времени. Некоторые токсичные вещества можно обнаружить только этим способом. Результаты СА помогают врачу в диагностике и поиске причины заболеваний, выявлении скрытых заболеваний и предрасположенности к ним; позволяют более точно назначать лекарственные препараты и разрабатывать индивидуальные схемы восстановления минерального баланса.
В фармакологии СА позволяет проводить анализ проб фармакологических препаратов при их вомидации, а также определении фальсифицированных препаратов. В токсикологии УФ и ИК спектроскопии позволили проводить идентификацию многих алкалоидов из экстрактов Стаса.
4. Дискретность энергетических состояний атома. Постулаты Бора.
Линейчатый характер спектров излучения и поглощения атомов свидетельствует о том, что атом может излучать (поглощать) энергию не в любых количествах, а только вполне определенными порциями (квантами).
Исходя из представления о дискретности энергетических состояний атома Н.Бор в 1913 г. усовершенствовал атомную модель Резерфорда, создав квантовую теорию строения атома. В ее основу положены 3 постулата:
1. Электроны могут двигаться в атоме не по любым орбитам, а только по орбитам вполне определенного радиуса. На этих орбитах, называемых стационарными, момент количества движения электрона
 (12) –условие квантования
(12) –условие квантования
Где m-масса электрона, 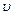 -его скорость,r-радиус орбиты, n-квантовое число (n=1.2.3…)
-его скорость,r-радиус орбиты, n-квантовое число (n=1.2.3…)
2. Движение электронов по стационарным орбитам не сопровождается излучением(поглощением) энергии.
3. Переход электрона с одной стационарной орбиты на другую сопровождается излучением (поглощения) кванта энергии.
Величина 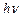 этого кванта равна разности энергий (W1 и W2) стационарных состояний атома до и после излучения (поглощения):
этого кванта равна разности энергий (W1 и W2) стационарных состояний атома до и после излучения (поглощения):
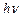 = W1-W2 (13)-условие частоты
= W1-W2 (13)-условие частоты
Т.о., частота э/м волн, излучаемых атомом, определяется не частотой вращения электронов в атоме, а разностью энергий стационарных состояний атома.
Постулаты Бора, сохранив в основном модель атома Резерфорда, вместе с тем освободили ее от упомянутых выше недостатков (противоречий опыту).
4. Квантовая теория строения атома водорода.
В атоме водорода вокруг ядра (протона), несущего заряд e, движется один электрон. Ядро можно считать неподвижным, поскольку его масса в 1840 раз больше массы электрона; орбиты электрона в первом приближении можно считать круговыми.
Центростремительной силой, удерживающей электрон на орбите радиусом r, является кулоновская сила притяжения между электроном и ядром:
 (14)
(14)
m-масса электрона, 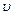 -его скорость,
-его скорость,
Решая (14) совместно с (12), получим выражение для радиуса стационарных орбит атома водорода
 (15)
(15)
Где n=1,2,..Для n=1, r1≈0.53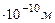
Полная энергия W электрона в атоме слагается из кинетической энергии Wк поступательного движения электрона по орбите и потенциальной энергии Wп притяжения электрона к ядру.
Учитывая (14), получим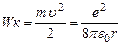 (16)
(16)
Потенциальная энергия должна быть отрицательна и равна
 (17)
(17)
 (18)
(18)
Т.е. полная энергия электрона оказывается отрицательной и равной по абсолютной величине его кинетической энергии. Подставляя в (18) выражение для r из (15), получим
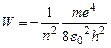 (19)
(19)
По этой формуле можно рассчитать энергию электрона для любой стационарной орбиты.
Величина полной энергии электрона, находящегося на стационарной орбите, называется уровнем энергии атома.
Согласно (19), энергия атома возрастает с увеличением квантового числа n, или с увеличением радиуса электронной орбиты. Так как W отрицательна, уменьшение ее абсолютной величины соответствует возрастанию энергии.
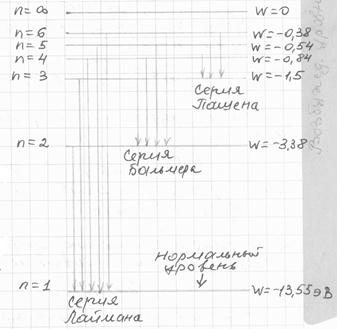
Энергетический уровень W=-13,55эВ называется нормальным уровнем, все остальные уровни называются возбужденными.
Выведем общую формулу для частоты 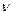 излучения атома. Для этого (19) подставим в (13):
излучения атома. Для этого (19) подставим в (13):
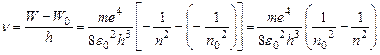 (20)
(20)
Где n.Wсоответствуют начальным состояниям атома (до излучения)
А n0.W0 –после излучения
 (21) –постоянная Ридберга
(21) –постоянная Ридберга
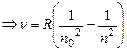 (22)
(22)
Эмпирические формулы (9),(10) и (11) являются частными случаями (22).
Примеры решения задач
1.Вычислить радиус первой орбиты атома водорода и скорость электрона на этой орбите
Решение: Радиус первой орбиты вычисляется по формуле (15) для n=1:
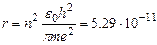
Для определения скорости воспользуемся выражением (12)


После расчетов получаем 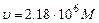 м/с.
м/с.
2. Определить энергию фотона при переходе с одной орбиты на другую
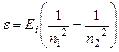 , где Ei-энергия ионизации атома водорода, n1- номер орбиты, на которую переходит электрон, n2-номер орбиты, с которой переходит электрон
, где Ei-энергия ионизации атома водорода, n1- номер орбиты, на которую переходит электрон, n2-номер орбиты, с которой переходит электрон
Получаем для серии Пашена n1=3, для второй линии этой серии m=2, n2=n1+m=3+2=5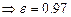 эВ
эВ
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 785; Нарушение авторских прав?; Мы поможем в написании вашей работы!