
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электрохимические реакции
|
|
|
|
Проводники первого и второго рода
Ранее, при рассмотрении составных частей электрохимических систем, были использованы такие понятия, как проводники первого и второго рода. Разберем эти понятия поподробнее.
Твердые и жидкие проводники, прохождение через которые электрического тока не вызывает переноса вещества в виде ионов, называются проводниками первого рода. Электрический ток в проводниках первого рода осуществляется потоком электронов (электронная проводимость). К таким проводникам относятся твёрдые и жидкие металлы и некоторые неметаллы (графит, сульфиды цинка и свинца). Их удельное сопротивление r лежит в пределах 10–8 – 10–5 Ом×м. Температурный коэффициент проводимости отрицателен, то есть с ростом температуры электропроводность уменьшается.
Вещества, прохождение через которые электрического тока вызывает передвижение вещества в виде ионов (ионная проводимость), называются проводниками второго рода. Типичными проводниками второго рода являются растворы солей, кислот и оснований в воде и некоторых других растворителях (10–2 £ r £ 104 Ом×м), расплавленные соли (10–3 < r < 10–1 Ом×м) и некоторые твёрдые соли (101 £ r £ 106 Ом×м). Температурный коэффициент электропроводности положителен. Как правило, в проводниках второго рода электричество переносится положительными (катионы) и отрицательными (анионы) ионами, однако некоторые твёрдые соли характеризуются униполярной проводимостью, то есть переносчиками тока в них являются ионы только одного знака - катионы (например, в AgCl) или анионы (BaCl2, ZrO2+CaO, растворы щёлочных металлов в жидком аммиаке).
Деление проводников в зависимости от типа проводимости (электронная или ионная) является условным. Известны твёрдые вещества со смешанной проводимостью, например Ag2S, ZnO, Cu2O и др. В некоторых солях при нагревании наблюдается переход от ионной проводимости к смешанной (CuCl).
Проводники второго рода называются электролитами. Это могут быть чистые вещества или растворы. Часто электролитами называют вещества, растворы которых проводят электрический ток. Эти растворы называют растворами электролитов.
Электрохимические реакции протекают на границе электрод (проводник первого рода) - электролит (проводник второго рода). Они вызваны невозможностью для электронов - носителей тока в электродах свободно двигаться в электролите. Эти реакции состоят в обмене электронами между электродом и ионами (молекулами) в растворе, при этом ионы (молекулы) теряют или изменяют свой электрический заряд. Это - первичная электрохимическая реакция, продукты которой нередко вступают в дальнейшие реакции, не связанные непосредственно с переносом тока ионами. Примерами катодных реакций могут служить следующие реакции:
Cu2+ + 2e ® Cu (1)
Fe3+ + e ® Fe2+ (2)
2H3O+ + 2e ® H2(г) + 2H2O (3)
На аноде могут протекать реакции типа:
4OH– ® O2 + 2H2O + 4e (4)
Fe2+ ® Fe3+ + e (5)
2Cl– ® Cl2(г) + 2e (6)
Zn ® Zn2+ + 2e (7)
Материал электрода может участвовать в электрохимической реакции [реакция (7)], но может быть и инертным (остальные реакции). В последнем случае на поверхности электрода могут выделяться металлы [реакция (1)] или газы [реакции (3, 4, 6)]. Наконец, электрохимическая реакция может протекать и при отсутствии перехода ионов из раствора к электроду и обратно. В этих случаях перенос электричества осуществляют только электроны, но у поверхности электрода в растворе ионы изменяют свою валентность [реакции (2) и (5)]. Совокупность двух электрохимических реакций, из которых одна протекает на катоде, а другая - на аноде, даёт химическую реакцию электролиза или реакцию, протекающую в электрохимическом элементе:
Cu2+ + 2Cl– ® Cu(т) + Cl2 (1) + (6)
2H3O+ + 2OH– ® 1/2 O2 + H2 + 3H2O (3) + 1/2 (4)
или H2O ® 1/2 O2 + H2
Законы электролиза (законы Фарадея)
Поскольку прохождение электрического тока через электрохимические системы связано с химическими превращениями, между количеством протекающего электричества и количеством прореагировавших веществ должна существовать определенная зависимость. Она была открыта Фарадеем и получила свое выражение в первых количественных законах электрохимии, названных впоследствии законами Фарадея.
Первый закон Фарадея. Количества веществ, превращённых при электролизе, пропорциональны количеству электричества, прошедшего через электролит:
Dm = k э q = k э It,
Dm – количество прореагировавшего вещества; k э – некоторый коэффициент пропорциональности; q – количество электричества, равное произведению силы тока I на время t. Если q = It = 1, то Dm = k э, то есть коэффициент k э представляет собой количество вещества, прореагировавшего в результате протекания единицы количества электричества. Коэффициент k э называется электрохимическим эквивалентом.
Второй закон Фарадея отражает связь, существующую между количеством прореагировавшего вещества и его природой: при постоянном количестве прошедшего электричества массы различных веществ, испытывающие превращение у электродов (выделение из раствора, изменение валентности), пропорциональны химическим эквивалентам этих веществ:
Dm i /A i = const.
Можно объединить оба закона Фарадея в виде одного общего закона: для выделения или превращения с помощью тока 1 г-экв любого вещества (1/z моля вещества) необходимо всегда одно и то же количество электричества, называемое числом Фарадея (или фарадеем):
Dm = 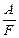 It =
It = 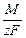 It.
It.
Точно измеренное значение числа Фарадея
F = 96484,52 ± 0,038 Кл/г-экв.
Таков заряд, несомый одним грамм-эквивалентом ионов любого вида. Умножив это число на z (число элементарных зарядов иона), получим количество электричества, которое несёт 1 г-ион. Разделив число Фарадея на число Авогадро, получим заряд одного одновалентного иона, равный заряду электрона:
e = 96484,52 / (6,022035×1023) = 1,6021913×10–19 Кл.
Законы, открытые Фарадеем в 1833 г., строго выполняются для проводников второго рода. Наблюдаемые отклонения от законов Фарадея являются кажущимися. Они часто связаны с наличием неучтённых параллельных электрохимических реакций. Отклонения от закона Фарадея в промышленных установках связаны с утечками тока, потерями вещества при разбрызгивании раствора и т.д. В технических установках отношение количества продукта, полученного при электролизе, к количеству, вычисленному на основе закона Фарадея, меньше единицы и называется выходом по току:
ВТ =  =
= 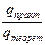 .
.
При тщательных лабораторных измерениях для однозначно протекающих электрохимических реакций выход по току равен единице (в пределах ошибок опыта). Закон Фарадея точно соблюдается, поэтому он лежит в основе самого точного метода измерения количества электричества, прошедшего через цепь, по количеству выделенного на электроде вещества. Для таких измерений используют кулонометры. В качестве кулонометров используют электрохимические системы, в которых нет параллельных электрохимических и побочных химических реакций. По методам определения количества образующихся веществ кулонометры подразделяют на электрогравиметрические, газовые и титрационные. Примером электрогравиметрических кулонометров являются серебряный и медный кулонометры. Действие серебряного кулонометра Ричардсона, представляющего собой электролизер
(–) AgïAgNO3×aqïAg (+),
основано на взвешивании массы серебра, осевшей на катоде во время электролиза. При пропускании 96500 Кл (1 фарадея) электричества на катоде выделится 1 г-экв серебра (107 г). При пропускании n F электричества на катоде выделяется экспериментально определенная масса (D m к ). Число пропущенных фарадеев электричества определяется из соотношения
n = D m /107.
Аналогичен принцип действия медного кулонометра.
В газовых кулонометрах продуктами электролиза являются газы, и количества выделяющихся на электродах веществ определяют измерением их объемов. Примером прибора такого типа является газовый кулонометр, основанный на реакции электролиза воды. При электролизе на катоде выделяется водород:
2Н2О + 2 е – = 2ОН– + Н2,
а на аноде – кислород:
Н2О = 2Н+ + ½ О2 + 2 е –
Число фарадеев электричества, прошедшее через раствор, равно
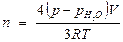 ,
,
где р – внешнее давление, Па; 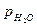 – давление насыщенного пара воды при температуре опыта, Па; V – суммарный объем выделенного газа, м3 .
– давление насыщенного пара воды при температуре опыта, Па; V – суммарный объем выделенного газа, м3 .
В титрационных кулонометрах количество вещества, образовавшегося в процессе электролиза, определяют титриметрически. К этому типу кулонометров относится титрационный кулонометр Кистяковского, представляющий собой электрохимическую систему
(–) PtïKNO3 , HNO3ïAg (+).
В процессе электролиза серебряный анод растворяется, образуя ионы серебра, которые оттитровывают. Число фарадеев электричества определяют по формуле
n = mVc,
где m – масса раствора, г; V – объем титранта, пошедший на титрование 1 г анодной жидкости; c – концентрация титранта, г-экв/см3 .
Лекция 46
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 3297; Нарушение авторских прав?; Мы поможем в написании вашей работы!