
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Растворимость твердых веществ в жидкостях
|
|
|
|
Растворимость твердых веществ также определяется природой растворителя и растворенного вещества и также зависит от температуры. В отличие от растворимости газов, растворимость твердых тел сравнительно мало изменяется с давлением.
Различия в растворимости твердых тел можно иллюстрировать примерами. В 100 г воды при 25°С растворяется 257 г AgNO3 и лишь 3•10-20 HgI. Вода — хороший растворитель сахара, а спирт его практически не растворяет. Нафталин очень хорошо растворяется в спирте и не растворим в воде.
Следует заметить, что вследствие отсутствия общей теории растворов вопрос о зависимости растворимости от физико-химических свойств растворителя и растворенного вещества еще нельзя считать до конца решенным, и конкретные сведения о растворимости твердых тел целиком основаны на опытных данных.
В настоящее время установлен ряд правил о растворимости веществ, но они не обладают универсальностью, не свободны от различного рода исключений и потому носят в большинстве случаев качественный характер. Например, было замечено, что неполярные растворители, как правило, хорошо растворяют полярные вещества и плохо неполярные. Неполярные растворители, наоборот, хорошо растворяют, неполярные, вещества и плохо — полярные. В том случае, если один из компонентов раствора полярен, а второй неполярен, растворимость бывает незначительной.
Растворимость большинства твердых веществ с повышением температуры увеличивается. однако бывают и исключения. Так, растворимость СаCrО4 и Са(ОН)2 в воде с повышением температуры уменьшается.
Зависимость растворимости от температуры обычно изображают в виде кривых растворимости. На рис. 4 СЛ. 6 приведены кривые растворимости некоторых солей в воде.
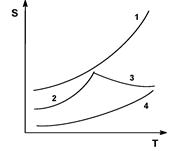
Рис. 4. Зависимость растворимости солей в воде от температуры. 1 – KNO3, 2 – Na2SO4*10H2O, 3 – Na2SO4, 4 – Ba(NO3)2.
Резкий излом на кривой растворимости сульфата натрия соответствует превращению Na2SO4•10Н2O в безводный Na2SO4. Растворение кристаллогидрата Na2SO4•10Н2O сопровождается поглощением тепла, а растворение безводной соли идет с выделением тепла.
Если соль способна к образованию кристаллогидратов (рис. 5 СЛ. 7), то химический состав и область существования каждого кристаллогидрата можно сравнительно легко определить по характерным кривым растворимости: каждой точке перехода соответствует излом на кривой растворимости.

Рис. 5. Зависимость растворимости ZnCl2 в воде от температуры.
Изменением растворимости с температурой часто используются для очистки веществ путем перекристаллизации. При остывании горячего насыщенного раствора, какой либо соли, загрязненной примесями, значительная часть соли выделится осадок, а загрязняющие примеси остаются в растворе, так как последний даже на холоде не будет насыщенным раствором по отношению к примесям.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 958; Нарушение авторских прав?; Мы поможем в написании вашей работы!