
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Влияние химического состава на структуру и свойства
|
|
|
|
Сталь 12ХГФЛ ГОСТ 21357-87.
В сталях содержится много разных элементов. Все они оказывают на структуру и свойства стали то или иное влияние, которое нельзя игнорировать. Компоненты стали можно разделить на 3 группы: 1) постоянные компоненты; 2) элементы примеси; 3) легирующие элементы.
Постоянными компонентами стали являются C (до 1,5 %), Si (до 0,52 %) и Mn (до 0,9 %). В качестве элементов-примесей в сталях всегда присутствуют S и P, а также газы – кислород, азот и водород. Легирующими элементами являются Cr, Ni, Cu, Mo, Co, V, Zr, W, Nb, Ti, Al, B и другие элементы, а также Si и Mn свыше указанных выше концентраций.
Углерод оказывает решающее влияние на структуру и свойства углеродистых и легированных конструкционных сталей (Рис. 2.1).
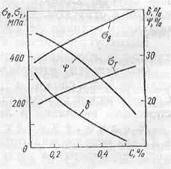
Рис. 2.1.1 Влияние углерода на механические свойства литейной конструкционной нелегированной стали (после нормализации)
С увеличением содержания углерода до эвтектоидного состава в структуре стали прочность и твердость стали возрастает, а пластические свойства, наоборот, снижаются. Это обусловлено тем, что при этом увеличивается доля прочной составляющей перлита и уменьшается доля пластичной составляющей феррита. В заэвтектоидной области с увеличением содержания углерода в стали твердость продолжает возрастать, хоть и менее интенсивно, прочность снижается, как и пластические свойства. Такое изменение свойств стали связано с соответствующим появлением и увеличением в структуре стали доли вторичного цементита, который выделяется по границам перлитных (бывших аустенитных) зерен.
Кремний в обычных концентрациях (0,20-0,52 %) стали является раскислителем стали. Одновременно он упрочняет феррит, т. к. входит в состав низкотемпературного твёрдого раствора углерода в α-Fe. Поэтому с увеличением его концентрации в стали прочность повышается, а пластичность падает.
Марганец в обычных концентрациях (0,45-0,90 %) вводят в сталь для раскисления и устранения нежелательного влияния серы. Он частично замещает железо в цементите, но в основном присутствует в растворенном состоянии в феррите, способствуя некоторому повышению прочности стали.
Сера является нежелательной примесью, так каквызывает красноломкость стали, т. е высокотемпературную её хрупкость. Последнее обусловлено тем, что сера практически не растворяется вγ-Fe, но образуетс железом сульфид FeS. Вследствие этого при кристаллизации стали формируется легкоплавкая эвтектика (γ-Fe + FeS) с температурой плавления 988 0С. Она располагается по границам аустенитных зёрен. Это способствует межзёренному разрушению стали и образованию горячих трещин при затруднённой усадке отливки. Красноломкость может быть устранена за счет связывания серы в сульфид марганца MnS. Для этого содержание марганца должно в 1,71 превышать содержание серы в стали, но фактически это превышение составляет не менее 8-10. Однако, сера и в связанном состоянии является нежелательной примесью, так как включения MnS повышают загрязненность стали неметаллическими включениями и ухудшают её свойства. Поэтому содержание серы ограничивают в пределах 0,020-0,060 % в зависимости от требований к отливкам.
Фосфор также является нежелательной примесью, так как вызывает хладноломкость стали. При небольших его содержаниях он полностью растворяется в феррите. Это способствует повышению его прочности и снижению пластичности, особенно при низких температурах. С увеличение содержания фосфора температура перехода твердого раствора в хрупкое состояние повышается, т. е хладностойкость стали снижается. С увеличением содержания углерода вредное влияние фосфора усиливается. Это обусловлено тем, что C и P, являются конкурентами как элементы, образующие с железом твёрдые растворы внедрения. Поэтому с увеличением содержания углерода в стали фосфор вытесняется из твёрдого раствора. В этих условиях при повышенных содержаниях фосфора избыточное его количество связывается железом в фосфид Fe3P, который, располагаясь по границам зерен, способствует хрупкому межзеренному разрушению стали. Поэтому в отливках общего назначения допускается Р ≤ 0,030-0,050 %, в отливках ответственного и особо ответственного назначения допустимое содержание фосфора Р ≤ 0,025 %, а в хладностойких сталях - Р ≤ 0,020 %.
Газовые примеси ( водород, азот и кислород) попадают в сталь из шихты и из атмосферы плавильного агрегата. Водород в жидкой стали присутствуют в растворенном (атомарном) состоянии. Но при её кристаллизации и последующем охлаждении вследствие изменения растворимости часть водорода выделяется в свободном (молекулярном) состоянии. Это сопровождается формированием в отливках газовых дефектов (раковин, пористости, флокенов). Поэтому в стали содержание водорода желательно иметь ниже 2,5·10-4 %. Азот в жидкой стали также, как правило, присутствует в растворенном (атомарном) состоянии. При кристаллизации и последующем охлаждении стали вследствие снижения растворимости избыточный азот выделяется из раствора в свободном (молекулярном) состоянии с формированием газовых дефектов. Если в стали содержатся нитридообразующие элементы (Al, Ti, Zr, V и Nb), то азот может быть связан в нитриды. Тогда вероятность формирования в стальных отливках газовых дефектов снижается. Кислород в жидкой нераскисленной стали присутствует в растворенном (атомарном) состоянии. При кристаллизации стали содержание растворенного кислорода уменьшается. Сверхравновесно растворенный кислород связывается в оксид (FeO) и монооксид углерода по реакции [C] + [O] = {CO]. Результатом протекания последней реакции является формирование в стальных отливках газовых раковин. Для предотвращения этого стали для отливок всегда раскисляют элементами с высоким сродством к кислороду (Si, Al, Ca и др.). Тогда реакции образования FeO и CO подавляются и в стали образуются включения SiO2, Al2O3, CaO и др.
Легирующие элементы, за исключением бора, образуют с железом твердые растворы замещения. Поэтому они оказывают влияние на положение точек А3 и А4 на диаграмме состояния Fe-Fe3C и таким образом определяют область существования α-Fe (феррита) и γ-Fe (аустенита). По этому показателю легирующие элементы можно разделить на две группы:
~ элементы, повышающие точку А4 и понижающие точку А3 (Ni, Cu, Mn, C, N), расширяют область существования аустенита до широких интервалов концентраций легирующих элементов и обеспечивают получение аустенитной структуры стали при комнатной и отрицательной температурах;
~ элементы, сужающие область устойчивости аустенита (Al, Si, V, Cr, Mo, W, Ti, P и др.), наоборот, расширят область устойчивости феррита и обеспечивают получение ферритной структуры стали при комнатной и отрицательной температурах.
Легирующие элементы в жидкой стали находятся в растворенном состоянии, но в твердой стали они могут присутствовать в различных формах состояния:
- в растворенном в железе состоянии;
- в карбидах, нитридах и интерметаллидах;
- в неметаллических (оксидных, сульфидных, окси-сульфидных) включениях.
Легирующие элементы, расположенные в Периодической системе левее железа, распределяются между твердым раствором на основе железа и неметаллическими фазами (карбидами, нитридами, оксиды, сульфиды и т.д.). А легирующие элементы, расположенные в Периодической системе правее железа, не образуют неметаллических фаз и потому присутствуют только твердом растворе на основе железа.
Эффективность легирования тем выше, чем большая часть легирующего элемента находится в составе твердого раствора. Легирующие элементы имеют атомные размеры отличные от железа. Поэтому при растворении легирующих элементов параметры кристаллической решётки железа изменяются. Чем сильнее искажается кристаллическая решётка, тем выше эффект упрочнения твердого раствора. Изменение периода кристаллической решетки при легировании феррита описывается следующей зависимостью:
Δ a = Σ(Ka,i · CЛЭ),
где Δ a – изменение периода решётки железа при образовании легированного феррита;
Ka,i – коэффициент удельного изменения периода решётки железа при растворении в нем 1 % i-того легирующего элемента;
CЛЭ – содержание легирующего элемента.
Эффект упрочнения легированного феррита можно аналогично количественно оценить, считая вклад легирующих элементов при этом аддитивным:
Δ σ т = Σ(Kσ i · CЛЭ),
где Δ σ т – прирост предела текучести феррита, МПа;
Kσi – коэффициент упрочнения феррита или прирост его предела текучести при растворении в нем 1 % i-того легирующего элемента, МПа / %.
Значения Kσi для некоторых легирующих элементов приведены ниже:
Элемент i: C+N P Si Ti Al Cu Mn Cr Ni Mo V
Kσi, МПа / %: 4670 690 85 80 60 40 35 30 30 10 2
Аналогичные закономерности упрочнения наблюдаются при легировании аустенита. (Рис. 2.1.2). При этом элементы, образующие твердые растворы внедрения (C, N) сильнее упрочняют аустенит, чем элементы, образующие с железом твердые растворы замещения.
Элементы с кристаллической решёткой, родственной γ-Fe (ГЦК) – Ni, Cu, Al, Mn и др., способствуют формированию в структуре стали аустенита или продуктов его распада.
Элементы с кристаллической решёткой, родственной α-Fe (ОЦК) – Cr, V, Mo, Nb, W и др., а также Si способствуют стабилизации в структуре стали феррита.
Карбидообразующие элементы (Mn, Cr, Mo, W, Nb, V, Zr, Ti) образуют карбиды или участвуют вместе с железом в их образовании. Некарбидообразующие элементы (Ni, Co, Al, Si, Cu) растворяются в железе и понижают устойчивость цементита и карбидов других элементов, способствуют их распаду при термической обработке (отжиге).
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 2577; Нарушение авторских прав?; Мы поможем в написании вашей работы!