
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Механические и технологические свойства конструкционных материалов. Детали машин чрезвычайно разнообразны и для их изготовления необходимы материалы с самыми различными свойствами
|
|
|
|
Детали машин чрезвычайно разнообразны и для их изготовления необходимы материалы с самыми различными свойствами. Требования к материалам особенно возросли в эпоху научно-технического прогресса. В некоторых случаях для изготовления изделий необходимы материалы с повышенной коррозионной стойкостью, теплопроводностью и электропроводностью, особыми магнитными свойствами, тугоплавкостью, сверхпроводимостью и т. п. Для правильного использования имеющихся материалов, также как и для обработки деталей из них, важно иметь представление об их структуре, так как это даст возможность учитывать влияние режимов эксплуатации или обработки на те или иные характеристики изделия.
Металлические и большинство неметаллических твердых материалов имеют кристаллическое строение. Характерными признаками кристаллических тел являются способность сохранять свою форму и оставаться твердыми при нагреве вплоть до критической температуры, при которой они дискретно переходят в жидкое состояние. Переход кристаллических тел из твердого в жидкое состояние и наоборот совершается изотермически, т. е. при определенной температуре, называемой температурой плавления.
Элементарные частицы, из которых состоят кристаллические тела (атомы, ионы, молекулы) расположены в пространстве упорядоченно и образуют кристаллические решетки. В кристаллической решетке можно выделить элементарный объем, многократно повторяющийся и состоящий из минимального количества элементарных частиц, — элементарную ячейку; совокупность этих ячеек характеризует особенности строения кристаллического тела данного типа. Элементарные частицы в кристаллической решетке находятся во взаимодействии, определяемым их электронным строением. От характера этого взаимодействия зависят электрические, магнитные, тепловые и оптические свойства материала, его температуры плавления и испарения, модуль упругости и другие свойства.
Металлы — кристаллические тела, атомы которых располагаются в геометрически правильном порядке, образуя кристаллы, в отличие от аморфных тел (например, смола), атомы которых находятся в беспорядочном состоянии.
Располагаясь в металлах в строгом порядке, атомы в плоскости образуют атомную сетку, а в пространстве — атомно-кристаллическую решетку. Линии на этих схемах являются условными; в действительности никаких линий не существует, а атомы колеблются возле точек равновесия, т. е. узлов решетки с большой частотой. Элементарные ячейки таких кристаллических решеток приведены на рис. 1. Все кристаллические тела образуют семь разновидностей кристаллических решеток, из которых для металлов наиболее характерны объемно-центрированная кубическая (ОЦК), гранецентрированная кубическая (ГЦК) и гексагональная плотноупакованная (ГПУ) (рис. 1)
В ячейке кубической объемно-центрированной решетки атомы расположены в вершинах куба и в центре куба; такую решетку имеют хром, ванадий, вольфрам, молибден и др. В ячейке кубической гранецентрированной решетки атомы расположены в вершинах и в центре каждой грани куба; такую решетку имеют алюминий, никель, медь, свинец и др. В ячейке гексагональной решетки атомы расположены в вершинах шестиугольных оснований призмы, в центре этих оснований и внутри призмы; гексагональную решетку имеют магний, титан, цинк и др. В реальном металле кристаллическая решетка состоит из огромного количества ячеек.
Размеры кристаллической решетки характеризуются ее параметрами, измеряемыми в ангстремах — А (1А = 10 -8 см или lA = 0,1 Нм). Параметр кубической решетки характеризуется длиной ребра куба, обозначается буквой а и находится в пределах 0,28—0,6 Нм (2,8 — 6А). Для характеристики гексагональной решетки принимают два параметра — сторону шестигранника а и высоту призмы с. Когда отношение с/а -- 1,633, то атомы упакованы наиболее плотно, и поэтому такая решетка называется гексагональной плотноупакованной.
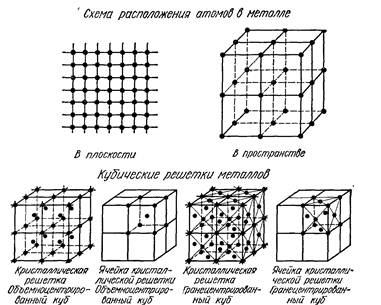
Рис.1. Атомно-кристаллическое строение металлов.
Свойства кристалла определяются не только типом кристаллической решетки, но и характером взаимодействия атомов, ионов и электронов между собой. При переходе паров металла в жидкость, а затем в твердое состояние его атомы сближаются настолько, что валентные электроны получают возможность переходить от одного атома к другому и свободно перемещаться, таким образом, по всему объему металла, обеспечивая высокую электро- и теплопроводность. Между электронами и положительными ионами возникают силы электрического взаимодействия.

|
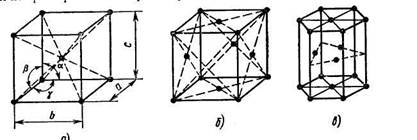
Рис. 2. Схемы кристаллических решеток:
а – объемно-центрированная кубическая; б — гранецентрированная кубическая; в — гексагональная плотноупакованная.
В зависимости от температуры и давления многие металлы могут образовывать различные типы кристаллических решеток. Эта способность металлов носит название полиморфизма или аллотропии. Полиморфные превращения свойственны таким широко применяемым в машиностроении металлам, как Fe, Ti, Mn, Co, Sn. Полиморфные модификации элементов обычно обозначают, начиная с наиболее низкотемпературны, буквами α, β, γ, δ и т. д. Так например: железо при нагреве до температуры 910 °С образует модификацию α-Fe с ОЦК-решеткой, в интервале 910—1400 °С — γ-Fe с ГЦК-решеткой и свыше 1400 °С — δ-Fe с решеткой ОЦК. При этом происходит существенное изменение свойств материала. Это явление широко используют в технике для улучшения обрабатываемости металлов, при их термообработке и других процессах.
Для характеристики формы и размера элементарной ячейки кристаллической решетки используют (рис.2) шесть основных параметров: расстояния по осям координат — a, b, c называемые периодом решетки, и три угла — α, β, γ между этими отрезками. Кроме основных параметров в кристаллографии приняты еще другие, дополнительно характеризующие кристаллическую решетку.
В различных плоскостях кристаллической решетки атомы расположены с различной плотностью и поэтому многие свойства кристаллов в различных направлениях различны. Такое различие называется анизотропией.
Все кристаллы анизотропны. В отличие от кристаллов аморфные тела (например, смола) в различных направлениях имеют в основном одинаковую плотность атомов и, следовательно, одинаковые свойства, т. е. они изотропны.
В металлах, состоящих из большого количества по-разному ориентированных мелких анизотропных кристаллов (поликристалл), свойства во всех направлениях одинаковы (усредненные). Эта кажущаяся независимость свойств от направления называется квазиизотропией *.
Если в структуре металла создается одинаковая ориентировка кристаллов, то появляется анизотропия.
При переходе металла из жидкого состояния в твердое происходит так называемый процесс кристаллизации. Основы теории кристаллизации разработаны основоположником науки о металлах — металловедения Д. К. Черновым, который установил, что кристаллизация состоит из двух процессов: зарождения мельчайших частиц кристаллов (зародышей кристаллизации) и роста кристаллов из этих центров (рис.3).
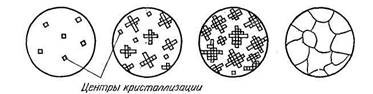
Рис.3. Последовательные этапы процесса кристаллизации.
Рост кристаллов заключается в том, что к их зародышам присоединяются все новые атомы жидкого металла. Сначала кристаллы растут свободно, сохраняя правильную геометрическую форму, но это происходит только до момента встречи растущих кристаллов. В месте соприкосновения кристаллов рост отдельных их граней прекращается и развиваются не все, а только некоторые грани кристаллов. В результате кристаллы не имеют правильной геометрической формы. Такие кристаллы называют кристаллитами или зернами. Величина зерен зависит от числа центров кристаллизации и скорости роста кристаллов. Чем больше центров кристаллизации, тем больше кристаллов образуется в данном объеме и каждый кристалл (зерно) меньше. На образование центров кристаллизации влияет скорость охлаждения. Чем больше скорость охлаждения металла, тем больше возникает в нем центров кристаллизации, и зерна получаются мельче (рис.4). Это подтверждается на практике в тонких сечениях литых деталей охлаждающихся более быстро, металл всегда получается более мелкозернистым, чем в толстых массивных литых деталях, охлаждающихся медленнее. Однако не всегда можно регулировать скорость охлаждения.
Всем кристаллам присуща анизотропия, т. е. неравномерность свойств по направлениям, определяемая различными расстояниями между атомами в кристаллической ячейке. Наиболее сильно анизотропия выражена у металлов, имеющих асимметричное кристаллическое строение. От направления действия сил в кристалле существенно зависят такие показатели физических свойств, как прочностные характеристики, модуль упругости, термический коэффициент расширения, коэффициенты тепло- и электропроводности, показатель светового преломления и др. Анизотропия характерна и для поверхностных слоев кристаллов. Такие свойства, как поверхностное натяжение, электронные потенциалы, адсорбционная способность, химическая активность существенно различаются у различных граней кристалла.

Рис.4. Влияние скорости охлаждения на возникновение центров кристаллизации и на величину образующихся зерен.
1 - медленное охлаждение, 2 – ускоренное охлаждение, 3 – быстрое охлаждение.
Строение и свойства реальных кристаллов отличаются от идеальных, представленных на рис. 1, вследствие наличия в них дефектов, которые подразделяют на поверхностные и внутренние. Реальный единичный кристалл обладает свободной (наружной) поверхностью, на которой уже вследствие поверхностного натяжения решетка будет искажена. Это искажение может распространяться и на прилегающую к поверхности зону.
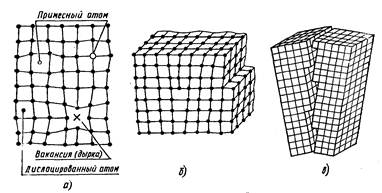
Рис.5. Дефекты кристаллической решетки:
а — точечные; б — линейные; в - двухмерные (плоскостные)
Дефекты внутреннего строения подразделяют на нульмерные (точечные), одномерные — линейные и двухмерные, т. е. развитые в двух направлениях. К точечным дефектам относятся: вакансии в случае, когда отдельные узлы кристаллической решетки не заняты атомами; дислоцированные атомы, когда отдельные атомы оказываются в междуузлиях, или примесные атомы, количество которых даже в чистых металлах весьма велико. Около таких дефектов решетка будет упруго-искаженной на расстоянии одного-двух ее периодов (рис. 5, а). Хотя относительная концентрация точечных дефектов может быть невелика, они вызывают чрезвычайно большие изменения физических свойств материала. Например, тысячные доли атомного процента примесей к чистым полупроводниковым кристаллам изменяют их электрическое сопротивление в 105—108 раз.
Линейные дефекты малы в двух измерениях кристаллической решетки и достаточно велики в третьем. К таким дефектам относятся смещения атомных плоскостей или дислокации и цепочки вакансий (рис. 5, б). Важнейшим свойством таких дефектов является их подвижность внутри кристалла и активное взаимодействие между собой и с другими дефектами.
Плотность дислокаций в кристаллах велика: в недеформированных кристаллах их количество на 1 см3 достигает 106—108; при пластической деформации происходит возникновение новых дислокаций, и это число увеличивается в тысячи раз. Двухмерные дефекты характерны для поликристаллических материалов, т. е. для материалов, состоящих из большого количества мелких кристаллов, различно ориентированных в пространстве.
Граница сросшихся при затвердевании кристаллов представляет собой тонкую, до 10 атомных диаметров, зону с нарушением порядка в расположении атомов. В поликристаллическом теле границы отдельных кристаллов имеют криволинейные поверхности раздела, а сами кристаллы — неправильную форму. Поэтому их, в отличие от правильно ограниченных кристаллов, называют кристаллитами или зернами. Зерна поликристалла при затвердевании растут из различных центров кристаллизации и ориентация осей кристаллических решеток соседних зерен различна. Зерно металла состоит из отдельных блоков, ориентированных один по отношению к другому под небольшим углом. Границы между ними представляют собой обычно скопления дислокаций (рис. 5, в). Поверхностные дефекты малы только в одном направлении; в двух других они могут достигать размера кристаллита.
Влияние дефектов строения на свойства материалов огромно. Например, прочность реальных кристаллов на сдвиг из-за наличия дефектов строения уменьшается на три-четыре порядка по сравнению с той же характеристикой идеального кристалла. Влияние дефектов строения на прочностные характеристики металлов не однозначно. Из представленной на рис. 6 зависимости видно, что прочность практически бездефектных кристаллов (так называемых «усов») очень высока. Увеличение количества п дефектов строения в 1 см3 приводит к резкому снижению прочности (ветвь А). Точка Рк характеризует прочность металлов, которые принято называть «чистыми». Дальнейшее увеличение дефектов, например, введением легирующих примесей или методами специального искажения кристаллической решетки повышает реальную прочность металлов (ветвь В). Для создания наиболее прочных материалов стараются получить оптимальное количество дефектов. Наибольшее упрочнение достигается при плотности дислокаций 1012 —1018 на 1 см3.

Рис. 6. Зависимость прочности кристаллического тела от плотности дефектов строения
Кроме влияния на прочностные характеристики дефекты решетки играют большую роль в процессах диффузии и самодиффузии, которые во многом определяют скорости протекания химических реакций в твердом теле, а также ионную проводимость кристаллов. Дефекты кристаллической решетки, распределенные необходимым образом по объему кристалла, позволяют создавать в одном образце области с различными типами проводимости, что является необходимым при изготовлении некоторых полупроводниковых элементов.
В технике значительно чаще применяют не чистые металлы, а сплавы, состоящие из двух или нескольких элементов, называемых компонентами. В качестве компонентов сплавов могут быть как чистые элементы, так и химические соединения. Широкое применение сплавов в качестве машиностроительных материалов можно объяснить тем, что они обладают разнообразным комплексом свойств, которые могут быть направленно изменены в зависимости от количества и вида компонентов, а также с помощью термической или других видов обработки.

Рис. 7. Виды кристаллических решеток сплавов.
а — твердый раствор замещения; б — твердый раствор внедрения; в — химическое соединение
При сплавлении компоненты образуют в сплаве фазы — однородные объемы, разграниченные друг от друга поверхностями раздела — границами, при переходе через которые свойства могут изменяться скачкообразно. В сплавах образуются следующие основные фазы: твердые растворы, химические соединения и механические смеси.
Твердые растворы являются наиболее распространенной фазой в металлических сплавах. Характерной особенностью их строения является сохранение кристаллической решетки металла-растворителя. Растворенные металлы могут быть распределены в ней в виде твердого раствора замещения (рис. 7, а) в том случае, если у обоих компонентов однотипные решетки, достаточно близкие атомные радиусы и физико-химические свойства, или в виде твердого раствора внедрения (рис. 7, б), если атомный радиус растворенного компонента достаточно мал.
Химические соединения обычно образуются между металлами и неметаллами и обладают свойствами неметаллических включений, а также между металлами. При этом образуется новый тип кристаллической решетки, отличной от решеток составляющих компонентов и обладающий другими свойствами (рис.7, в). При сплавлении компонентов с весьма различными атомными радиусами и электрохимическими свойствами взаимная растворимость практически отсутствует. В этом случае образуется механическая смесь кристаллов компонентов.
. Как правило, в многокомпонентных металлических сплавах можно одновременно встретить три вида фаз. Направленным изменением сочетания компонентов в сплавах можно изменять количество дефектов строения и, следовательно, управлять физико-механическими характеристиками.
При выборе материала для конструкции исходят из комплекса свойств, которые подразделяют на механические, физико-химические, технологические и эксплуатационные. К основным механическим свойствам относят прочность, пластичность, ударную вязкость, усталостную прочность, ползучесть, твердость и износостойкость. Под прочностью понимают способность материала сопротивляться деформации или разрушению под действием статических или динамических нагрузок. При статических нагрузках производят испытания на растяжение, сжатие, изгиб и кручение. Показателем прочности является предел прочности образца испытуемого металла, приведенного на рис. 9, а.
 ,
,
где Р — нагрузка, необходимая для разрушения стандартного образца, МН; F0 — площадь поперечного сечения образца в мм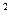 .
.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 511; Нарушение авторских прав?; Мы поможем в написании вашей работы!