
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Получение. 1) Выделение из аммиачной воды, образующейся при сухой перегонке каменноугольной смолы
|
|
|
|
1) Выделение из аммиачной воды, образующейся при сухой перегонке каменноугольной смолы.
2) Конденсация ацетилена и HCN.

| раскаленные
трубки

| 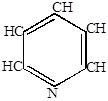
|
3) Синтез Ганца-Чичибабина – конденсация карбонильных соединений с аммиаком (наиболее распространенный промышленный метод синтеза соединений ряда пиридина).
 
| 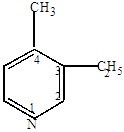
| (1) | ||
| 4-метил-3-этилпиридин | ||||
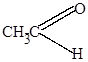
|
+ NH3  -4H2O
-4H2O
| |||
| ацетальдегид | 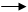
| 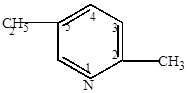
| (2) | |
| 2-метил-5-этилпиридин |
2-метил-5-этилпиридин нашел применение для получения мономера винилпиридиновых латексов.

| (Cr2O3 +
другие окислители)
T0
 -H2
-H2
| 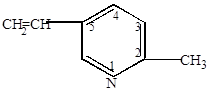
|
| 2-метил-5-винилпиридин |
| n |
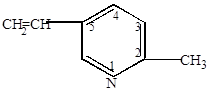
|
полимеризация

| 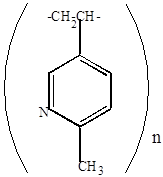
|
| поли-2-метил-5-винилпиридин |
Химические свойства пиридина сходны со свойствами бензола. Проявляет ароматические свойства (более ярко выраженные, чем у пятичленных гетероциклов), однако распределение электронной плотности в пиридине не вполне равномерное, он проявляет ненасыщенность в большей степени, чем бензол (но меньше, чем тиофен). Это вытекает из электронного строения пиридина. В кольце пиридина 3 двойные связи, 6 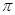 -электронов, образующих ароматический секстет. Поэтому неподеленная пара электронов азота мало участвует в сопряжении с
-электронов, образующих ароматический секстет. Поэтому неподеленная пара электронов азота мало участвует в сопряжении с 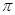 -электронами кольца. Поскольку азот обладает более высокой электроотрицательностью, чем углерод, электронное облако кольца оттянуто к азоту, и пиридин имеет дипольный момент, направленный к азоту.
-электронами кольца. Поскольку азот обладает более высокой электроотрицательностью, чем углерод, электронное облако кольца оттянуто к азоту, и пиридин имеет дипольный момент, направленный к азоту.
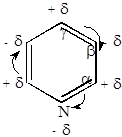
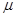 =2,2Д
=2,2Д
Самая высокая электронная плотность у азота. Электронная плотность в 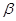 -положении выше, чем в
-положении выше, чем в 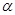 и
и 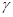 .
.
Химические реакции пиридина можно подразделить на следующие типы:
1) реакции аминного азота;
2) реакции электрофильного замещения в ядре;
3) реакции нуклеофильного замещения в ядре;
4) реакции окисления и восстановления.
1) реакции аминного типа
а) пиридин проявляет основные свойства благодаря наличию трехвалентного атома азота, имеющего неподеленную пару электронов. Однако, пиридин – основание менее сильное, чем пиперидин, но более сильное, чем анилин.
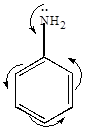
| 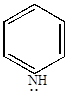
| 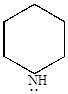
|
| Кд=4,0.10-10 | Кд=1,7.10-9 | Кд=1,33.10-3 |
р-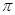 -сопряжение
-сопряжение
Основность пиридина
Меньшая основность пиридина по сравнению с (СН3)N объясняется различием в гибридизации: в (СН3)N азот находится в состоянии sp3-гибридизации, а в пиридине – в sp2-гибридизации (Веселовская, 1982г).
Доля s-электронов на орбите, занятой неподеленной парой электронов, больше при sp2-гибридизации, чем при sp3-гибридизации, а s-электронное облако менее вытянуто и прочнее удерживается ядром (при sp3-гибридизации неподеленная пара состоит из 1 s-электрона и 1 sp3-гибридного электрона, при sp2-гибридизации – из 1 s-электрона и 1 sp2-гибридного электрона, один р-электрон расположен перпендикулярно плоскости кольца и участвует в образовании ароматического секстета).
Например,
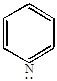
|
+ HCl 
| 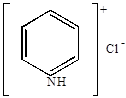
|
| хлористый пиридиний |
б) пиридин образует комплексные соли с галоидными алкилами.
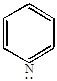
|
+ C2H5I 
| 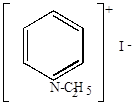
|
| йодистый этил | N-этилпиридинийиодид |
Эти соли непрочны, при нагревании изомеризуются с переходом радикала в положение 2 или 4 (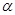 или
или 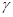 ).
).
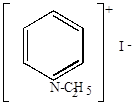
| T0
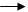 
| 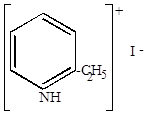
|
 -этилпиридинийиодид -этилпиридинийиодид
| ||
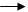
| 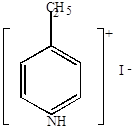
| |
 -этилпиридинийиодид -этилпиридинийиодид
|
2) Реакции электрофильного замещения
Пиридин труднее вступает в эти реакции, чем бензол. В большинстве случаев это вызывается промежуточным образованием катиона пиридиния, где атом азота несет положительный заряд и влияет на кольцо как заместитель второго рода.
Механизм электрофильного замещения.
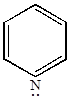
|
+X+
| 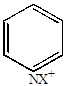
| +X+

| 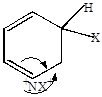
|
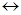
| 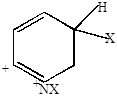
|
При присоединении в 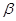 -положение резонансная стабилизация
-положение резонансная стабилизация 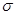 -комплекса не приводит к возникновению у азота 2-го положительного заряда.
-комплекса не приводит к возникновению у азота 2-го положительного заряда.
Если бы присоединение происходило в 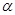 -положение
-положение

|
+X+
| 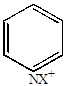
| +X+

| 
|
мало вероятно
Нитрование, сульфирование и др. идут при высоких температурах и в основном в положение 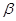 .
.
а) сульфирование
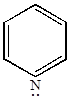
|
+ HOSO2OH 
| 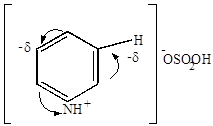
| HOSO2OH
дым.
 (HgSO4)
кат.
(HgSO4)
кат.
|
| катион пиридиния (кислый сернокислый пиридиний) | |||
 -H2O
-H2O
| 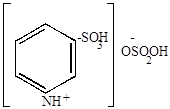
| ||
кислый сернокислый 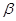 -пиридиний -пиридиний
|
б) нитрование
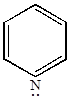
|
+HONO2 
| 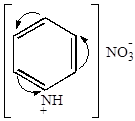
| HONO2
конц.
 3000
3000
| 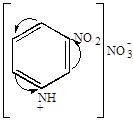
|
| азотнокислый пиридиний | азотнокислый
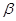 -нитропиридиний -нитропиридиний
|
При более высокой температуре образуются и другие изомеры.
3) Реакции нуклеофильного замещения
Благодаря электронооттягивающему действию азота ядро пиридина обедняется электронами, и атака нуклеофильных реагентов протекает легче, чем у бензола.
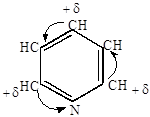
|
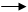  + KOH + KOH
| 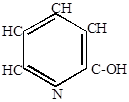
|
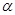 -оксипиридин -оксипиридин
| ||
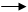
| 
| |
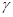 -оксипиридин -оксипиридин
|
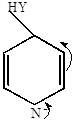
Механизм нуклеофильного замещения

|
+Y-
| 
|
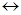
| 
|
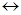
| 
|
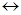
| 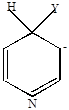
|

|
+Y-
| 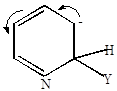
|
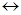
| 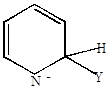
|
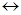
| 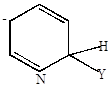
|
Граничные структуры (мезомерные формы аниона). Атака нуклеофильного реагента происходит в 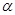 или
или 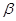 -положение, в которых легче образуется
-положение, в которых легче образуется 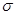 -комплекс, т.к. его стабилизация не связана с образованием мезомерных форм, имеющих отрицательные заряды рядом с азотом.
-комплекс, т.к. его стабилизация не связана с образованием мезомерных форм, имеющих отрицательные заряды рядом с азотом.
4) Реакции окисления и восстановления
а) Окисление пиридина происходит трудно. При определенных условиях реакция может идти с образованием N-окиси.
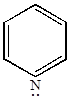
| + |
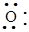  (H2O2 + CH3COOH)
(H2O2 + CH3COOH)
| 
|
Двойные связи при этом не затрагиваются. N-окись отличается от пиридина большей легкостью протекания реакций электрофильного замещения.
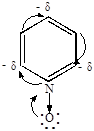
| 1000
+KNO3  (H2SO4 дым.)
(H2SO4 дым.)
| 
| +H2O + KHSO4 |
| N-окись паранитропиридина | кислый сернокислый калий |
При этом реакция идет в 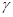 -положение вследствие сопряжения ненасыщенных пар электронов с
-положение вследствие сопряжения ненасыщенных пар электронов с 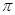 -электронами кольца.
-электронами кольца.
б) окисление гомологов пиридина протекает довольно легко за счет окисления боковой цепочки с образованием пиридинкарбоновых кислот.
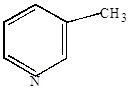
|
+ 3 O  (KMnO4) –H2O
(KMnO4) –H2O
| 
|
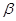 -пиколин -пиколин
| 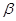 -пиридинкарбоновая кислота (никотиновая) -пиридинкарбоновая кислота (никотиновая)
|
в) восстановление пиридина протекает легче, чем у бензола.

|
+ 6 H (Na+C2H5OH)
(Na+C2H5OH)
| 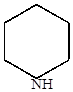
|
| пиперидин |
При более энергичном гидрировании молекулярным водородом в присутствии катализаторов Pt, Pd и температуре 1800С происходит раскрытие цикла.

| Pt, Pd
+ 4 H2  C5H11NH2
1800 C5H11NH2
1800
|
| амиламин |
Восстановление иодистым водородом приводит к отщеплению аммиака.

| 2800
+ 11 HI  C5H12 + NH4I + 5 I2 C5H12 + NH4I + 5 I2
|
| пентан йодистый аммоний |
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 565; Нарушение авторских прав?; Мы поможем в написании вашей работы!