
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства сопряженных диенов
|
|
|
|
Для всех типов диенов, как и для всех алифатических непредельных углеводородов, характерны реакции электрофильного присоединения, механизм которых был рассмотрен в разделе алкены. Сопряженные диены демонстрируют некоторые особенности протекания реакций AE.
Например, бромирование бутадиена в присутствии двух- и более кратного избытка брома приводит к присоединению четырех атомов галогена с образование 1,2,3,4-тетрабромбутана.

В условиях моноприсоединения (эквимолярная смесь бутадиена и брома) образуется не только 3,4-дибромбутен-1, но и 1,4-бутен-2. Соотношение изомеров зависит от температуры проведения реакции. При проведении реакции при -80оС основным продуктом реакции является 3,4-дибромбутен-1, а при +40оС – 1,4-дибромбутен-2. Причем, если смесь, полученную при низкой температуре, выдержать при +40оС, результат будет точно таким же, как если бы реакцию изначально проводили при +40оС.

Исследования реакций присоединения многочисленных реагентов с самыми разными сопряженными диенами показали, что такое поведение вообще характерно для сопряженных диенов, т.е. реагент может присоединяться не только к соседним углеродным атомам диенового фрагмента – 1,2-присоединение, но и концевым углеродам – 1,4-присоединение.

Для понимания химического поведения сопряженных диенов необходимо рассмотреть особенности механизма реакций электрофильного присоединения в этом гомологическом ряду.
Рассмотрим механизм присоединения хлористого водорода к гексадиену-2,4. Как было показано выше, реакции AE протекают как двухстадийный процесс, в котором первая стадия представляет собой присоединение электрофильной частицы с образованием наиболее стабильного карбокатиона.
Атака протона по p-электронам диенового фрагмента теоретически может привести к двум карбокатионам А и Б.
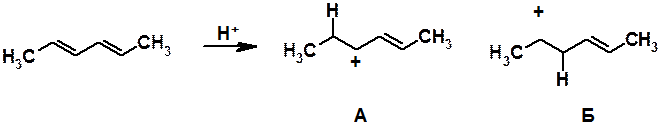
Оба катиона являются вторичными и, основываясь на этой характеристике, нельзя предсказать какой из них будет более устойчивым. Однако при внимательном рассмотрении структуры катионов можно заметить, что в катионе А вакантная орбиталь позитивированного атома углерода находится в сопряжении с электронами p-связи. Формула, приведенная выше, не отражает реального строения образующегося катиона. При атаке электрофила по концевому атому диенового фрагмента образуется катион, строение которого следует отображать с помощью набора граничных структур.
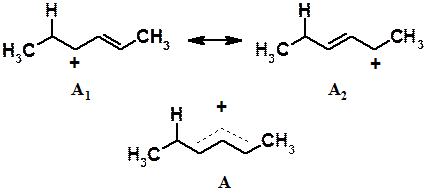
Реально образующийся карбокатион может быть отображен с помощью структуры А, в которой положительный заряд распределен между тремя атомами углерода, что приводит к уменьшению энергии (увеличению стабильности) промежуточного продукта. Таким образом, хотя катионы А и Б и являются вторичными, катион А более устойчив вследствие делокализации (так называемый аллильный карбокатион) и именно он образуется в результате взаимодействия с электрофилом. Далее анион хлора может присоединиться ко второму или четвертому углеродному атому диенового фрагмента с образованием соответственно 4-хлорбутена-2 и 2-хлорбутена-3.

Как было показано выше, соотношение изомеров в реакции бромирования бутадиена зависит от температуры проведения реакции. Каждый из изомеров устойчив при низкой температуре, но продолжительная выдержка любого из них при +40оС приводит к образованию смеси, содержащей 20% продукта 1,2- и 80 % продукта 1,4-присоединения. Имеющиеся данные позволяют сделать вывод, что получаемая при повышенной температуре смесь является равновесной смесью продуктов 1,2- и 1,4-присоединения, а повышенное содержание в ней 1,4-дибромбутена-2 должно быть объяснено большей устойчивостью промежуточно образующегося аллильного карбокатиона.
В целом 1,2- и 1,4-присоединение к сопряженным диенам является классическим случаем общего для органической химии явления – протекания параллельных реакций, одна из которых (1,2-присоединение) идет в условиях кинетического, а другая (1,4-присоединение) – термодинамического контроля (см. Введение). Все реакции электрофильного присоединения одной молекулы реагента к сопряженным диенам протекают подобным образом, отличаясь лишь температурными интервалами и соотношением продуктов 1,2- и 1,4-присоединения.
Результат гидрирования сопряженных диенов зависит от условий проведения реакции. Каталитическое гидрирование всегда протекает как 1,2-процесс, приводя в конце концов к алкану.

Гидрирование натрием в этаноле или в жидком аммиаке всегда протекает как 1,4-присоединение водорода.
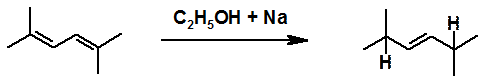
Поскольку алкены в этих условиях не вступают в реакцию гидрирования, образование алканов не происходит.
В 1928 г. О. Дильс и К. Альдер (Нобелевская премия 1950 г.) открыли реакцию своего имени или «реакцию диенового синтеза».
В реакции Дильса-Альдера взаимодействие сопряженного диена с диенофилом (соединением с активированной кратной связью) приводит к образованию шестичленного циклического алкена (аддукта).

Диены и диенофилы, не имеющие заместителей, вступают в реакцию с большим трудом. Бутадиен-1,3 реагирует с этиленом с низким выходом только при температуре более 200оС и давлении около 400 атм. В случаях, когда диен несет электронодонорные, а диенофил – электроноакцепторные заместители, реакция обычно протекает при комнатной температуре или незначительном нагревании с количественным выходом.
Эта реакция очень важна для препаративной органической химии, поскольку позволяет в одну стадию из простых исходных веществ получить сложные циклические соединения.
Реакция Дильса-Альдера классифицируют как [4+2]-циклоприсоединение. Это один из вариантов так называемых перициклических реакций, составляющих самостоятельный раздел органической химии.
В течение долгого времени реакцию Дильса-Альдера относили к так называемым «реакциям без механизма», поскольку никаких промежуточных продуктов в этом превращении не удавалось и до настоящего времени не удалось зафиксировать.
Несмотря на то, что, как видно из схемы, реакция представляет собой сложный процесс, в котором суммарно происходит разрыв трех p-связей и образование двух s- и одной p-связи, процесс является одностадийным, проходящим через единственное переходное состояние.
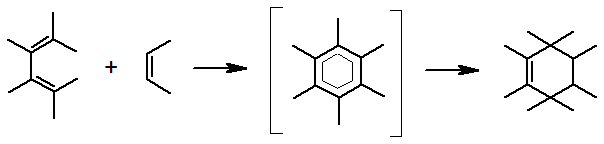
В циклическом переходном состоянии происходит согласованный процесс перераспределения электронной плотности. Атомы С-1 и С-4 диена, а также углероды кратной связи диенофила изменяют тригональную гибридизацию на тетраэдрическую, с образованием двух s-связей. Второй и третий атомы диена сохраняют начальную гибридизацию с образованием двойной связи. Так как s-связи энергетически выгоднее, чем p-связи, реакция протекает с выделением тепла.
Поскольку в сопряженных диенах связь С2-С3 имеет частично двоесвязанный характер благодаря сопряжению p-электронов, свободное вращение относительно этой связи затруднено. Сопряженные диены могут существовать в двух устойчивых s-цис - и s-транс -конформациях (s – от ангийского single).
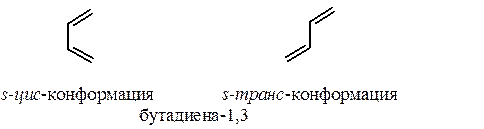
Согласованный процесс перераспределения электронной плотности в реакции Дильса-Альдера осуществляется только в том случае, если диен находится в s-цис- конформации.
В реакцию наряду с производными бутадиена-1,3 могут вступать циклические, гетероциклические диены, а также гетеродиены. Некоторые возможные структуры приведены ниже:

В качестве диенофилов наиболее часто используют малеиновый ангидрид, тетрацианэтилен, акриловую кислоту и ее производные – нитрил и эфиры.
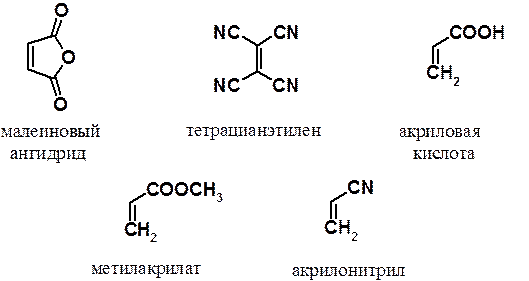
Кроме олефинов, в реакции Дильса-Альдера могут быть использованы алкины и соединения, имеющие двойную связь углерод-гетероатом. Например, следующие группировки:

|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 1530; Нарушение авторских прав?; Мы поможем в написании вашей работы!