
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Молекулярная диффузия
|
|
|
|
Молекулярной диффузией называется перенос распределяемого вещества, обусловленный беспорядочным движением самих молекул. Молекулярная диффузия описывается первым законом Фика, согласно которому количество вещества dM, продиффундировавшего за время dt через элементарную поверхность dF (нормальную к направлению диффузии), пропорционально градиенту концентрации dc/dn этого вещества:
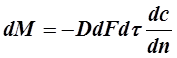 (2.1)
(2.1)
или
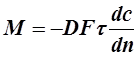 (2.2)
(2.2)
Из выражения (2.2.) следует, что удельный поток вещества, переносимого молекулярной диффузией через единицу поверхности (F=1) в единицу времени (t=1), или скорость молекулярной диффузии, составляет
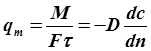 (2.3)
(2.3)
По своей структуре закон Фика аналогичен закону Фурье, описывающему передачу тепла теплопроводностью, причем аналогом градиента температур является в данном случае градиент концентраций, представляющий собой изменение концентрации диффундирующего вещества на единицу длины нормали между двумя поверхностями постоянных, но различных концентраций.
Коэффициент пропорциональности D в выражении закона Фика называется коэффициентом молекулярной диффузии, или просто коэффициентом диффузии. Знак минус перед правой частью первого закона Фика указывает на то, что молекулярная диффузия всегда протекает в направлении уменьшения концентрации распределяемого компонента.
Согласно уравнению (2.1), коэффициент диффузии выражается следующим образом:
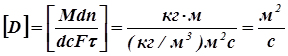
откуда (до сокращения одноименных величин) вытекает физический смысл D.
Коэффициент диффузии показывает, какое количество вещества диффундирует в единицу времени через единицу поверхности при градиенте концентрации, равном единице.
Возвращаясь к аналогии с теплопередачей, можно отметить, что коэффициент диффузии D является аналогом коэффициента температуропроводности а.
Коэффициент молекулярной диффузии представляет собой физическую константу, характеризующую способность данного вещества проникать вследствие диффузии в неподвижную среду. Величина D таким образом не зависит от гидродинамических условий, в которых протекает процесс.
Значения коэффициента диффузии D возрастают с увеличением температуры и давления. Обычно величина D возрастает с увеличением температуры и понижением давления (для газов). В каждом конкретном случае значение D определяют по опытным данным или по теоретическим и полуэмпирическим уравнениям с учетом температуры и давления, при которых протекает процесс диффузии.
Примером приближенной зависимости для расчета коэффициента молекулярной диффузии D газа А в газ В или в обратном направлении является следующее уравнение:
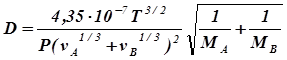 (2.4)
(2.4)
где D - коэффициент диффузии, м2/с;
Т - температура, К;
Р - давление (абсолютное), кгс/см2;
МА, МВ - мольные массы газов А и В;
vA, vB - мольные объемы газов А и В, определяемые как сумма
атомных объемов элементов, входящих в состав газа.
Мольные и атомные объемы различных веществ приводятся в справочниках (6,с.288).
Как следует из формулы (2.4), если известно значение коэффициента диффузии D1 при температуре Т1 и давлении Р1, то значение коэффициента диффузии D2 при температуре Т2 и давлении Р2 можно найти из уравнения:
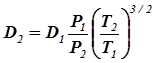 (2.5)
(2.5)
Значение коэффициентов диффузии в воздухе для некоторых газов и паров приведены в (6, табл.XLII, с.540)
Коэффициент диффузии газов или капельных жидкостей в жидкости при температуре 200С можно вычислить по следующей приближенной формуле:
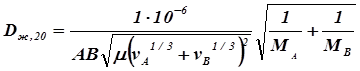 (2.6)
(2.6)
где m - динамический коэффициент вязкости жидкости, мПа×с;
А,В – коэффициенты, зависящие от свойств растворенного вещества
и растворителя.
Значения коэффициентов А и В для некоторых веществ, растворенных в воде представлены в (6, с.289).
Коэффициент диффузии газа в жидкости D t (при температуре t) cвязан с коэффициентом диффузии Dж20, (при температуре 200С) следующей приближенной зависимостью:
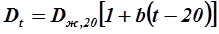 (2.7)
(2.7)
в которой температурный коэффициент b может быть определен по эмпирической формуле:
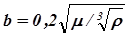 (2.8)
(2.8)
где m - динамический коэффициент вязкости жидкости при 200С, мПа×с;
r - плотность жидкости, кг/м3.
Значения коэффициентов диффузии некоторых газов в воде приведены в (6, табл.XLIII, с.540).
Коэффициенты диффузии газа в среду другого газа имеют значения 0,1 – 1 см2/с, а при диффузии газа в жидкость они в 104 – 105 раз меньше и составляют примерно 1 см2/сутки. Таким образом, молекулярная диффузия является весьма медленным процессом, особенно в жидкостях.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 13931; Нарушение авторских прав?; Мы поможем в написании вашей работы!