
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Явище амфотерності. Рівноваги у розчинах амфотерних сполук. Використання явища амфотерності в аналітичній хімії
|
|
|
|
До амфотерних відносять сполуки(амфоліти), які у розчинах поводять себе і як кислоти і як основи – гідроксиди деяких металів(Zn(OH)2, Cr(OH)3, Al(OH)3, Pb(OH)2, Sn(OH)2 та інші); аніони кислих солей (HCO-3, H2PO4- та інші). Якщо у розчині амфоліту присутній більш сильний донор протонів (кислота), то він веде себе як основа (акцептор протонів) і навпаки, в присутності більш сильного акцептора протонів (основи) амфоліт віддає свої протони поводячись як кислота.
Таким чином амфоліт у розчині може дисоціювати як кислота і як основа. Наприклад, для малорозчинного гідроксиду цинку, можливо представити рівноваги наступним чином:
Zn(OH)2 - осад
I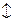 II
II
2H+ + ZnO22- 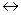 Zn(OH)2
Zn(OH)2 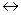 Zn2+ + 2OH-
Zn2+ + 2OH-
дисоціація по типу кислоти дисоціація по типу основи
Кожна з цих рівноваг характеризується своєю константою:
Kk = K1 =  ; Ko = KII =
; Ko = KII = 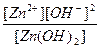 .
.
Порівнюючи константи рівноваги можливо передбачити які властивості амфоліту більш виражені. Якщо Кк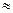 Ко то у амфоліту кислотні і основні властивості виражені приблизно однаково. Для Pb(OH)2 KPb(OH)2=9,6*10-4 > KH2PbO2 = 2*10-16 і більш виражені основні властивості. Для гідроксиду алюмінію KAl(OH)3=8*10-25 <KH3AlO3 = 4*10-13 більш виражені кислотні властивості.
Ко то у амфоліту кислотні і основні властивості виражені приблизно однаково. Для Pb(OH)2 KPb(OH)2=9,6*10-4 > KH2PbO2 = 2*10-16 і більш виражені основні властивості. Для гідроксиду алюмінію KAl(OH)3=8*10-25 <KH3AlO3 = 4*10-13 більш виражені кислотні властивості.
Завдяки наявності таких рівноваг амфоліт у розчині кислоти реагує як основа:
Zn(OH)2 + 2 H+ 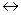 Zn2+ + H2O,
Zn2+ + H2O,
а у розчині лугу – як кислота:
H2ZnO2 + 2OH- 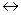 ZnO22- + H2O.
ZnO22- + H2O.
В обох випадках порушується рівновага, внаслідок чого цинк гідроксид буде розчинятися і в розчинах кислот і в розчинах луг.
Явище амфотерності широко використовується в аналітичній хімії для розділення катіонів. Наприклад, якщо аналізуєма суміш містить катіони Al3+ і Fe3+, то діючи лугом їх осаджують у вигляді гідроксидів, а додаючи надлишок лугу переводять амфотерний гідроксид алюмінію у розчин при цьому гідроксид феруму не розчиняється і залишається у осаду.
Контрольні питання до теми 1.9С
9.1.Які розчини звуться буферними?
9.2.Чим зумовлена дія буферної суміші при додаванні сильних кислот, основ, або розведенні?
9.3Що таке гідроліз солі?
9.4.Як гідролізується сіль, утворена катіоном сильної основи і аніоном сильної кислоти?
9.5Як гідролізується сіль, утворена катіоном слабкої основи і аніоном сильної кислоти?
9.6.Як гідролізується сіль, утворена катіоном сильної основи і аніоном слабкої кислоти?
9.7.Як гідролізується сіль, утворена катіоном слабкої основи і аніоном слабкої кислоти?
9.8.Які речовини відносять до амфолітів?
9.9.Як дисоціює амфоліт у розчині?
|
|
|
|
|
Дата добавления: 2014-01-15; Просмотров: 1632; Нарушение авторских прав?; Мы поможем в написании вашей работы!