
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Третий закон термодинамики
|
|
|
|
Энтропия изолированной системы, при наличии в ней неравновесных (необратимых) процессов, всегда возрастает.
Этот рост энтропии продолжается до тех пор, пока в системе не установится равновесие, то есть не прекратятся все неравновесные процессы. В состоянии равновесия энтропия изолированной системы имеет максимальное значение.
Третий закон термодинамики называют ещё тепловой теоремой Нернста. Эту теорему сформулировал в 1906 году немецкий физик Нерст на базе широких экспериментальных исследований поведения вещества при низкой температуре.
Благодаря этой теореме энтропия s, а также другие, связанные с ней функцией состояния становятся численно определёнными и практически полезными.
Дело в том, что энтропия определяется через её дифференциал ds. Поэтому сама величина s определена лишь с точностью до постоянной интегрирования s о. Там, где в расчётах имеют дело с дифференциалом энтропии, эта постоянная s о не влияет на результат.
Однако, поскольку в некоторые термодинамические формулы входит произведение Т · s о. Из-за этой неопределённости практически пользоваться такими формулами было бы нельзя.
Таким образом. Встаёт вопрос об абсолютном значении энтропии.
Ответом природы на этот вопрос и является теорема Нернста. В редакции Планка эта теорема звучит так:
при абсолютном нуле температуры (0, К) энтропия любого вещества принимает значение s о, не зависящее от давления, агрегатного состояния и других характеристик вещества. Эту величину s о можно принять равной нулю, получив, таким образом, абсолютную нормировку энтропии любого вещества.
То есть энтропия любой системы при абсолютном нуле всегда может быть принята равной нулю:
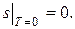 (13.1)
(13.1)
Это утверждение, подтверждаемое опытными данными, и называется третьим законом термодинамики.
Примечание:
Физический смысл энтропии можно прояснить как при анализе равновесных процессов, так и при изучении неравновесных процессов. При этом более глубокий термодинамический смысл энтропии раскрывается при анализе неравновесных процессов. (Отметим, что все реальные процессы являются в той или иной мере неравновесными). Смысл этот состоит в том, что изменение энтропии является мерой необратимости процессов в замкнутой системе и характеризует направление естественных процессов в такой системе.
14. Основные соотношения для расчёта процессов
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 468; Нарушение авторских прав?; Мы поможем в написании вашей работы!