
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные определения. Лекция 3. Квантово-химическая модель атома
|
|
|
|
Лекция 3. Квантово-химическая модель атома
1. Законы движения в квантовой механике принимают статистический характер.
2. Описание систем осуществляется с помощью волновой функции ψ (x, y, z, t), которая характеризует состояние системы.
3. 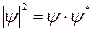 - это функция распределения вероятности (плотности вероятности).
- это функция распределения вероятности (плотности вероятности).
4. 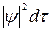 - это вероятность нахождения частицы в элементе пространства объемом dτ.
- это вероятность нахождения частицы в элементе пространства объемом dτ.
5. Основное уравнение квантовой химии - это уравнение Шредингера:
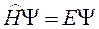 (1)
(1)
где 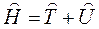 - оператор полной энергии системы (гамильтониан), сумма оператора кинетической энергии всех частиц системы
- оператор полной энергии системы (гамильтониан), сумма оператора кинетической энергии всех частиц системы 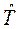 и оператора их потенциальной энергии
и оператора их потенциальной энергии 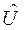 ; Е - полная энергия системы.
; Е - полная энергия системы.
Решение такого уравнения является сложной математической задачей, поэтому к основным подходам при исследовании проблемы многих тел можно относить различные приближенные методы (Хюккеля, Хартри-Фока, вариационный метод и т.д).
6. Решением уравнения (1) является набор собственных функцийψ1, ψ2,..., ψn и собственных значенийE1, E2,..., En (электронный спектр системы).
7. К волновым функциям предъявляются требования конечности, непрерывности и однозначности.
8. В некоторых случаях одному значению Eі могут соответствовать несколько состояний системы, описываются различными волновыми функциями ψі1, ψі2 или ψі1, ψі2, ψі3. Такие состояния называют вырожденными (дважды или трижды).
9. Собственные функции ψ1, ψ2,..., ψn уравнения Шредингера, принадлежащих различным собственным значением Е, ортогональны. То есть, области нахождения частицы в состояниях ψі и ψk взаимно не накладываются при i ≠ k.
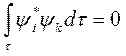 (2)
(2)
10. Вероятность найти частицу во всем пространстве определения функции равна:
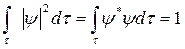 , (условие нормировки) (3)
, (условие нормировки) (3)
Функция, соответствующая условию нормировки (1), называется нормированной. Функции, отвечающие одновременно условиям (2) и (3), называются ортонормированными.
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 384; Нарушение авторских прав?; Мы поможем в написании вашей работы!