
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Стандартизация титрантов в перманганатометрии
|
|
|
|
Приготовить первичный стандартный раствор из KMnO4 нельзя, поскольку он не отвечает всем требованиям, перечисленным выше (в качестве примесей содержит MnO2, который способен катализировать реакцию окисления воды:
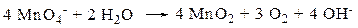 ,
,
что сопровождается изменением концентрации KMnO4 в растворе, кроме того, часть KMnO4 расходуется на реакции с примесями органических веществ, всегда присутствующих в воде. На устойчивость раствора KMnO4 влияет свет. Поэтому готовят раствор приблизительной концентрации, оставляют его на несколько дней (7-10) и стандартизируют первичным стандартом (Na2C2O4 и Н2С2O4∙2H2O)

Для создания среды используют разбавленную H2SO4. Применение HCl и HNO3 недопустимо, поскольку HCl проявляет ярко выраженные восстановительные свойства и может реагировать с KMnO4 с выделением Cl2, а HNO3 проявляет окислительные свойства и может взаимодействовать с определяемыми восстановителями.
Реакция KMnO4 с Н2С2O4 – автокаталитическая, т.е. вначале протекает медленно, поэтому раствор Н2С2O4 нагревают до ~ 70-80оС, а после появления в смеси катализатора Mn2+ реакция ускоряется.
Метод перманагантометрии широко применяют на практике для определения восстановителей и окислителей, а также веществ, не проявляющих окислительных или восстановительных свойств (например, для определения ионов Ca2+ в материалах как биологического, так и небиологического происхождения).
Для определения восстановителей используют прямое титрование:


Для определения окислителей (K2Cr2O7) используют обратное титрование. Суть его в том, что к раствору окислителя добавляют заведомо известный избыточный объем рабочего раствора восстановителя, например, FeSO4. Затем не прореагировавший остаток FeSO4 титруют KMnO4, т.е. в этом случае необходимы два рабочих раствора.
|
|
|



При определении индифферентных веществ, например, ионов Са2+, можно пользоваться только одним рабочим раствором KMnO4 (заместительное титрование) или двум титрантами (KMnO4 и Н2С2O4) – обратное титрование.
При использовании косвенного титрования анализируемый раствор, содержащий Са2+, обрабатывают растворимым оксалатом (Na2C2O4), т.о. чтобы полностью осадить Са2+ в виде твердого реактива CaC2O4. Осадок отфильтровывают и растворяют в кислоте H2SO4:
 ,
,
а затем

При использовании обратного титрования к анализируемому раствору добавляют избыток стандартного раствора Н2С2O4, осадок отбрасывают, а избыток Н2С2O4 титруют KMnO4.
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 2564; Нарушение авторских прав?; Мы поможем в написании вашей работы!