
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Дыхательная цепь, ее компоненты и организация
|
|
|
|
Краткая история открытия и изучения окислительного фосфорилирования.
Процесс окислительного фосфорилирования был открыт отечественными биохимиками Энгельгардом, Белицером и Цыбаковой. В период с 1937 по 1941 год эти ученые показали, что энергия, выделяющаяся в огромном количестве при полном окислении метаболитов в цитратном цикле, используется клеткой для синтеза АТФ. Исследования были затем продолжены в нескольких лабораториях как отечественных так и зарубежных. В результате к 1950 году выяснилось, что:
1. способность осуществлять окислительное фосфорилирование присуща исключительно митохондриям;
2. этот процесс является общим для всех аэробных организмов и представляет собой универсальный биохимический путь;
3. окисление (дыхание) и фосфорилирование могут быть разобщены с помощью определенных соединений, например: 2,4-динитрофенола (ввели в практику Лумис и Липман);
4. точки фосфорилирования связаны с цепью переноса электронов.
К настоящему времени общепринятой стала хемиоосмотическая теория окислительного фосфорилирования, сформулированная английским биохимиком Митчеллом.
Дыхательная цепь локализована на внутренней мембране митохондрии и включает в себя три трансмембранных белковых комплекса (комплексы I, III и IV), и два типа подвижных молекул-переносчиков электронов – убихинон (кофермент Q) и цитохром С. Между комплексом I и III расположен комплекс II – сукцинатдегидрогеназа, который катализирует окисление сукцината до фумарата в цикле Кребса. Рядом с комплексом IV расположен комплекс V, представляющий собой фермент АТФ-синтазу.
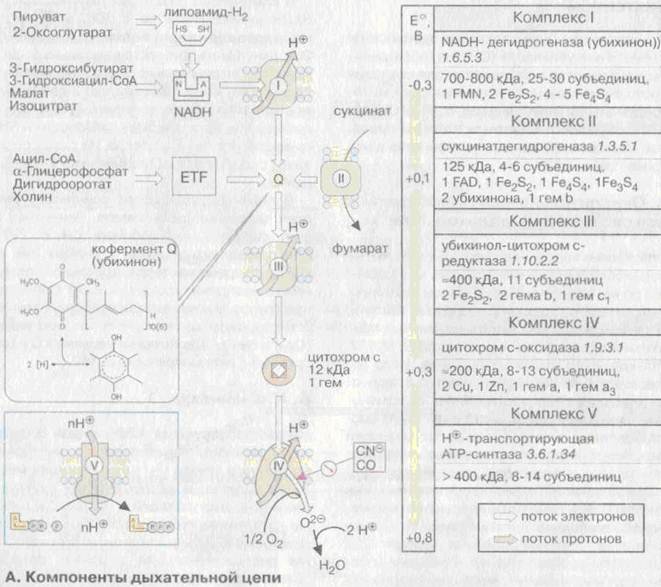
 Комплексы дыхательной цепи построены из множества полипептидов и содержат ряд различных окислительно-восстановительных коферментов, связанных с белками. Строение этих коферментов было нами рассмотрено на одной из предыдущих лекций и дано в пособии «Витамины и коферменты». Кроме того в состав комплексов входят железо-серные центры, а также ионы меди. Состав комлексов I –V и их взаимное расположение представлены на рис. А и Б.
Комплексы дыхательной цепи построены из множества полипептидов и содержат ряд различных окислительно-восстановительных коферментов, связанных с белками. Строение этих коферментов было нами рассмотрено на одной из предыдущих лекций и дано в пособии «Витамины и коферменты». Кроме того в состав комплексов входят железо-серные центры, а также ионы меди. Состав комлексов I –V и их взаимное расположение представлены на рис. А и Б.
Комплексы I, III и IV встроены во внутреннюю митохондриальную мембрану и представляют собой протонные каналы. Перенос протонов этими комплексами протекает векторно из матрикса в межмембранное пространство. При переносе электронов в дыхательной цепи повышается концентрация протонов в межмембранном пространстве. Комплекс II также встроен во внутреннюю митохондриальную мембрану, но переноса протонов через неё он не осуществляет. Этот комплекс осуществляет дегидрирование сукцината до фумарата в цитратном цикле с помощью простетической группы – ФАД и подвижного кофермента – убихинона. Комплекс V не относится к дыхательной цепи, его роль заключается в синтезе АТФ. Детальная структура комплексов еще не установлена.
Хотя, все комплексы с I по V интегрированы во внутренней мембране митохондрий, тем не менее они не контактируют друг с другом, а электроны переносятся между ними убихиноном и цитохромом с. Убихинон благодаря липофильной боковой цепи свободно перемещается в мембране между комплексами I и II, II и III (2 молекулы убихинона). Водорастворимый цитохром с находится на внешней стороне внутренней мембраны и перемешается между комплексом III и комплексом IV.
Окисление НАДН комплексом I происходит на внутренней стороне мембраны в матриксе, где осуществляется цитратный цикл и β-окисление жирных кислот – самые важные источники НАДН. В матриксе протекают также восстановление кислорода и образование АТФ.
Комплексы I, II и IV, составляющие дыхательную цепь являются протонными насосами.
Электроны поступают в дыхательную цепь следующими путями:
1 Путь. При окислении 1 молекулы НАДН комплекс I переносит 2 электрона через кофермент ФМН и Fe/S центры на подвижный переносчик электронов – убихинон, локализованный на мембране между комлексами I и II. При этом убихинон восстанавливается до убихинола. При этом одновременно через протонный канал комплекса I переносится 4 протона из матрикса в межмембранное пространство против градиента.
Далее эти 2 электрона от убихинола передаются на кофермент ФАД комплекса II, а с ФАД через Fe/S-центры на вторую молекулу убихинон, локализованный между комплексами II и III.
Затем электроны с второй молекулы убихинола поступают на активный центр комплекса III, который поставляет далее электроны через 2 гема b и Fe/S центр и гем с1 на небольшой гемсодержащий белок – цитохром С. При прохождении 2 электронов через комплекс III через его протонный канал в межмембранное пространство из матрикса также поступает 4 протона.
Цитохром С – водорастворимый белок, находящийся в растворе в межмембранном пространстве, восприняв электроны далее переносит их к комплексу IV. Комплекс IV - цитохром С: оксидаза (дыхательный фермент Варбурга) содержит два медьсодержащих центра и геммы (гем a, и гем a3), через которые электроны, наконец, поступают к кислороду.
При восстановлении кислорода образуется анион О-2, который связывает 2 протона и переходит в воду. При прохождении 2 электронов через комплекс IV, через его протонный канал поступает в межмембранное пространство 2 протона.
Таким образом при окислении 1 молекулы НАДН через дыхательную цепь передаются 2 электрона на кислород, т.е. образуется 1 молекула воды и в межмембранное пространство против градиента нагнетается 10 протонов (4Н+ + 4Н+ + 2Н+ = 10Н+).
2 Путь. Окислению подвергается сукцинат, образующийся в цикле Кребса. Его окисление начинается с передачи электронов на убихинон и далее по всей рассмотренной выше цепочке переносчиков на кислород.
Таким образом при окислении 1 молекулы сукцината через дыхательную цепь передаются 2 электрона на кислород, т.е. образуется 1 молекула воды и в межмембранное пространство против градиента нагнетается 6 протонов (4Н+ + 2Н+ = 10Н+), поскольку комплекс I в окислении сукцината не участвует.
Последовательность протекающих превращений в дыхательной цепи можно изобразить способом, предложенным Болдуином для написания уравнений последовательных циклических реакций:
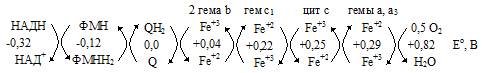
На этой схеме не показаны Fe/S центры и Cu+2/Cu+1 центры.
При переносе электронов возникает ЭДС равная разности потенциалов окислителя и восстановителя: ЭДС =ΔЕo = +0,82 – (-0,32) = 1,14 В.
Разность потенциалов позволяет найти изменение стандартной свободной энергии (ΔGo)
-ΔGo = - n·F·ΔЕo
При переносе пары электронов (n = 2) величина изменения стандартной свободной энергии равна:
-ΔGo = -2·96,5·1,14 = 220,0 кДж/моль
Перенос 2 электронов от НАДН к кислороду, т.е. образование 1 молекулы воды сопровождается переносом в межмембранное пространство из матрикса 10 Н+ вследствие чего возникает разность в рН. рН в межмембранном пространстве меньше чем в матриксе. Межмембранное пространство имеет более кислую реакцию по сравнению с матриксом.
Поток электронов сопряжен с переносом протонов из матрикса митохондрии в мжмембранное пространство комплексами I, III и IV, что создает протонный градиент.
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 4051; Нарушение авторских прав?; Мы поможем в написании вашей работы!