
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства. Физические и химические свойства фтора
|
|
|
|
Физические и химические свойства фтора
Фтор – светло-желтый газ с резким специфическим запахом. Фтор и его соединения ядовиты (за исключением CF4, SF6 и др.). Газообразный фтор растворим в жидком HF.
1. Фтор – сильный окислитель. Он энергично и бурно реагирует с большинством простых веществ (за исключением N2, He, Ne, Ar) с образованием фторидов.

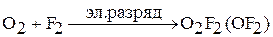

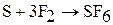

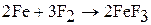
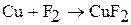
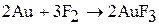
Фтор реагирует даже с благородными газами: криптон взаимодействует с фтором под действием электрического разряда. Ксенон горит в атмосфере фтора ярким пламенем с образованием фторидов.
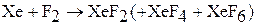
При взаимодействии с любым простым веществом чаще всего фтор окисляет его до максимальной степени окисления.
2. Фтор со взрывом взаимодействует с водородом даже при низких температурах:

2. Энергично фтор взаимодействует с водой:
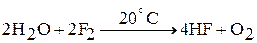
Кроме кислорода образуется также озон и дифторид кислорода OF2.
Прим. При растворении фтора в воде при температуре 0 ºС и ниже образуется фторноватистая кислота HOF – неустойчивая светло-желтая жидкость. При комнатной температуре фторноватистая кислота разлагается с образованием фтороводорода и кислорода.
3. Фтор вступает в реакцию с соединениями кремния (SiO2 – кварц):
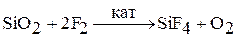
Катализатором данной реакции является вода, с совершенно сухим кварцем (или стеклом) фтор не взаимодействует.
Фтор хранят в посуде из никеля и его сплавов, меди, алюминия, нержавеющей стали, потому что на поверхности металла под действием фтора образуется защитная пленка соответствующих фторидов металлов.
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 2218; Нарушение авторских прав?; Мы поможем в написании вашей работы!