
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Кипение и замерзание растворов
|
|
|
|
(Второй закон Рауля)
Второй закон Рауля определяет изменение температуры кипения и замерзания растворов по сравнению с чистыми растворителями.
Данный растворитель закипает при той температуре, при которой давление его насыщенного пара достигает атмосферного
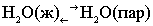 .
.
Раствор закипает при более высокой температуре, так как концентрация молекул растворителя в нём всегда ниже, чем в чистом растворителе, и давление насыщенного пара раствора достигает атмосферного при более высокой температуре.
Температура замерзания (кристализации) раствора ниже температуры замерзания чистого растворителя. Это обусловлено более низким давлением пара растворителя над раствором, чем над растворителем.
Второй закон Рауля определяет, чему равно изменение температуры кипения и замерзания растворов.
Изменение температуры кипения и замерзания растворов пропорционально моляльной концентрации растворов
Δt0кипения = Кэ См,
Δt0замерзания = Кк См.
Рассмотрим коэффициенты пропорциональности:
Кэ - эбуллиоскопическая константа,
Кк - криоскопическая константа.
Каждый растворитель имеет свои значения Кэ и Кк.
Эбулеоскопические и криоскопические константы некоторых растворителей приведены в табл.1.
Таблица 1
| Растворитель | Кэ | Кк |
| H2O | 0,53 0c | 1,86 0c |
| C6H6 | 2,57 0c | 5,02 0c |
Вывод: изменение температуры кипения и замерзания растворов зависит от природы растворителя концентрации раствора.
Физический смысл этих констант заключается в том, что при концентрации раствора, равной 1 моль/кг, данные константы равны изменению температуры кипения или замерзания данного раствора.
В отличие от чистых растворителей, которые кипят и замерзают при постоянной температуре, растворы кипят и замерзают в некотором интервале температур.
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 642; Нарушение авторских прав?; Мы поможем в написании вашей работы!