
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
H фосфора ( V ) Cl
|
|
|
|
H OH
О CN
Частица присоединения
Офильная продукт
1. Взаимодействие с цианидом натрия:

 // │ + H2O
// │ + H2O
Н3С—С + Na— C≡N ————→[ CH3—C―O―Na ]———→H3C—CH—C≡N
\ цианид │ – NaOH │
Н натрия H OH
ацетальдегид 2-цианоэтоксид натрия 2- гидрокси-
пропанонитрил
2. Взаимодействие с водой:
О ОН
// │

 СН3—С + НОН СН3—С—ОН
СН3—С + НОН СН3—С—ОН
\ │
Н Н
ацетальдегид гидрат ацетальдегида
3. Взаимодействие со спиртами:
Ацетали – соединения, содержащие при одном атоме углерода две алкоксильные группы (—OR):
OR1
/
R—C——OR2
\
H ацеталь
Полуацетали – соединения, содержащие при одном атоме углерода гидроксильную и алкоксильную группу:
OR1
/
R—C——OH
\
H
O O—R1
// /
R—C + R1—OH————→R—C——OH
\ \
H H
полуацеталь
O OR1
// /
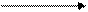
 R—C + 2R1—OH R—C——OR1 + H2O
R—C + 2R1—OH R—C——OR1 + H2O
\ \
H H
ацеталь
II. Окисление (качественные реакции на альдегидную группу):
1. Реакция серебряного зеркала:
AgNO3 + 3NH4OH ———→ [ Ag (NH3)2 ]OH + 2H2O + NH4NO3
O O
// t //
R—C + 2[ Ag (NH3 )2 ]OH ——→ R—C + 2Ag↓ + 4NH3↑ + H2O
\ \
H OH
альдегид кислота
2. Окисление гидроксидом меди (II):
 CuSO4 + 2KOH Cu (OH)2 ↓ + K2SO4
CuSO4 + 2KOH Cu (OH)2 ↓ + K2SO4
голубой
O O
// t //
R—C + 2Cu (OH)2 ↓ ———→ R—C + 2CuOH↓ + H2O
 \ \ желт. цв.
\ \ желт. цв.
Сu2O↓ H2O
кирпично-
красного
цвета
III. Галогенирование:
О O
// //
СН3—С + 6J2 + 3KOH ———→ CJ3—C + 3KJ + 3H2O
\ \
Н H
ацетальдегид иодаль
IV. Альдольная конденсация:
|
 О Н О ОН О
О Н О ОН О

 // │ // │ ║
// │ // │ ║
СН3—С + С—С—Н ———→СН3—С—СН2—С—Н
\ │ │
Н Н Н
этаналь этаналь альдоль
V. Взаимодействие с пятихлористым фосфором и тионилхлоридом:
O Cl
// │
R—C + PCl5 —————→ R—C—H + POCl3
\ хлорид │
O Cl
// │
R—C + SOCl2 —————→ R—C—H + SO2↑
\ тионилхлорид │
|
|
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 422; Нарушение авторских прав?; Мы поможем в написании вашей работы!