
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теория мономолекулярной адсорбции Ленгмюра
|
|
|
|
Фундаментальным вкладом в учение об адсорбции явилась теории Ленгмюра. Эта теория учитывает ограниченность адсорбционного объема и поверхности адсорбента.
Суть ее можно изложить, приняв следующие допущения:
1) адсорбция локализована (молекулы не перемещаются по поверхности) на отдельных адсорбционных центрах, каждый из которых взаимодействует только с 1 молекулой адсорбата – образуется мономолекулярный слой;
2) адсорбционные центры энергетически эквивалентны – поверхность эквипотенциальна;
3) адсорбированные молекулы не взаимодействуют друг с другом.
Предположим, что при адсорбции происходит квазихимическая реакция между компонентом и адсорбционным центром поверхности:

 - образующийся комплекс на поверхности.
- образующийся комплекс на поверхности.
При увеличении концентрации В реакция сдвигается вправо, адсорбционных центров становиться меньше. Тогда без учета коэффициентов активности константа равновесия адсорбции равна
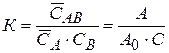
В этом соотношении  ,
,
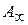 - емкость адсорбционного слоя, число адсорбционных центров на единицу поверхности или массы адсорбента,
- емкость адсорбционного слоя, число адсорбционных центров на единицу поверхности или массы адсорбента,
 - число оставшихся адсорбционных центров на единицу поверхности или массы адсорбента,
- число оставшихся адсорбционных центров на единицу поверхности или массы адсорбента,
А - величина адсорбции.
Исходя из этого, получим уравнение изотермы адсорбции:
 (4.18)
(4.18)
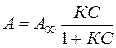 (4.19)
(4.19)
Так как для газов С пропорциональна их парциальным давлениям, то для них изотерма адсорбции принимает вид:
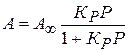 (4.20)
(4.20)
На рисунке приведена типичная изотерма адсорбции Ленгмюра:
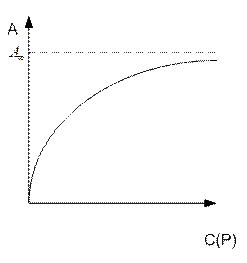
Уравнение Ленгмюра в координатах линейной формы:

Анализ уравнения:
1. При малых концентрациях или давлениях когда 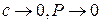
 (4.21)
(4.21)
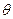 - степень заполнения поверхности,
- степень заполнения поверхности, 
 (4.22)
(4.22)
Уравнение Ленгмюра в этом случае соответствует закону Генри – величина адсорбции линейно растет с увеличением концентрации (давления).
2. При больших С и Р, когда КС >> 1 и К Р >> 1 получим соотношение:

- насыщение мономолекулярного слоя.
Зная величину 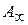 можно рассчитать удельную поверхность адсорбента:
можно рассчитать удельную поверхность адсорбента:
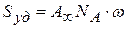 (4.23)
(4.23)
где 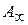 - предельная адсорбция в моль/кг (на единицу массы адсорбента),
- предельная адсорбция в моль/кг (на единицу массы адсорбента),
 - число Авогадро,
- число Авогадро,
 - площадь, занимаемая 1 молекулой.
- площадь, занимаемая 1 молекулой.
Экспериментальные результаты по определению изотермы адсорбции обычно обрабатывают с помощью изотермы Ленгмюра, записанного в линейной форме:
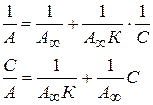
Из графика 
Отсекаемый отрезок прямой на оси ординат равен  . Таким образом графически из изотермы адсорбции можно найти оба постоянных параметра адсорбции -
. Таким образом графически из изотермы адсорбции можно найти оба постоянных параметра адсорбции - 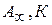 .
.
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 1066; Нарушение авторских прав?; Мы поможем в написании вашей работы!