
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ефект Джоуля-Томсона
|
|
|
|
Ефект Джоуля-Томсона для газу Ван-дер-Ваальса.
Ефект Джоуля-Томсона.
Ефект Джоуля-Томсона
2. Термодинамічна теорія ефекту Джоуля-Томсона.
4. Зрідження газів. Наднизьки температури.
Література: [1] стор. 253-261, [2] стор. 370-383, [7] стор.69-73,143-146, 401-413
· В чому суть і які причини ефекту Джоуля-Томсона?
· Охарактеризуйте критичну температуру.
· Назвіть методи зрідження газів.
ü Доведіть з допомогою якісних міркувань, що існують області тисків для даного газу, при яких інтегральний ефект Джоуля-Томсона може бути тільки або додатнім, або від’ємним, і існує область тисків, при яких ефект може бути як додатнім, так і від’ємним в залежності від кінченого тиску.
Досліди Гей-Люсака та Джоуля (див. Лекція 7), які дали можливість визначити залежність внутрішньої енергії ідеального газу від температури та об’єму, мали невисоку точність, оскільки теплоємність повітря була малою в порівняні із теплоємністю балонів і води в калориметрі. Через це малі зміни температури складно виявити. На протязі 1852-1862 рр. Джоуль і Томсон виконали ряд дослідів, які, з одного боку, дозволили остаточно встановити залежність внутрішньої газу від об’єму; з іншого, з їх допомогою було відкрито нове явище, яке отримало назву ефекту Джоуля-Томсона.
 В дослідах Джоуля-Томсона бралась циліндрична трубка, покрита теплоізолюючим матеріалом. В середині трубки між двома металевими сітками
В дослідах Джоуля-Томсона бралась циліндрична трубка, покрита теплоізолюючим матеріалом. В середині трубки між двома металевими сітками 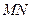 і
і 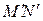 розміщувалось пробка із плотної вати або шовкові очоси. Досліджуваний газ під дією різниці тисків повільно протікав крізь пробку. Через наявність пробки протікання газу було спокійним, тобто без турбулентних рухів. Крім того, пробка забезпечувала повільність протікання, так що кінетичною енергією руху центру мас газу можна було знехтувати. За цих умов в кожний момент часу газ по обидві сторони пробки знаходився в стані термодинамічної рівноваги. Наявність теплоізолюючої оболонки забезпечувало адіабатність процесу протікання газу. Тиски газу
розміщувалось пробка із плотної вати або шовкові очоси. Досліджуваний газ під дією різниці тисків повільно протікав крізь пробку. Через наявність пробки протікання газу було спокійним, тобто без турбулентних рухів. Крім того, пробка забезпечувала повільність протікання, так що кінетичною енергією руху центру мас газу можна було знехтувати. За цих умов в кожний момент часу газ по обидві сторони пробки знаходився в стані термодинамічної рівноваги. Наявність теплоізолюючої оболонки забезпечувало адіабатність процесу протікання газу. Тиски газу 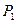 та
та 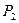 підтримувались постійними. Пробка і газ під час процесу обмінювались між собою теплом. Але коли процес ставав стаціонарним, теплообмін закінчувався, а отже її внутрішня енергія залишалась незміною При стаціонарному протіканні з одного боку від пробки встановлювалось незміною. При стаціонарному протіканні з одного боку від пробки встановлювалось постійна температура газу
підтримувались постійними. Пробка і газ під час процесу обмінювались між собою теплом. Але коли процес ставав стаціонарним, теплообмін закінчувався, а отже її внутрішня енергія залишалась незміною При стаціонарному протіканні з одного боку від пробки встановлювалось незміною. При стаціонарному протіканні з одного боку від пробки встановлювалось постійна температура газу 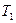 , а по інший – постійна температура
, а по інший – постійна температура 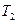 . Ці температури і вимірювались в досліді.
. Ці температури і вимірювались в досліді.
Стаціонарне протікання газу крізь пробку називається процесам Джоуля-Томсона, а зміна температури газу при такому протіканні – єфектом Джоуля-Томсона.
Відділимо подумки зліва від пробки об’єм 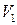 , що займає простір
, що займає простір 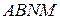 . Після проходження крізь пробку виділена порція газу займе простір
. Після проходження крізь пробку виділена порція газу займе простір 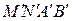 з об’ємом
з об’ємом 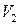 . Границя
. Границя 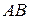 переходить в
переходить в 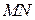 . При цьому над газом виконується робота
. При цьому над газом виконується робота 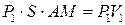 (S – площа поперечного перетину трубки). Границя
(S – площа поперечного перетину трубки). Границя 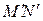 переходить в положення
переходить в положення 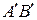 , і газ виконує роботу
, і газ виконує роботу 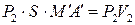 . Повна робота, виконана газом, дорівнює
. Повна робота, виконана газом, дорівнює 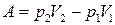 . Тепло до системи не надходить. Фізичний стан пробки і її внутрішня енергія залишились незмінними. Перший закон термодинаміки можна записати
. Тепло до системи не надходить. Фізичний стан пробки і її внутрішня енергія залишились незмінними. Перший закон термодинаміки можна записати
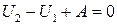
або
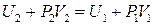 .
.
 За означеннями ентальпія
За означеннями ентальпія 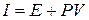 . Тому останній вираз означає, що в процесі Джоуля-Томсона ентальпія
. Тому останній вираз означає, що в процесі Джоуля-Томсона ентальпія 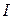 газу не змінюється
газу не змінюється
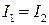 . (1)
. (1)
2. Термодинамічна теорія ефекту Джоуля-Томсона. Диференціальний і інтегральний ефекти
Нехай з різних боків в пробки підтримується мала різниця тисків 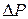 . В досліді вимірюється відповідна до неї різниця температур
. В досліді вимірюється відповідна до неї різниця температур 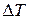 . Задача: маючи
. Задача: маючи 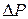 і рівняння стану газу, розрахувати
і рівняння стану газу, розрахувати 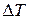 . Візьмемо в якості незалежних змінних
. Візьмемо в якості незалежних змінних 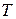 і
і 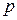 , тоді, враховуючи (1), можемо записати
, тоді, враховуючи (1), можемо записати
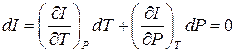 .
.
 Раніше було показано, що
Раніше було показано, що 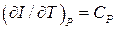 ; використаємо також співвідношення
; використаємо також співвідношення 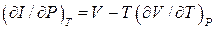 (отримати самостійно), звідки
(отримати самостійно), звідки
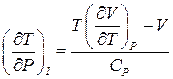 . (2)
. (2)
Якщо газ ідеальний, то 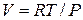 ,
, 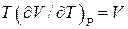 , а тому
, а тому 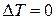 . Для ідеальних газів ефект Джоуля-Томсона відсутній. Для реальних газів відбувається або нагрів, або охолодження.
. Для ідеальних газів ефект Джоуля-Томсона відсутній. Для реальних газів відбувається або нагрів, або охолодження.
Збільшення або зменшення температури реального газу при його стаціонарному протіканні крізь пробку має назву диференціального ефекту Джоуля-Томсона. Формула (2) описує цей ефект.
Цією назвою підкреслюють, що величини 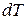 і
і 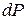 є малими величинами, так що їх відношення можна замінити похідною
є малими величинами, так що їх відношення можна замінити похідною 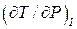 .
.
Інтегральний ефект.
Виділяють і інтегральний ефект Джоуля-Томсона. В цьому випадку різниця тисків достатньо велика – десятки, а інколи і сотні атмосфер, зміна температури також суттєва. Завдяки цьому інтегральний ефект використовується в техніці для отримання низьких температур.
Інтегральний ефект реалізується шляхом дроселювання газу – протіканням газу крізь малий отвір, з різних боків якого підтримується значна різниця тисків. В цьому випадку ентальпія також зберігається. Дроселювання не є рівноважним процесом. Однак початковий та кінцевий стани є рівноважними. Вони повністю визначаються значеннями ентальпії та тиску. При розрахунку зміни температури реальний процес можна змінити квазістатичним, що відбувається при постійній ентальпії. Вважаємо, що інтегральний ефект Джоуля-Томсона складається із неперервної послідовності диференціальних ефектів:
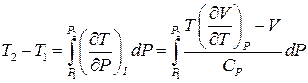 . (3)
. (3)
Така зміна реального процесу квазістатичним підходить лише для розрахунку параметрів газу в кінцевому стані. Результат виходить вірним не тому, що обидва процеси тотожні, а через те, що вони приводять до одного і того ж кінцевого стану.
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 2031; Нарушение авторских прав?; Мы поможем в написании вашей работы!