
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Квантовый выход первичной фотохимической реакции
|
|
|
|
Кроме общего квантового выхода  различают еще дифференциальные квантовые выходы:
различают еще дифференциальные квантовые выходы:
1. Первичный квантовый выход g1 равен отношению числа прореагировавших возбужденных молекул в первичном акте к числу поглощенных квантов.
2. Вторичный квантовый выход g2 является мерой развития вторичных реакций и равен отношению числа образовавшихся в процессе молекул продукта к числу молекул, прореагировавших в первичном акте. По определению, g = g1 g2.
Экспериментальная величина квантового выхода является важной характеристикой. Она позволяет судить о том, является ли данная частица результатом первичной физико-химической реакции, или она образуется в результате протекания сложного многостадийного процесса. Если  > 1, то реакция заведомо является сложной. Если
> 1, то реакция заведомо является сложной. Если  < 1, то можно сказать, что существенен вклад дезактивации за счет излучения и за счет внутримолекулярных переходов и эффект среды.
< 1, то можно сказать, что существенен вклад дезактивации за счет излучения и за счет внутримолекулярных переходов и эффект среды.
В практических исследованиях для изучения кинетики ФХР используют упрощенные схемы, к числу которых относится механизм Штерна-Фольмера.
Этот механизм рассматривает только три первичных процесса, протекающих после реакции фотохимической активации молекулы. Запишем схемы реакций и кинетические уравнения
Поглощение кванта света 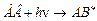
 -константа скорости образования возбужденных частиц -константа скорости образования возбужденных частиц 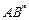
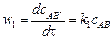 (14) (14)
|
Дезактивация за счет излучения 
 - константа скорости дезактивации возбужденных молекул за счет обратного испускания квантов света - константа скорости дезактивации возбужденных молекул за счет обратного испускания квантов света
 (15) (15)
|
Дезактивация за счет внутримолекулярных переходов 
 -константа скорости дезактивации возбужденных молекул за счет превращения поглощенной энергии в ее тепловые формы -константа скорости дезактивации возбужденных молекул за счет превращения поглощенной энергии в ее тепловые формы
 (16) (16)
|
Химическая реакция 
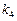 - константа скорости химической реакции - константа скорости химической реакции
 (17) (17)
|
Применим метод стационарных концентраций для нахождения концентрации неустойчивой промежуточной частицы АВ *.
 (18)
(18)
Откуда получаем
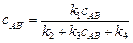 (19) Þ (17)
(19) Þ (17)
Отсюда скорость химической реакции  (20)
(20)
Выразим первичный квантовый выход  в следующем виде:
в следующем виде:
 (21)
(21)
Из этого уравнения следует, что квантовый выход первичной фотохимической реакции всегда меньше единицы.
Пример фотохимической реакции – поглощение диоксида углерода и воды растениями (фотосинтез).
Реакция соответствует уравнению 
Квантовый выход этой реакции равен 0,1 в расчете на одну молекулу диоксида. Реакция протекает за счет солнечной энергии, которая поглощается зеленым пигментом хлорофиллом, содержащимся в растениях. Фотосинтез – основа жизни на Земле, так как пополняет запасы кислорода и синтезирует органические вещества в клетках.
Другой важнейший пример – это реакция 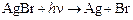 , лежащая в основе фотографического процесса.
, лежащая в основе фотографического процесса.
Рассмотрим экспериментальное определение квантового выхода реакции. Для этого введем такое понятие, которое называется тушением, это отношение числа поглощенных квантов света к числу испускаемых при дезактивации, т.е.  .
.
Величину тушения найдем как
 (22)
(22)
Если изобразить графически экспериментальные данные по тушению в координатах 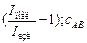 то по угловому коэффициенту и отрезкам на оси ординат можно найти все константы скоростей отдельных стадий, а затем и квантовый выход реакции.
то по угловому коэффициенту и отрезкам на оси ординат можно найти все константы скоростей отдельных стадий, а затем и квантовый выход реакции.
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 1820; Нарушение авторских прав?; Мы поможем в написании вашей работы!