
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Диаграммы фазовых равновесий с перитектическим превращением
Лекция № 8
Физическое материаловедение
Тема: Т – Х - ДИАГРАММЫ ФАЗОВЫХ РАВНОВЕСИЙ ДВОЙНЫХ СИСТЕМ С ОГРАНИЧЕННОЙ РАСТВОРИМОСТЬЮ КОМПОНЕНТОВ
Одной из особенностей рассмотренных выше диаграмм с эвтектикой является то, что компоненты системы А и В, растворяясь друг в друге, понижают температуру плавления раствора как со стороны А, так и со стороны В.
Если же при ограниченной растворимости компонентов друг в друге один из них, например В, растворяясь в А, понижает температуру плавления растворов на его основе, а компонент А, растворяясь в В, наоборот, повышает Т пл раствора, то вместо эвтектического превращения на диаграмме присутствует так называемое перитектическое превращение (n – точка перитектики, рис. 8.1 а).
Эвтектическое превращение в двойной системе заключается в распаде раствора при охлаждении на две другие фазы; перитектическое превращение, наоборот, представляет собой процесс образования одной фазы за счет взаимодействия двух других фаз, полностью или частично исчезающих при этом. Эта реакция записывается так:
| Ж + Тв 1 ↔ Тв 2 или Ж + α ↔ β (охлаждение ↔ нагрев) | (8.1) |
Перитектическое превращение в двойной системе является нонвариантным. Составы трех равновесных фаз, как и на линии эвтектики, определяются точками пересечения горизонтальной линии перитектики ab с наклонными линиями на фазовой диаграмме (т. е. точками a, n, b).
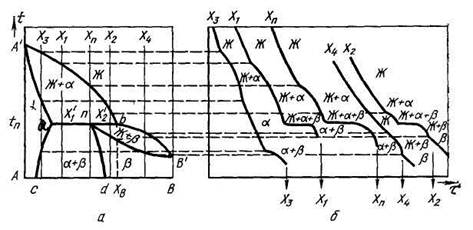
| Рис. 8.1. Фазовая диаграмма с перитектическим превращением (а) и кривые охлаждения (б) сплавов, указанных на диаграмме. |
На рис. 8.1 б приведены кривые охлаждения для пяти сплавов Х n, Х 1, Х 2, Х 3, X 4, составы которых показаны на рис. 8.1 а. На кривых охлаждения указан фазовый состав сплавов в различных температурных интервалах.
Задача 8.1. Определить вариантность системы при температуре Т n, рис. 8.1 а.
Протяженность площадки на кривых охлаждения при Т n для сплавов Х n, Х 1, Х 2 пропорциональна количеству1 взаимодействующих жидкого раствора и твердой фазы (по количеству фазы, образовавшейся по перитектической редакции при Т n). Для сплава Х n эти относительные количества принимаются за 100%, для остальных сплавов по протяженности площадки с помощью правила рычага можно определить долю сплава, претерпевающую перитектическое превращение.
Для сплавов, составы которых лежат в интервале от Х а до Х n, количество жидкой фазы при температуре Т n недостаточно, чтобы произошло взаимодействие со всей твердой фазой. В итоге после перитектического превращения, кроме новой фазы, сплавы будут содержать и избыточное количество первичных кристаллов фазы α. Для сплава X 1 при температуре чуть ниже Т n количество избыточных кристаллов в сплаве будет равно (Х 1n/ аn)·100%.
Аналогично для сплавов, составы которых лежат в интервале от Х n до Х b, количество фазы α при Т n будет мало по сравнению с количеством жидкой фазы. В итоге по завершении перитектического превращения в сплавах сохранится избыточное количество жидкой фазы.
В сплаве Х 2 ее относительное количество составит (nX 2/ nb ж)·100%.
Важной особенностью системы с перитектикой является то, что при температуре Т n кристаллизация завершается только у части сплавов, претерпевающих перитектическое превращение. Как видно из диаграммы на рис. 8.1 для сплавов в интервале от Х n до X кристаллизация завершается ниже Т n на линии nВ '.
Линией ликвидуса (начало кристаллизации) является линия А ' bВ ', а линией солидуса - линия А ' аnВ '. Линия аС называется кривой растворимости. Линия аb - перитектической горизонталью, на ней лежат три фигуративные точки а, n и b, отвечающие составу фаз, претерпевающих нонвариантное превращение.
Если превращение, аналогичное перитектическому, происходит с участием только твердых фаз, то его называют перитектоидным.
| Тв 1 + Тв 2 ↔ Тв 3 или α + β ↔ γ (охлаждение ↔ нагрев) | (8.2) |
___________________
1 Количественное сопоставление размеров горизонтальных площадок на кривых охлаждения или нагрева возможно лишь для сплавов одинаковой массы.
|
Дата добавления: 2014-01-11; Просмотров: 1694; Нарушение авторских прав?; Мы поможем в написании вашей работы!