
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Структура активных центров катализаторов гидрообессеривания
|
|
|
|
Хотя АНМ и АКМ катализаторы в сульфидной форме (в дальнейшем Co(Ni)MoSX/Al2O3) применяются в промышленности примерно с середины прошлого века, исследования с целью определения химической структуры активных центров все еще продолжаются. Особенно плодотворными в этом отношении были семидесятые и восьмидесятые годы, когда было выдвинуто множество моделей активных центров этих катализаторов. В обзорной статье [4] приведено сравнение различных моделей активных центров и обсуждено их согласование с наблюдаемыми экспериментальными фактами. На рис. 1.6 изображены модели активных центров, обсуждаемые ниже.
Активностью в прямом удалении серы обладает дисульфид молибдена, имеющий слоистую кристаллическую структуру (рис. 1.6, а). Установлено, что «ободковые» центры (см. рис.) активны в гидрировании, а «краевые» - в реакции прямого удаления серы. Небольшие количества сульфида Co или Ni, добавляемые к MoS2, повышают его активность, хотя сами ее и не проявляют. Говорят, что Co или Ni являются промоторами.
Некоторые авторы предполагали, что промотор и MoS2 являются отдельными кристаллитами в близком контакте, при этом промотор активирует водород. Это модель контактного синергизма (рис. 1.6, б). Это предположение не нашло экспериментального подтверждения.
Предполагалось также, что промотор связан с носителем, и это приводит к повышенной стабильности нанесенного монослоя MoS2 (рис. 1.6, в). Впоследствии было показано, что нахождение промотора в носителе (фактически в виде алюмоникелевой или алюмокобальтовой шпинели) делает его неактивным в катализе.
Существуют еще модели интеркаляции, декорирования и сульфидно-биметаллических соединений. Они предполагают внедрение актомов промотора в кристаллическую решетку MoS2 – в оъеме или на границе слоев (рис. 1.6, г). В этих моделях принимается, что MoS2 существует на поверхности в виде объемных многослойных кристаллитов.
Сравнительно недавно установлено, что наиболее активным компонентом Co(Ni)MoSX/Al2O3 катализаторов являются небольшие кристаллиты MoS2, представляющие собой монослои или короткие слоистые упаковки (рис. 1.7). Наиболее активными каталитическими центрами являются атомы Co(Ni), связанные сульфидными мостиками с поверхностью этих образований. Это соединение было открыто группой исследователей под руководством H.Topsoe и получило название «фаза Co-Mo-S». Было установлено, что обнаруженное ранее оптимальное мольное соотношение Со/(Со+Мо) = 0,3 объясняется тем, что в этом случае все краевые позиции кристаллита MoS2 покрыты Co или Ni. Точная природа этих краевх центров не установлена.

Р и с. 1.6. Модели активных центров сульфидных алюмокобальтмолибденовых катализаторов
Найдено, что константа скорости реакции ГДС прямо пропорциональна содержанию ионов промотора в фазе Co-Mo-S. Остается не понятым следующий экспериментальный факт: как установлено Мессбауэровской эмиссионной спектроскопией, лишь около 10 % фазы Co-Mo-S представляет собой активные центры для удаления серы.
Исходя из совокупности имеющихся экспериментальных данных, можно считать, что 1) ионы Co(Ni) и Mo(W) находятся в непосредственной близости; 2) на поверхности сульфидной фазы есть анионные вакансии; 3) Ni2+ (Co2+) – компенсирующие ионы на ребрах кристаллитов MoS2.

Р и с. 1.7. Промотирование гидродесульфирующей активности в зависимости от содержания Со на катализаторе в виде Со-Мо-S
Процессы образования анионных вакансий протекают при активации катализатора (где - вакансия аниона):
Ni2+S2- + H2 ® H2S + Ni0
Ni0 + 2Mo4+ ® Ni2+ + 2Mo3+
Структура активного центра и механизм реакции обессеривания указан на схеме (рис. 1.8).
Лекция 10.
1.3. Способы введения активных компонентов в катализаторы гидроочистки и их модифицирование
Существует два способа введения активных компонентов в каталитическую систему: пропитка гранул носителя растворами соединений активных компонентов; совместная формовка носителя с соединениями активных компонентов. Применяется также их сочетание.
В табл. 1.1 приведено сравнение ГДС активности АКМ катализаторов, синтезированных в промышленных условиях различными методами.
Данные таблицы согласуются с наиболее принятой в последнее время моделью активной поверхности АКМ (АНМ) катализатора. Действительно, наименьшую активность проявляет катализатор 4, в котором не обеспечен контакт Мо и Со. Способ синтеза в данном случае способствует образованию алюмокобальтовой шпинели и исключению Со из активной фазы. Максимальный контакт Мо и Со, а также максимальную доступность активных компонентов для реагирующих веществ обеспечивает способ синтеза катализатора 1. При других способах синтеза часть активных компонентов связана в объеме носителя.
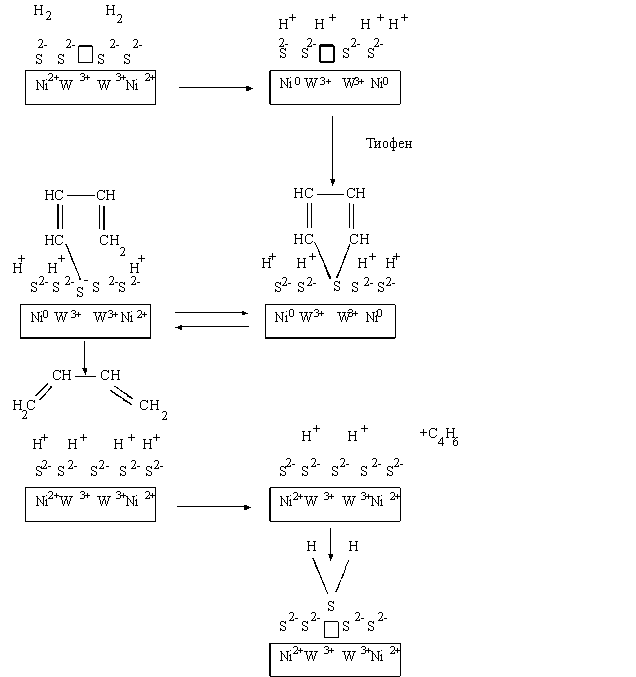
Р и с. 1.8. Предполагаемый механизм гидрообессеривания тиофена:
 - анионная вакансия; прямоугольник означает, что на включенных катионах могут находиться (частично) делокализованные катионы
- анионная вакансия; прямоугольник означает, что на включенных катионах могут находиться (частично) делокализованные катионы
Введение в АКМ и АНМ катализаторы гидроочистки различных веществ называется модифицированием и позволяет повысить их термическую стабильность, механическую прочность, каталитическую активность.
Механическая прочность и термическая стабильность повышается при введении оксидов кремния, титана, борной и фосфорной кислот. Фосфорная кислота, по патентным данным, может также увеличивать общую пористость и объем макропор.
Таблица 1.1
Гидродесульфирующая активность катализаторов СоМо/g-А12О3
| Способ синтеза катализатора | Степень ГДС |
| 1. Пропитка g-А12О3 совместным аммиачным раствором солей Со и Мо | |
| 2. Соэкструзия бемита с растворами солей Со и Мо | |
| 3.Соэкструзия бемита с солью Мо, термообработка, пропитка таствором соли Со | |
| 4. Соэкструзия бемита с раствором соли Со, термообработка, пропитка раствором соли Мо |
Добавки Ti, P, B, Si, V увеличивают активность катализаторов в реакции ГДС. При этом нужно подобрать оптимальное содержание модификатора, т.к. его избыток приводит к снижению каталитической активности. Например, Р2О5 не должно быть более 1 %. Т.е. зависимость активности от содержания добавки проходит через максимум. Большое значение имеет также способ синтеза модифицированного катализатора: последовательность операций, соединение, из которого вводится модификатор, температуры и продолжительность сушки и прокаливания, рН растворов и т.д.
1.4. Пористая структура, размер и форма частиц катализаторов гидроочистки
Пористость катализаторов гидроочистки является важным фактором их эффективности. Сопротивление массопереносу в порах катализатора значительно для всех видов сырья, от легких дистиллятов до остатков, но для тяжелых видов сырья оно особенно значительно. Влияние пористой структуры катализаторов гидроочистки на их активность неоднократно обсуждалось, но единого мнения относительно оптимальной структуры нет.
Для тяжелых видов сырья (дизельные фракции и более тяжелое сырье) однозначно установлено преимущество крупнопористых катализаторов. Крупнопористый катализатор медленнее закоксовывается вследствие дезактивирования. Мелкие поры блокируются коксом уже в первые часы работы. В широкопористом катализаторе кокс откладывается на стенках крупных пор, в меньшей степени препятствуя доступу сырья к активным центрам. Оптимальный эффективный радиус пор в этом случае составляет 8 – 10 нм.
В последние годы отечественные производители также стали выпускать катализаторы с меньшим диаметром гранул, что увеличивает площадь внешней поверхности и делает более доступной внутреннюю поверхность. В том случае, когда форма гранул катализатора отличается от цилиндрической (например, представляет собой трилистник в поперечном сечении), увеличивается отношение площади внешней поверхности к объему гранулы, и внутренняя поверхность гранулы также становится более доступной. Сложная форма гранул увеличивает долю свободного объема в слое катализатора, пористость слоя катализатора и уменьшает перепад давления в слое (рис. 1.9).
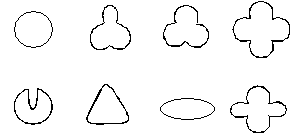
Р и с. 1.9. Различная форма гранул катализаторов
Изменение формы гранул и уменьшение диаметра преследует одну цель – уменьшить отношение объема гранулы к площади внешней поверхности. Зависимость активности катализатора от этой величины представлена на рис. 1.10.
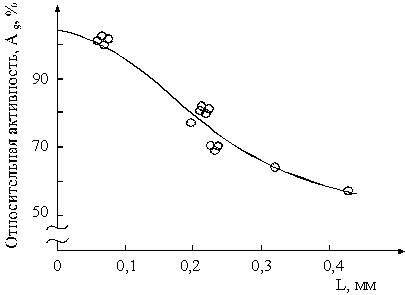
Р и с. 1.10. Зависимость относительной активности от отношения объема гранулы катализатора к ее наружной поверхности (L, мм) при переработке остаточного сырья
1.5. Сульфидирование катализаторов гидроочистки
Катализаторы гидроочистки производятся в оксидной форме: NiO–MoO3/Al2O3. Рабочим состоянием катализатора гидроочистки в условиях процесса является его сульфидная форма. Одна из основных стадий формирования активной фазы – сульфидирование катализатора. Она, как правило, проводится непосредственно в реакторе.
Установлено, что наивысшей активностью обладают дисульфид молибдена и смешанный сульфид никеля (NiS +Ni2S). При обработке катализатора гидроочистки в сульфидной форме водородом в присутствии сероводорода конкурируют две реакции:
сульфидирование
MoO3 + H2 + H2S ® MoS2 + 3H2O
3NiO + H2 + 2H2S ® Ni3S2 + 3H2O
и восстановление
MoO3 + H2 ® MoO2 + H2O
NiO и CoO могут восстанавливаться до металлов.
Реакции сульфидирования, как правило, протекают не полностью. Содержание серы в сульфидированном катализаторе, независимо от способа сульфидирования, практически никогда не отвечает составу MoS2- Ni3S2. По данным, начальная степень сульфидирования катализатора в зависимости от применяемых реагентов составляет 100% (H2S), 77 % (меркаптаны), 40 % (сернистое дизельное топливо). Содержание кокса на катализаторе после гидроочистки в течение 96 ч вакуумного газойля составило: 7 % (H2S), 8,2 % (меркаптаны), 9,7 % (сернистое дизельное топливо), 11,4 % (без сульфидирования). Содержание серы в гидрогенизате: 0,18 % (H2S), 0,21 % (меркаптаны), 0,29 % (сернистое дизельное топливо), 0,35 % (без сульфидирования).
На рис. 1.11 представлена зависимость изменения активности катализаторов от времени опыта для разных условий предварительной обработки катализатора.
Как видно из рисунка, максимальную активность проявляет сульфидированный катализатор, наихудшие результаты наблюдаются в случае предварительного восстановления. При этом более «жесткое» предварительное восстановление приводит к меньшей стационарной активности катализатора. Это объясняется тем, что восстановление водородом, особенно при высоких температурах, приводит к образованию из МоО3 восстановленной формы – МоО2, который очень трудно перевести в сульфид.
Практически более важными являются способы сульфидирования, когда катализатор обрабатывают смесью, содержащей, кроме водорода и H2S, еще и какой-либо углеводород. Результаты сравнительного исследования таких способов сульфидирования представлены в табл.1.2.
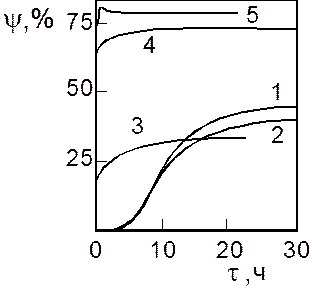
| Данные, приведенные в таблице, свидетельствуют о том, что присутствие в реакционной смеси углеводородов на стадии сульфидирования отрицатель-но сказывается на каталитической активности. Максимальную активность проявляет образец катализа-тора, сульфидированный смесью H2 + H2S (образец 1). Присутствие в сульфиди-рующей смеси додекана (образец 2) резко снижает каталитическую активность, очевидно, из-за того, что одновременно с переводом активных компонентов в сульфидную форму на активной поверхности происходило отложение кокса. |
| Рис. 1.11. Изменение степени превращения бензотиофена ψ при 250 0С от длительности испытания τ при различных условиях: 1 – без обработки; 2 – восста-новление 10 ч при 250 0С; 3 - восстановление 1 ч при 400 0С; 4 – то же, затем сульфидирование при 250 0С; 5 - сульфидирование при 250 0С. |
Сравнение активности образцов 1 и 3 показывает, что контакт катализатора в оксидной форме, до сульфидирования, с углеводородом еще более резко снижает активность. Это происходит, несмотря на то, что для обработки применялся углеводород с низкой молекулярной массой – этан, коксогенность которого значительно ниже, чем додекана, применявшегося при обработке образца 2. По-видимому, основную роль в снижении каталитической активности образца 3 играет не только закоксовывание активной поверхности, но и восстановление активных металлов, затрудняющее их перевод в сульфидную форму.
При обработке образцов 2 и 4 применялись одни и те же реагенты, но в разной последовательности. Сравнение активности, полученной на этих образцах, свидетельствует о том, что и после сульфидирования в реакционной смеси должно присутствовать определенное количество H2S. Это отмечается и в других литературных источниках: постоянное поддержание определенного минимума парциального давления сероводорода сохраняет катализатор длительное время активным. Это имеет место в условиях гидроочистки, но в случае образца 4 его активная поверхность контактировала с углеводородом в отсутствие H2S, и это предположительно привело к закоксовыванию образца и резкому снижению его активности.
Таблица 1.2
|
|
|
|
|
Дата добавления: 2014-01-14; Просмотров: 2350; Нарушение авторских прав?; Мы поможем в написании вашей работы!