
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Коррозия и защита металлов
|
|
|
|
Пример 1. Возможна ли коррозия сплава, состоящего из мелкодисперсных кристаллов висмута и свинца: а) в аэрируемой воде; б) в изолированном от воздуха сосуде с водой? Для среды, в которой коррозия возможна, составьте схему микрогальванических элементов, возникающих в процессе коррозии. Составьте уравнения анодного и катодного процессов и результирующее (суммарное) уравнение процесса коррозии.
Решение. Как любой окислительно-восстановительный процесс, коррозия возможна, если потенциал окислителя больше потенциала восстановителя (Eокисл > Eвосст). Отсюда следует, что в первую очередь будет окисляться, т.е. корродировать, металл, имеющий меньший электродный потенциал. Таким металлом в данном примере является свинец (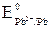 = –0,13 В <
= –0,13 В < 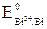 = +0,22 В). Окислителем будут те ионы или молекулы в окружающей среде, которые имеют больший потенциал.
= +0,22 В). Окислителем будут те ионы или молекулы в окружающей среде, которые имеют больший потенциал.
а) В аэрируемой воде из двух возможных окислителей – иона водорода воды H+ и растворенного в воде кислорода O2 – более сильным окислителем является кислород, так как его потенциал больше (в нейтральной среде 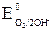 = +0,81 В >
= +0,81 В > 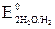 = –0,41 В). Коррозия возможна, так как Eокисл = +0,81 В > Eвосст = –0,13 В.
= –0,41 В). Коррозия возможна, так как Eокисл = +0,81 В > Eвосст = –0,13 В.
Схема гальванического элемента: Pb | O2; H2O | Bi. Анодом является свинец, катодом – висмут. Протекают процессы:
Анод Pb – 2 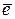 = Pb2+ │ 2
= Pb2+ │ 2
Катод O2 + 4 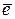 + 2H2O = 4OH– │ 1
+ 2H2O = 4OH– │ 1
2Pb + O2 + 2H2O = 2Pb(OH)2 ↓
Продуктом коррозии является труднорастворимый гидроксид свинца Pb(OH)2.
б) В отсутствие кислорода единственным окислителем могли бы быть ионы водорода из воды. Но поскольку Eокисл = –0,41 В < Eвосст = –0,13 В, коррозия невозможна.
Пример 2. Какие процессы будут протекать при коррозии бериллия и меди, находящихся в контакте? Составьте уравнения анодного и катодного процессов и результирующее (суммарное) уравнение процесса коррозии в следующих средах: а) во влажном воздухе; б) в растворе гидроксида натрия; в) в растворе хлороводородной кислоты.
Решение. Из контактирующих металлов более активным восстановителем является бериллий, так как 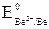 = –1,85 В <
= –1,85 В < 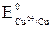 = +0,34 В, поэтому, в первую очередь, корродирует бериллий.
= +0,34 В, поэтому, в первую очередь, корродирует бериллий.
а) Во влажном воздухе окислителем является кислород. Коррозия возможна, так как его потенциал значительно больше потенциала бериллия. Бериллий будет являться анодом и окисляться, а медь – катодом, где будет восстанавливаться кислород:
Анод Be – 2 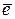 = Be2+ │ 2
= Be2+ │ 2
Катод O2 + 4 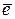 + 2H2O = 4OH– │ 1
+ 2H2O = 4OH– │ 1
2Be + O2 + 2H2O = 2Be(OH)2 ↓
Продуктом коррозии является труднорастворимый гидроксид бериллия.
б) Поскольку гидроксид бериллия амфотерен, в щелочном растворе процесс анодного окисления бериллия заканчивается образованием гидроксокомплекса:
Анод Be – 2 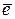 + 4OH– = [Be(OH)4]2–
+ 4OH– = [Be(OH)4]2–
Несмотря на то, что потенциал кислорода больше, чем иона водорода воды, доступ кислорода к поверхности катода (медь) ограничен из-за малой его растворимости и медленной диффузии. Поэтому в щелочном растворе (pH 14) при условии 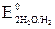 = –0,82 В >>
= –0,82 В >> 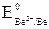 = –1,85 В, окислителем является ион водорода воды
= –1,85 В, окислителем является ион водорода воды
Катод 2H2O + 2 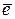 = H2 + 2OH–
= H2 + 2OH–
Результирующее уравнение процесса коррозии получим, суммируя уравнения анодного и катодного процессов:
Be + 2H2O + 2OH– = [Be(OH)4]2– + H2
или
Be + 2H2O + 2NaOH = Na2[Be(OH)4] + H2
в) По тем же кинетическим причинам, что и в предыдущем случае, окислителем является ион водорода H+. Уравнения процессов:
Анод Be – 2 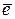 = Be2+
= Be2+
Катод H2 + 2 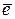 = H2
= H2
Be + 2H2 = Be2+ + H2
или
Be + 2HCl = BeCl2 + H2
Задания
181-192. Какие коррозионные процессы могут протекать при контакте двух металлов? Составьте уравнения анодного и катодного процессов и результирующее (суммарное) уравнение процесса коррозии в заданных условиях. Если коррозия невозможна, то объясните, почему?
| Номер задачи | Металлы | Среда |
| Cu, Fe | а) раствор HCl | |
| б) влажный воздух | ||
| Zn, Fe | а) речная вода | |
| б) раствор HCl | ||
| Cu, Ag | а) аэрируемый раствор H2SO4 | |
| б) закрытый сосуд с раствором HCl | ||
| Ni, Fe | а) влажный воздух | |
| б) раствор H2SO4 | ||
| Cr, Ni | а) морская вода | |
| б) раствор H2SO4 | ||
| Cu, Zn | а) влажный грунт | |
| б) раствор HCl | ||
| Cu, Sn | а) раствор H2SO4 | |
| б) влажный воздух | ||
| Sn, Fe | а) раствор H2SO4 | |
| б) морская вода | ||
| Al, Cu | а) раствор H2SO4 | |
| б) раствор NaOH | ||
| Sn, Ag | а) раствор HCl | |
| б) влажный воздух | ||
| Cu, Ni | а) раствор HCl | |
| б) вода при отсутствии в ней растворенного кислорода | ||
| Cu, Au | а) раствор H2SO4 в контакте с воздухом | |
| б) раствор H2SO4 при отсутствии в окружающей среде кислорода |
193. Приведите пример катодного покрытия для никеля. Напишите уравнения анодного, катодного и суммарного процессов коррозии, протекающих в аэрируемом водном растворе и в солянокислой среде при частичном нарушении такого покрытия.
194. Приведите пример анодного покрытия для кадмия. Напишите уравнения анодного, катодного и суммарного процессов коррозии, протекающих в сернокислом растворе и во влажном воздухе, при частичном нарушении такого покрытия.
195. Какие металлы можно использовать для протекторной защиты железа? Для одного из примеров напишите уравнения анодного, катодного и суммарного процессов коррозии в аэрируемом водном растворе и в сернокислой среде.
196. В чем сущность катодной защиты от коррозии? Какие процессы протекают на электродах при катодной защите стального трубопровода, проложенного во влажном грунте?
197. К какому типу покрытий относится лужение (покрытие оловом) меди? Напишите уравнения анодного, катодного и суммарного процессов коррозии, протекающих во влажном воздухе и в сернокислой среде при частичном нарушении этого покрытия.
198-200. Возможна ли в средах (а) и (б) коррозия сплава, представляющего собой смесь мелкодисперсных кристаллов металлов X и Y?
В случае возможности коррозии составьте схему микрогальванических элементов, возникающих в процессе коррозии. Напишите уравнения анодного и катодного процессов и суммарное уравнение процесса коррозии. Если коррозия невозможна, то объясните, почему?
| Номер задачи | X | Y | Среда | |
| Ag | Cu | а) аэрируемый раствор HCl | б) изолированный от воздуха раствор HCl | |
| Cd | Bi | а) раствор H2SO4 | б) влажный воздух | |
| Pb | Sb | а) влажный воздух | б) вода при отсутствии растворенного в ней кислорода |
Варианты контрольных заданий
| Номер варианта | Номера задач | |||||||||
| Контрольная работа №1 | Контрольная работа №2 | Контрольная работа №3 | ||||||||
Приложения
|
|
|
|
|
Дата добавления: 2014-11-07; Просмотров: 2116; Нарушение авторских прав?; Мы поможем в написании вашей работы!