
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Примеры решения задач. В зависимости от концентрации ионов водорода различают три среды
|
|
|
|
В зависимости от концентрации ионов водорода различают три среды.
В нейтральной среде [H+] = [OH-]= 10-7 моль/л, рН= – lg 10-7 = 7. Эта среда характерна как для чистой воды, так и для нейтральных растворов. В кислых растворах [H+] > 10-7моль/л, рН < 7. В кислых средах рН меняется в пределах 0 < рН < 7. В щелочных средах [H+] < [ОН–] и [H+] < 10-7 моль/л, следовательно, рН > 7. Пределы изменения рН: 7 < рН < 14.
Реакции ионного обмена (РИО) – это реакции между ионами, протекающие в водных растворах электролитов. Отличительная особенность обменных реакций: элементы, входящие в состав реагирующих веществ, не меняют свою степень окисления. Реакции ионного обмена являются необратимыми реакциями и протекают при условии: 1) образования малорастворимого вещества, 2) выделения газообразного вещества, 3) образования слабого электролита.
При протекании РИО противоположно заряженные ионы связываются и выводятся из сферы реакции. Сущность реакций ионного обмена выражают с помощью ионных уравнений, которые, в отличие от молекулярных, показывают истинных участников реакции. При составлении ионных уравнений следует руководствоваться тем, что вещества малодиссоциирующие, малорастворимые (выпадающие в осадок) и газообразные записываются в молекулярной форме. Сильные растворимые электролиты записываются в виде ионов. Поэтому при написании ионных уравнений необходимо пользоваться таблицей растворимости солей и оснований в воде.
Гидролиз – это процесс взаимодействия ионов соли с молекулами воды, приводящий к образованию малодиссоциирующих соединений; является частным случаем реакций ионного обмена. Гидролизу подвергаются соли, образованные:
1) слабой кислотой и сильным основанием (NaCH3COO, Na2CO3, Na2S,);
2) слабым основанием и сильной кислотой (NH4Cl, FeCl3,, AlCl3,);
3) слабым основанием и слабой кислотой (NH4CN, NH4CH3COO).
Соли, образованные сильной кислотой и сильным основанием, гидролизу не подвергаются: Na2SO4, BaCl2, NaCl, NaJ и т.д.
Гидролиз солей увеличивает концентрации ионов Н+ или ОН–. Это приводит к смещению ионного равновесия воды и в зависимости от природы соли сообщает раствору кислую или щелочную среду (см. примеры решения задач).
Пример 1. Вычислить константу диссоциации уксусной кислоты СН3СООН, зная, что в 0,1М растворе она диссоциирована на 1,32%.
Р е ш е н и е. Для решения задачи воспользуемся законом разбавления Оствальда – уравнение (13), в котором С – концентрация уксусной кислоты, a – степень ее диссоциации в данном растворе, значение которой равно 1,32/100=0,0132. Таким образом, 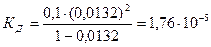
Ответ: константа диссоциации уксусной кислоты составляет 1,76×10-5.
Пример 2. Вычислить значение рН 0,1М раствора гидроксида аммония NH4OH, приняв степень диссоциации раствора равной 1%.
Р е ш е н и е. 1) Записываем уравнение диссоциации раствора NH4OH:
NH 4OH ⇄ NH4+ + OH–
2) Так как гидроксид аммония – слабый электролит и процесс его диссоциации носит обратимый характер, к моменту равновесия в 1 л раствора продиссоциировало С∙a моль NH4OH (С = 0,1 моль/л) и образовалось столько же моль ОН– – ионов:
[OH-] = С∙a = 0,1∙×0,01 = 1×10-3 моль/л, следовательно, рОН = 3
3) Рассчитываем значение рН: pH + pOH = 14, рН = 14 – 3 = 11.
Ответ: рН 0,1М раствора гидроксида аммония равно 11.
Пример 3. Выразить с помощью ионного уравнения сущность реакции:
Pb(NO3)2 + KI ®
Р е ш е н и е. 1) Составляем молекулярное уравнение реакции:
Pb(NO3)2 + 2KI ® PbI2¯ + 2KNO3
Отмечаем, что в результате образуется нерастворимое вещество PbI2.
2) Составляем полное ионное уравнение (все сильные электролиты записываем в виде ионов, слабые, уходящие из сферы реакции, – в виде молекул):
Pb2+ + 2NO3– + 2K+ + 2I– = PbI2¯ + 2K+ + 2NO3–
3) Составляем сокращенное ионное уравнение, в котором исключаем все ионы, повторяющиеся в обоих частях уравнения, т.е. ионы не участвующие в реакции:
Pb2+ + 2NO3 – + 2K+ + 2I– = PbI2¯ + 2K+ + 2NO3 –
Pb2++ 2I– = PbI2¯
Из сокращенного ионного уравнения видно, что сущность реакции сводится к взаимодействию ионов Pb2+ и I–, в результате которого образуется труднорастворимое вещество PbI2.
Пример 4. Определить характер среды водного раствора соли ZnCl2.
Р е ш е н и е. ZnCl2 – соль образованная сильной кислотой HCl и слабым основанием Zn(OH)2, следовательно, подвергается гидролизу по катиону. Так как катион двухзарядный, гидролиз будет протекать по двум ступеням.
I ступень:
а) записываем уравнение процесса диссоциации ZnCl2:
ZnCl2 = Zn2+ + 2Cl–
Подчеркнем ион, по которому идет гидролиз, это ион Zn2+.
б) процесс взаимодействия иона Zn2+ с водой происходит по схеме:
Zn2+ + H+–OH– ⇄ (ZnOH)+ + H+
в) запишем суммарное уравнение гидролиза:
ZnCl2 = Zn2+ + 2Cl–
 Zn2+ + H2O ⇄ (ZnOH)+ + H+
Zn2+ + H2O ⇄ (ZnOH)+ + H+
ZnCl2 + Zn2+ + H2O ⇄ Zn2+ + (ZnOH)+ + 2Cl– + H+
После преобразований получаем:
ZnCl2 + H2O ⇄ Zn(OH)Cl + HCl
В результате гидролиза образуется сильная кислота HCl, поэтому рН < 7.
II ступень:
При рассмотрении гидролиза по второй ступени используется аналогичный подход.
а) Zn(OH)Cl = (ZnOH)+ + Cl–
б) (ZnOH)+ + H+–OH– = Zn(OH)2 + H+
в) Zn(OH)Cl = (ZnOH)+ + Cl–
 (ZnOH)+ + H2O = Zn(OH)2 + H+
(ZnOH)+ + H2O = Zn(OH)2 + H+
Zn(OH)Cl + H2O = Zn(OH)2¯ + HCl
Таким образом, в результате гидролиза по второй ступени образуется сильная кислота HCl, которая создает кислую среду раствора (рН < 7).
1. 8. Растворы. Способы выражения концентрации растворов
Раствор – гомогенная (однородная) система, состоящая как минимум из двух компонентов, один из которых растворитель, другой – растворенное вещество. То есть состав раствора = растворитель + растворенное вещество. Например, водный раствор хлорида натрия состоит из двух компонентов: воды (растворителя) и хлорида натрия (растворенного вещества).
|
|
|
|
|
Дата добавления: 2014-11-07; Просмотров: 715; Нарушение авторских прав?; Мы поможем в написании вашей работы!