
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Синтез альдегидов с использованием методов окисления и дегидрирования
|
|
|
|
Альдегидыявляются химически активным классом органических соединений и широко используются в синтезах лекарственных веществ в качестве исходных веществ и полупродуктов. Однако при синтезе их окислительными методами возникают трудности, связанные с тем, что они, как правило, окисляются легче, чем субстрат, а также способны к реакциям полимеризации и конденсации. В связи с этим альдегиды лучше всего получать каталитическим дегидрированием спиртов.
Каталитическое дегидрирование спиртов ведут в присутствии катализаторов на основе меди и серебра. Процесс идет с хорошим выходом (около 90 %), но при температурах более 200 °С.

Окисление органических соединений в альдегиды возможно лишь при использовании селективных окислителей и катализаторов и специальных технологических приемов.
Применение высокоселективных окислителей в синтезе альдегидов:
· Оксид селена (IV) окисляет активированные метильные и метиленовые группы, находящихся рядом с карбонилом и ароматическим ядром. Таким способом могут быть получены алифатические, ароматические и гетероциклические альдегиды:



Жидкие вещества окисляют без растворителя, для твердых в качестве растворителя используют спирт, этилацетат, ксилол, диоксан. Выходы составляют 50—90 %.
· Комплексы оксида хрома (VI) и ДМСО в присутствии галогеноводорода и кислорода воздуха окисляют первичные спирты:
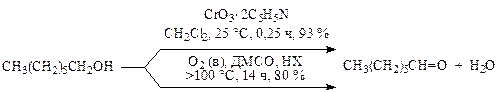
Считают, что в присутствии ДМСО и галогеноводородной кислоты (НХ) кислород окисляет не спирт, а образовавшийся диметилсульфид:
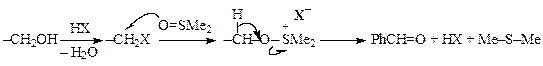
· Периодат натрия окисляет α-гликоли с разрывом углерод- углеродной связи при пониженных температурах 0—20 °C с количественным выходом:

· Уротропин(гексаметилентетрамин) окисляет бензиламины или бензилгалогениды (реакция Соммле):

В этом синтезе в альдегид окисляется алифатический амин, который в связи с повышенной электронной плотностью на атоме азота легко окисляется до имина даже таким окислителем, как уротропин. Считают, что реакция Соммле с галогенидами протекает через стадию образования четвертичной аммониевой соли с гексаметилентетрамином. При нагревании такой четвертичной аммонийной соли в слабокислой среде образуется азометин, гидролизующийся до амина. Амин окисляется уротропином до имина, который гидролизуется до альдегида:
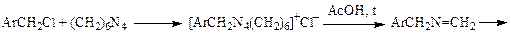

Электроноакцепторные заместители в ароматическом ядре замедляют реакцию (SN1). Ароматические альдегиды по этому методу образуются с выходом 50—80 %. В алифатическом ряду реакция не применяется вследствие малого выхода целевых продуктов (вероятно, в связи с меньшей активности алкилгалогенидов по сравнению с бензильными):
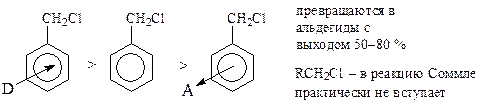
Из бисхлорметильных соединений образуются п- и м -диальдегиды. о -Диальдегиды не образуются.
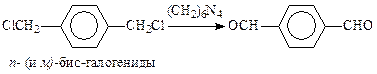
Неселективное окисление толуола и его производных воздухом в жидкой и газовой фазах приводит к образованию смеси продуктов. В жидкой фазе основным продуктом является бензойная кислота и ее производные. Бензальдегид образуется при этом в относительно небольших количествах.
Применение высокоселективных катализаторов (оксиды урана, молибдена и меди) при окислении толуола повышает выход бензальдегида до 85—90 %. Реакцию ведут в газофазной среде пропусканием смеси паров толуола и воздуха над катализатором при температуре 475—500 °С:
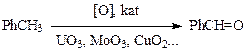
При использовании обычных окислителей необходимо применять специальные технологические приемы:
· Превращение образующегося альдегида в более стабильное производное (например, диацетат при окислении субстрата в присутствии уксусного ангидрида), которое в дальнейшем можно количественно превратить в альдегид (например, гидролизовать).

· Отгонка низкокипящего альдегида из реакционной массы.

· Извлечение образовавшегося альдегида в инертную фазу без окислителя (например, окисление MnO2 в эфире или дихроматом натрия в толуоле). Таким методом можно получить анисовый альдегид, который используется в синтезах некоторых лекарственных веществ, например, гипотензивного средства кардизема:

· Использование особенностей субстрата, окислителя и условий реакций, например:
а) окисление бензилхлорида и его замещенных производных бихроматом в щелочной среде:

В данном случае галогенид окисляется в таких условиях, при которых альдегид сохраняется.
б) При окислении толуола и его производных двуокисью марганца в серной кислоте альдегид сохраняется за счет пониженной активности окислителя и строго определенного температурного режима.

Кислотность среды зависит от количества окислителя. В тех случаях, когда двуокись марганца берут в избытке, используют водную серную кислоту. Если двуокись марганца взята в стехиометрическом соотношении, применяют избыток концентрированной серной кислоты.
Окислитель малоселективный, но низкая скорость реакции при температуре менее 40 °С позволяет получать альдегид, однако уже при 60—70 °С основным продуктом является бензойная кислота.
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 932; Нарушение авторских прав?; Мы поможем в написании вашей работы!