
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Примеры решения задач. Опыт 2. Влияние изменения температуры на смещение равновесия
|
|
|
|
Опыт 2. Влияние изменения температуры на смещение равновесия
Прибор, состоящий из двух шаров, заполнен смесью оксида азота (IV) и его димером. Чистый оксид азота (IV) существует при температуре выше 140 °С. Ниже этой температуры NO2 частично полимеризуется по уравнению
2NO2 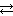 N2O4, ΔH° = –23 кДж.
N2O4, ΔH° = –23 кДж.
NO2 – газ бурого цвета, N2O4 – бесцветен. Изменение температуры позволяет судить о смещении равновесия в системе по изменению интенсивности окраски газов.
Один шар прибора опустить в стакан с холодной, а второй – в стакан с горячей водой. Наблюдать изменение интенсивности окраски газов в шарах.
Требования к результатам опыта
1. Сделать вывод о направлении смещения равновесия в данной реакции при нагревании и охлаждении.
2. Сформулировать правило смещения равновесия при изменении температуры.
3. Написать выражение константы равновесия для данной реакции.
Пример 6.1. При некоторой температуре в системе N2 (г) + 3Н2 (г) 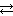 2NH3 (г) равновесные концентрации составляли (моль/л): [N2] = 1,5; [H2] = 1,7; [NH3] = 2,6. Вычислить константу равновесия этой реакции и исходные концентрации азота и водорода.
2NH3 (г) равновесные концентрации составляли (моль/л): [N2] = 1,5; [H2] = 1,7; [NH3] = 2,6. Вычислить константу равновесия этой реакции и исходные концентрации азота и водорода.
Решение. Константа равновесия данной реакции выражается уравнением
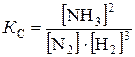 .
.
Подставляя данные задачи, получаем 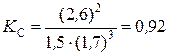 .
.
Исходные концентрации азота и водорода находим на основе уравнения реакции. Согласно уравнению реакции на образование 2 моль NH3 расходуется 1 моль N2. По условию задачи образовалось 2,6 моль NH3, на что израсходовалось 1,3 моль N2. Учитывая равновесную концентрацию азота, находим его исходную концентрацию:  = 1,5 + 1,3 = 2,8 моль/л.
= 1,5 + 1,3 = 2,8 моль/л.
По уравнению реакции на образование 2 моль NH3 необходимо 3 моль H2, а для получения 2,6 моль NH3 требуется 3×2,6/2 = 3,9 моль H2. Исходная концентрация водорода 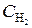 = 1,7 + 3,9 = 5,6 моль/л. Таким образом, К С = 0,92; исходные концентрации
= 1,7 + 3,9 = 5,6 моль/л. Таким образом, К С = 0,92; исходные концентрации  = 2,8,
= 2,8, 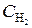 = 5,6 моль/л.
= 5,6 моль/л.
Пример 6.2. Реакция протекает по уравнению А + В 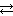 D + F. Определить равновесные концентрации реагирующих веществ, если исходные концентрации веществ А и В, соответственно, равны 2 и 1,2 моль/л, а константа равновесия реакции К С = 1.
D + F. Определить равновесные концентрации реагирующих веществ, если исходные концентрации веществ А и В, соответственно, равны 2 и 1,2 моль/л, а константа равновесия реакции К С = 1.
Решение. Так как все вещества в данной реакции реагируют в одинаковых соотношениях, обозначим изменение концентрации всех реагирующих веществ через x. К моменту установления равновесия образовалось х моль D и х моль F и соответственно [D] = x; [F] = x. По уравнению реакции на столько же уменьшились концентрации А и В, т. е. [A] = 2 – x; [B] = 1,2 – x. Подставим равновесные концентрации в выражение константы равновесия:
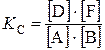 ;
; 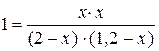 ; х = 0,75.
; х = 0,75.
Отсюда равновесные концентрации равны: [D] = 0,75 моль/л; [F] = 0,75 моль/л;
[A] = 2 – 0,75 = 1,25 моль/л; [B] = 1,2 – 0,75 = 0,45 моль/л.
Пример 6.3. Реакция протекает по уравнению 2SO2 + O2 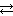 2SO3. В каком направлении сместится химическое равновесие, если объем системы уменьшить в 3 раза?
2SO3. В каком направлении сместится химическое равновесие, если объем системы уменьшить в 3 раза?
Решение. До изменения объема скорости прямой и обратной реакций выражались уравнениями:
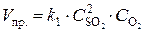 ;
; 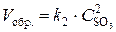 .
.
При уменьшении объема в 3 раза концентрация каждого из реагирующих веществ увеличится в 3 раза. После увеличения концентрации скорость прямой реакции стала 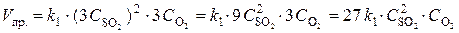 ,
,
т. е. возросла в 27 раз; а скорость обратной – 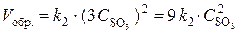 , т. е. возросла в 9 раз. Следовательно, равновесие сместится в сторону прямой реакции (вправо).
, т. е. возросла в 9 раз. Следовательно, равновесие сместится в сторону прямой реакции (вправо).
Пример 6.4. В какую сторону сместится химическое равновесие реакции А + В 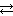 D, если повысить температуру на 30 °С? Температурные коэффициенты скорости прямой (γ1) и обратной (γ2) реакции равны соответственно 2 и 3.
D, если повысить температуру на 30 °С? Температурные коэффициенты скорости прямой (γ1) и обратной (γ2) реакции равны соответственно 2 и 3.
Решение. При повышении температуры на 30° скорость прямой реакции возрастет в 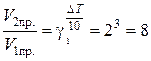 раз, а скорость обратной в
раз, а скорость обратной в 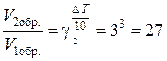 раз. Так как скорость обратной реакции возросла в 27 раз, а скорость прямой в 8 раз, то равновесие этой реакции при повышении температуры сместится в сторону обратной реакции (влево).
раз. Так как скорость обратной реакции возросла в 27 раз, а скорость прямой в 8 раз, то равновесие этой реакции при повышении температуры сместится в сторону обратной реакции (влево).
Пример 6.5. Как изменятся скорости прямой и обратной реакции, если в системе 2NO (г) + О2 (г) 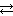 2NO2 (г) уменьшить давление в 2 раза? Произойдет ли при этом смещение равновесия? Если да, то в какую сторону?
2NO2 (г) уменьшить давление в 2 раза? Произойдет ли при этом смещение равновесия? Если да, то в какую сторону?
Решение. До уменьшения давления выражения для скорости прямой и обратной реакции имели вид 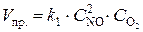 ;
; 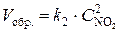 .
.
При уменьшении давления в 2 раза концентрации каждого из реагирующих веществ уменьшаются в 2 раза, так как общий объем системы увеличивается в 2 раза. Тогда 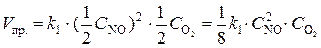 ;
;
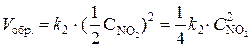 .
.
В результате уменьшения давления скорость прямой реакции уменьшилась в 8 раз, а скорость обратной – в 4 раза. Таким образом, скорость обратной реакции будет в 2 раза больше, чем прямой, и смещение равновесия произойдет в сторону обратной реакции, т. е. в сторону разложения NO2.
Пример 6.6. В каком направлении сместится равновесие реакции
COCl2 ↔ СО + Cl2, ∆ H° х.р. = +112,5 кДж
а) при повышении давления; б) с понижением температуры; в) при уменьшении концентрации хлора?
Решение. а). При повышении давления равновесие смещается в сторону реакции, идущей с уменьшением числа молекул газа, при понижении давления – в сторону реакции, идущей с увеличением числа молекул газа. В левой части приведенной реакции 1 молекула (COCl2), а в правой – 2 (1 СО и 1 Cl2), поэтому при повышении давления равновесие смещается в сторону обратной реакции.
б). При понижении температуры равновесие смещается в сторону экзотермической реакции, при повышении температуры – в сторону эндотермической. В нашем примере прямая реакция эндотермическая (∆ H° х.р. > 0), а обратная – экзотермическая, следовательно, при понижении температуры равновесие сместится в сторону обратной реакции. в). При увеличении концентрации исходных веществ и уменьшении концентрации продуктов реакции равновесие смещается в сторону продуктов реакции. При уменьшении концентрации хлора (продукта реакции) равновесие сместится в сторону прямой реакции, т.е. в сторону образования продуктов реакции.
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 1032; Нарушение авторских прав?; Мы поможем в написании вашей работы!