
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Металлическая связь
|
|
|
|
Атомы металлов отличаются от атомов других элементов тем, что сравнительно слабо удерживают свои внешние электроны. Поэтому в кристаллической решетке металла эти электроны покидают свои атомы, превращая их в положительно заряженные ионы. "Обобществленные" электроны передвигаются в пространстве между катионами и удерживают их вместе. Межатомные расстояния в металлах больше, чем в их соединениях с ковалентной связью. Такая связь существует не только в твердых кристаллах металлов, но и в расплавах и в аморфном состоянии. Она называется металлической.
 рисунок 17
рисунок 17
Металлическая связь - химическая связь, обусловленная наличием большого количества не связанных с ядрами подвижных электронов.
Единая система электронов в металлических веществах называется электронным газом. Металл можно представить в виде остова из положительных ионов, погруженного в электронный газ, который компенсирует силы взаимного отталкивания положительных ионов. В свою очередь, электронный газ может свободно двигаться через решетку, состоящую из ионов металла. В кристаллах металлов атомы ионизированы не полностью, и часть валентных электронов остается связанной. В результате возможно появление частично ковалентных связей между соседними атомами. Вклады ионной и ковалентной составляющей обнаружены во многих металлах. Металлическая связь имеет признаки, характерные как для ковалентной, так и для ионной связи.
Таблица 15 - Сравнение металлической связи с ионной и ковалентной
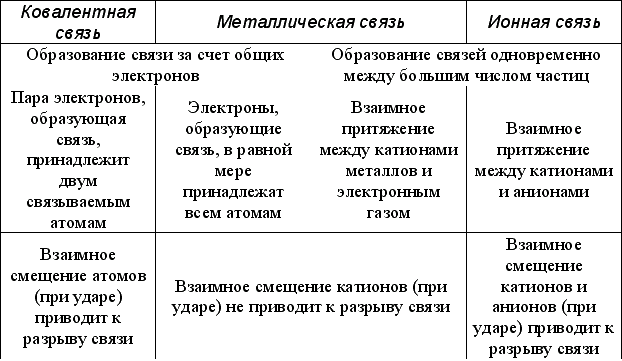
Важнейшим признаком металлов считают высокую электропроводность, которая уменьшается с ростом температуры. Электроны в металле беспорядочно движутся, переходя от одного атома к другому. А положительно заряженные ионы лишь слегка колеблются около своего положения в кристаллической решетке. Благодаря наличию свободных, не связанных с определенными атомами электронов, металлы хорошо проводят электрический ток и тепло. При нагревании металла колебания катионов усиливаются. Электронам труднее продвигаться между ними, поэтому электрическое сопротивление металла увеличивается.
Наличие свободных электронов обусловливают высокую теплопроводность металлов и характерный металлический блеск. Их высокая пластичность и ковкость связаны с возможностью взаимного смещения катионов в металлической кристаллической решетке без разрыва химической связи.
Физические свойства металлов, такие как высокую тепло- и электропроводность, пластичность и ковкость, характерный (металлический) блеск можно объяснить исходя из представлений об электронном газе. Однако количественные расчеты с использованием такой модели строения металлических кристаллов не всегда приводят к результатам, совпадающим с экспериментальными данными. Поэтому для более строгого описания состояния электронов в металле использу
|
|
|
|
|
Дата добавления: 2014-10-23; Просмотров: 939; Нарушение авторских прав?; Мы поможем в написании вашей работы!