
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Карбоновые кислоты
|
|
|
|
Карбоксильная группа в молекулах алифатических кислот должна получать наименьший номер и обозначается она суффиксом – овая кислота:
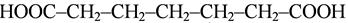 гептандиовая кислота
гептандиовая кислота
|
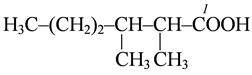 2,3-диметилгексановая кислота
2,3-диметилгексановая кислота
|
Если группа –COOH рассматривается как заместитель (и не входит в родоначальную структуру), то она получает название – карбоновая кислота:
 2-метилциклогексанкарбоновая кислота
2-метилциклогексанкарбоновая кислота
|
Карбоксигруппу обозначают приставкой карбокси - если в соединении присутствует другая группа, имеющая преимущество в перечислении:
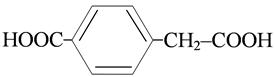 п-карбоксифенилуксусная кислота
п-карбоксифенилуксусная кислота
|
1.3. Электронное строение органических соединений
В составе органических соединений чаще всего находят следующие элементы: C, O, H, N, S, P, которые получили название элементов – органогенов.
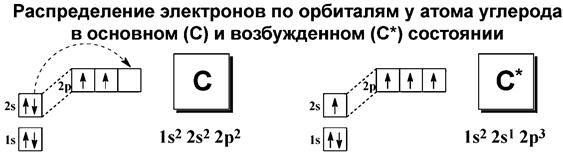
Электронное состояние углерода (невозбужденное) – 1S2 2S2 2P2, при переходе в возбужденное состояние - 1S2 2S1 2P3.
Интерес представляют S и P орбитали, поскольку валентные электроны углерода и элементов-органогенов находятся на них.
Гибридизация орбиталей – смешение нескольких атомных орбиталей различной формы и близкой энергии с образованием такого же числа новых гибридных орбиталей, расположение которых в пространстве соответствует геометрии молекулы. Гибридные орбитали за счет более эффективного перекрывания образуют более прочные связи по сравнению с негибридными. n
В органических соединениях углерод может находиться в одном из трех валентных состояний:
I валентное состояние – sp3-гибридизация, при которой происходит смешивание I S и 3 p-орбиталей, с возникновением 4-х гибридизованных орбиталей, расположенных в пространстве под углом 109º28´ по отношению друг к другу. Углерод в таком состоянии получил название тетрагонального атома углерода и встречается в предельных органических соединениях.
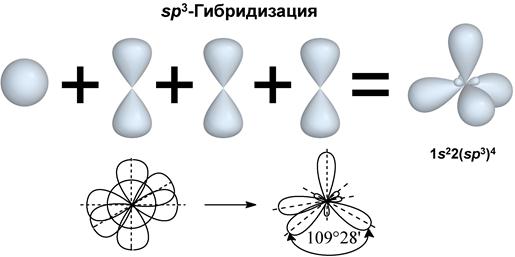
sp3-гибридные орбитали направлены в пространстве к вершинам тетраэдра (тетраэдрическая конфигурация).
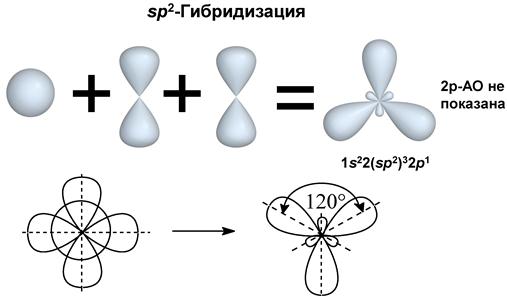
II валентное состояние – sp2-гибридизация, при которой происходит смешивание I S и 2 p-орбиталей, с возникновением 3-х гибридизованных орбиталей, расположенных в одной плоскости под углом 120º по отношению друг к другу. Негибридизованная p-орбиталь расположена перпендикулярно плоскости гибридизованных орбиталей. Углерод в таком состоянии называют тригональным и встречается он в соединениях с двойными связями (атом C в алкенах, карбонильной и карбоксильной группах).
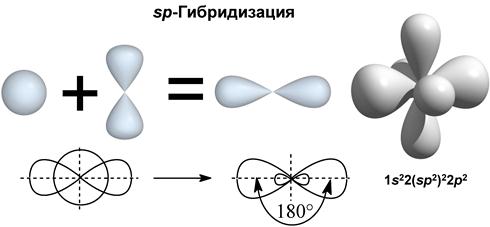
III валентное состояние – sp-гибридизация, при которой происходит смешивание I S и 1p-орбитали с возникновением 2-х гибридизованых орбиталей, расположенных в пространстве под углом 180º (линейно), а две негибридизованые p-орбитали расположены взаимно перпендикулярно друг другу. Sp-гибридизация характерна для углерода, связанного тройной связью или двумя двойными связями.
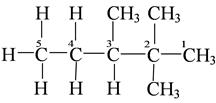
Если углерод образует одну углерод-углеродную связь, то его называют первичным, если две углерод-углеродные связи − то вторичным; если три углерод-углеродные связи – то третичным; если четыре углерод-углеродные связи – то четвертичным.
Например:
|
1-й и 5-й углероды – первичные; 4-й – вторичный; 3-й – третичный;
2-ой – четвертичный.
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 2024; Нарушение авторских прав?; Мы поможем в написании вашей работы!