
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лабораторная работа 3. Термический анализ металлов и сплавов
|
|
|
|
Экспериментальная часть
Задача № 2.1
Изучить при увеличении 200х и зарисовать структуру чистой сурьмы. Объяснить, каким образом микроанализ позволяет обнаружить границы зерен в металле.
Указать, в результате какого явления зерна одного и того же металла кажутся в микроскопе неодинаково окрашенными.
Задача № 2.2
Изучить при увеличении 200х и зарисовать структуру:
а) чистой меди;
б) латуни с содержанием 30% цинка после прокатки и отжига.
Объяснить, почему структура чистого металла (меди) и выбранного в задаче двухкомпонентного сплава (латуни) не отличаются принципиально при просмотре в микроскоп.
Какой способ анализа позволяет различить эти металлы?
Задача № 2.3
Изучить при увеличении 400х и зарисовать микроструктуру:
а) сплава системы «Pb–Sb» с 13% Sb;
б) сплавы той же системы с 25% Sb.
Объяснить, что собой представляют:
а) темная структурная составляющая в обоих образцах, условия её образования и количество фаз, из которых она состоит;
б) светлая структурная составляющая во втором образце (с 25% Sb). Указать условия образования зерен светлой составляющей и причины, по которым её зерна имеют большие размеры, чем зерна темной составляющей.
Контрольные вопросы
1. Что такое микроанализ?
2. Чем отличается металлографический микроскоп от биологического микроскопа?
3. Что такое «микрошлиф»?
4. Что такое «компонент», «фаза», «структура»?
5. Укажите на три основных типа соединений, составляющих структуру сплавов, опишите строение каждого из них, укажите число фаз в этих соединениях.
6. Что такое «анизотропия»?
7. Как образуются зерна в металлах и сплавах?
8. Как влияет размер зерен на механические свойства металлов и сплавов?
9. Что такое «эвтектика» и условия её образования?
10. Что такое «избыточный» компонент?
Цель работы – изучить порядок построения диаграмм состояния сплавов с помощью термического анализа (на примере диаграммы «Pb-Sb»).
Главная цель термического анализа – построение диаграммы состояния сплавов.
Диаграммы состояния сплавов имеют важнейшее значение в теории и практике металловедения и термической обработки деталей машин, станков и инструментов, т.к. на их основе выбирают температуры нагрева изделий при их термической обработке и создают новые сплавы.
Диаграммы состояния сплавов графическим образом отражают структуру сплавов в зависимости от их химического состава и температуры при условии, что сплавы находятся в термодинамически равновесном состоянии, т.е. при заданной температуре имеют наименьшую свободную энергию Гиббса (G). Это означает, что в таком состоянии все превращения в сплаве прошли полностью, и структура сплава сложилась окончательно.
Для того чтобы получить сплав в равновесном состоянии при заданной температуре его необходимо охлаждать (или нагревать) до этой температуры очень медленно и настолько, чтобы при этом все превращения в сплаве прошли до конца.
Диаграммы состояния сплавов строят в координатах «температура – химический состав сплава».
Построение диаграммы состояния осуществляют с помощью термического анализа, в процессе проведения которого получают ряд кривых охлаждения.
На кривой охлаждения определяют температуры критических точек сплавов, химический состав которых известен (см. рис.3.1).
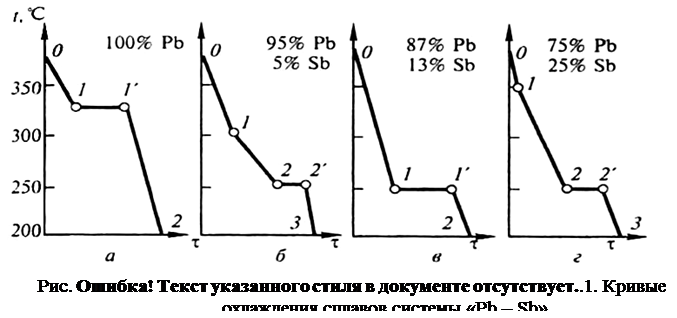
 Критическими точками называют температуры фазовых превращений в металлах и сплавах при их охлаждении или нагреве. В процессе любого превращения, связанного с образованием или исчезновением фаз сплава, выделяется или же поглощается скрытая теплота превращения, например, скрытая теплота кристаллизации (при охлаждении) или плавления (при нагреве сплава).
Критическими точками называют температуры фазовых превращений в металлах и сплавах при их охлаждении или нагреве. В процессе любого превращения, связанного с образованием или исчезновением фаз сплава, выделяется или же поглощается скрытая теплота превращения, например, скрытая теплота кристаллизации (при охлаждении) или плавления (при нагреве сплава).
В результате выделения теплоты превращения скорость охлаждения сплава уменьшается, и на кривой охлаждения, которая строится в координатах «температура – время охлаждения» (см. рис.3.1) образуется точка перегиба – критическая точка.
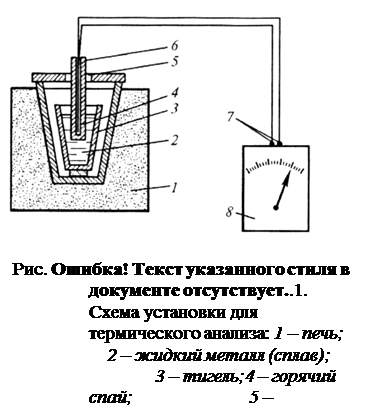
Экспериментальная установка для термического анализа включает (см. рис.3.2):
¾ электрическую печь – для нагрева сплава;
¾ тигель, в котором находится сплав;
¾ термопару с гальванометром (термоэлектрический пирометр) – для измерения температуры сплава;
¾ защитный чехол для термопары – для исключения контакта термопары с расплавленным сплавом.
Для проведения термического анализа (построения кривой охлаждения) тигель вместе со сплавом помещают в печь и нагревают до температуры, превышающей температуру плавления сплава, т.е. переводят его в жидкое состояние. Затем отключают питание печи и при охлаждении сплава через равные промежутки времени измеряют температуру сплава (с помощью термопары по показаниям гальванометра).
По экспериментальным данным строят кривую охлаждения в координатах «температура сплава – время охлаждения» и по наличию точек перегиба или площадок на кривой охлаждения определяют температуру соответствующих им критических точек сплава. Для более точного определения положения критических точек (точек перегиба на кривой охлаждения) иногда проводят построение касательных в месте отклонения линий охлаждения (или нагрева) от первоначальной зависимости.
Датчик температуры – термопара – представляет собой два проволочных проводника из специальных разнородных сплавов, концы которых сварены между собой и образуют горячий спай термопары (см. рис.3.2). Горячий спай термопары помещают в зону (точку), температуру которой следует измерить, а свободные концы термопары присоединяют к регистрирующему прибору (милливольтметру или гальванометру). Эти контакты называют холодными спаями термопары, который имеет комнатную температуру. Если между холодным и горячим спаем термопары имеется некоторая разность температур (Dt), то на концах термопары возникает небольшая по величине термоэлектродвижущая сила (ТЭДС), которая и фиксируется милливольтметром.
 ТЭДС тем больше, чем больше разность температур между указанными спаями и в свою очередь зависит от химического состава сплавов, составляющих термопару. Для перевода значений ТЭДС термопары в градусы Цельсия используют справочные таблицы или специальные тарированные графики (в координатах «t°С–ТЭДС.»).
ТЭДС тем больше, чем больше разность температур между указанными спаями и в свою очередь зависит от химического состава сплавов, составляющих термопару. Для перевода значений ТЭДС термопары в градусы Цельсия используют справочные таблицы или специальные тарированные графики (в координатах «t°С–ТЭДС.»).
Наиболее часто в качестве термопар применяют следующие сочетания металлов и сплавов: платинародий (10% родия) – платина (измерения температур до 1600°С); хромель – алюмель (до 1200°С); хромель – копель (до 800°С).
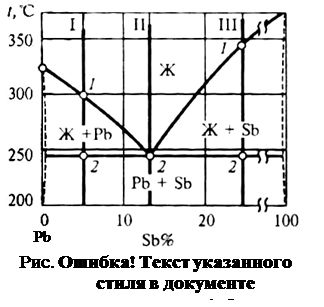
Определив критические точки сплавов данной системы различного химического состава, включая компоненты сплава, можно построить фазовую диаграмму состояния сплавов. Диаграмму состояния сплавов строят в координатах «температура – химический состав» сплава переносом критических точек с кривых охлаждения сплавов различного химического состава на диаграмму состояния. Критические точки соединяют затем линиями, которые, следовательно, представляют собой геометрическое место критических точек всех сплавов данной системы (см. рис.3.3). Далее каждую область диаграммы отмечают символами или названиями фаз, присутствующих в этих областях. Полученная диаграмма называется фазовой диаграммой состояния сплавов.
Фазовые диаграммы отображают равновесное состояние сплава, т.е. полученное при медленном охлаждении (или нагреве).
В неравновесном состоянии сплав находиться после ускоренного охлаждения, когда диффузионные процессы не успели пройти до конца про Однако такое состояние сплава неустойчиво и может изменяться (стремиться к равновесному) под действием внешних факторов (температура, время, давление). В металлических сплавах давление мало влияет на фазовое состояние сплава и считается постоянным и равным ~1 атм.
Наибольший интерес представляют структурные диаграммы, которые отображают не только фазовый состав сплава, но и его структуру (форму, размеры, распределение фаз). Структурные диаграммы позволяют судить о свойствах отдельных сплавов.
Для преобразования фазовой диаграммы в структурную необходимо прежде всего указать на превращения, протекающие на горизонтальных линиях фазовой диаграммы, а затем рассмотреть превращения, происходящие в характерных сплавах данной системы при их охлаждении (нагреве).
 Преобразование фазовой диаграммы состояния сплавов для компонентов, образующих смесь в твердом состоянии, показано на рис.3.4. На диаграмме можно выделить три области и три группы сплавов, которые отличаются по структуре: доэвтектические, эвтектические и заэвтектические. Этим областям соответствуют три характерных сплава I, II, III (см. рис.3.3 и 3.4).
Преобразование фазовой диаграммы состояния сплавов для компонентов, образующих смесь в твердом состоянии, показано на рис.3.4. На диаграмме можно выделить три области и три группы сплавов, которые отличаются по структуре: доэвтектические, эвтектические и заэвтектические. Этим областям соответствуют три характерных сплава I, II, III (см. рис.3.3 и 3.4).
Рассмотрим превращения в сплаве I при медленном охлаждении (аналогично проходят превращения во всех доэвтектических сплавах). До т.1, сплав охлаждается в жидком состоянии. В т.1 (на кривой охлаждения – точка перегиба) начинается кристаллизация сплава – в жидкости зарождаются центры кристаллизации избыточного компонента – Pb, которые в интервале температур от т.1 до т.2 растут и при этом образуются новые центры кристаллизации Pb. В результате этого жидкость обедняется Pb, а химический состав жидкости изменяется по линии ликвидус (см. рис.3.3) и стремится к эвтектическому составу сплава (13%Sb). В т.2 оставшаяся в сплаве жидкость эвтектического состава затвердевает при постоянной температуре в эвтектику (на кривой охлаждения – площадка).
При охлаждении сплава I ниже т.2 его структура не меняется и состоит при комнатной температуре из крупных зерен Pb и эвтектики Э[Pb+Sb].
Жидкость эвтектический сплава II кристаллизуется в т.2 в эвтектику. Температуры начала и конца кристаллизации сплава совпадают (на кривой охлаждения – только площадка). Структура сплава полностью состоит из эвтектики, т.к. исходный химический состав жидкости соответствовал эвтектическому.
Заэвтектический сплав III кристаллизуется аналогично I, но в интервале температур от т.1 до т.2 из жидкости выделяются зерна избыточной Sb, а не Pb, как в I сплаве. Поэтому его окончательная структура состоит из крупных зерен Sb и эвтектики Э[Pb+Sb].
Особенностью этой диаграммы является то, что кристаллизация всех сплавов заканчивается образованием эвтектики при одной и той же постоянной температуре. Поэтому линия солидус является горизонтальной прямой.
При построении диаграммы такого типа линия солидус не должна пересекать линии соответствующие чистым компонентам (100%Pb и 100%Sb), т.к. компоненты имеют одну критическую точку (т.1 на рис.3.3) перехода из жидкого в твердое состояние. При этом на кривой охлаждения наблюдается площадка, так как для чистых компонентов кристаллизация всегда идет при постоянной температуре.
Построенная диаграмма состояния позволяет определить (предсказать) физико-механические свойства сплавов различного химического состава в зависимости от структуры сплава. Эти зависимости установил Н.С. Курнаков.
Закономерности Н.С. Курнакова.
1. Если сплав представляет собой смесь двух фаз, то свойства сплава изменяются прямопропорционально изменению его химического состава. Поэтому для определения свойств подобного сплава достаточно знать свойства фаз, составляющих смесь, а затем построить линейную зависимость изменения свойств от концентрации второго компонента в сплаве.
2. Для однофазных сплавов (твердых растворов) закон изменения свойств – параболический.
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 2182; Нарушение авторских прав?; Мы поможем в написании вашей работы!