
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Найдите для каждого из ниже указанных титрантов характеристику его устойчивости и др. свойстав. Раствор калия бромата
|
|
|
|
Найдите для каждого из ниже указанных титрантов характеристику его устойчивости и др. свойства. Раствор йода
Найдите для каждого из ниже указанных титрантов характеристику его устойчивости и др. cвойства. Раствор калия перманганата
A. Устойчив несколько лет, не изменяется при нагревании до 100 0С., окислительные свойства зависят от [Н+] и природы кислоты.
B. Неустойчив, разложение ускоряется на свету, при нагревании, под действием кислот и оснований, титр устанавливается не сразу.*
C. Устойчив продолжительное время и инертен по отношению к хлороводородной кислоте.
D. Мало устойчив из-за летучести растворенного вещества и окисления кислородом воздуха, особенно на свету.
E. Устойчив неограниченно долго, вещество легко очищается перекристаллизацией.
A. Устойчив несколько лет, не изменяется при нагревании до 100 0С., окислительные свойства зависят от [Н+] и природы кислоты.
B. Неустойчив, разложение ускоряется на свету, при нагревании, под действием кислот и оснований, титр устанавливается не сразу
C. Устойчив продолжительное время и инертен по отношению к хлороводородной кислоте.
D. Мало устойчив из-за летучести растворенного вещества и окисления кислородом воздуха, особенно на свету.*
E. Устойчив неограниченно долго, вещество легко очищается перекристаллизацией.
A. Устойчив несколько лет, не изменяется при нагревании до 100 0С, окислительные свойства зависят от [Н+] и природы кислоты.
B. Неустойчив, разложение ускоряется на свету, при нагревании, под действием кислот и оснований, титр устанавливается не сразу.
C. Устойчив продолжительное время и инертен по отношению к хлороводородной кислоте.
D. Мало устойчив из-за летучести растворенного вещества и окисления кислородом воздуха, особенно на свету.
|
|
|
E. Устойчив неограниченно долго, вещество легко очищается перекристаллизацией.*
10. Какими методами можно определить антипирин
A. Йодометрия
B. Нитритометрия
C. И то, и другое*
D. Ни то, ни другое
11. Какими методами можно определить пероксид водорода
A. Иодометрия*
B. Нитритометрия
C. И то, и другое
D. Ни то, ни другое
12. Какими методами можно определить калия арсенит
A. Йодометрия*
B. Нитритометрия
C. И то, и другое
D. Ни то, ни другое
13. Какими методами можно определить магния сульфат
A. Йодометрия
B. Нитритометрия
C. И то, и другое
D. Ни то, ни другое*
14. Какими методами можно определить новокаин
A. Йодометрия
B. Нитритометрия*
C. И то, и другое
D. Ни то, ни другое
15. Какая, из приведенных ниже полуреакций восстановления калия перманганата наиболее широко используется в количественном анализе:
A. MnO4-+4H+3e-  MnO2 + 2H2O E0=+1,69 MnO2 + 2H2O E0=+1,69
|
B. MnO4-+8H+5e-  Mn2+ + 4H2O E0=+1,51 * Mn2+ + 4H2O E0=+1,51 *
|
C. MnO4- +2Н2О+3е-  MnO2 + 4ОН- E0=+0,60 MnO2 + 4ОН- E0=+0,60
|
D. MnO4-+e  MnO42- + 2H2O E0=+0,58 MnO42- + 2H2O E0=+0,58
|
Е. MnO4- +3Н2О+3е-  MnО(OН)2 + 4ОН- E0=+0,60 MnО(OН)2 + 4ОН- E0=+0,60
|
16. Подберите соответствующие индикаторы для фиксирования точки эквивалентности в перманганатометрии.
A. Раствор крахмала
B. Безиндикаторный*
C. Тропеолин 00
D. Метиловый оранжевый
E. Дифениламин
17. Подберите соответствующие индикаторы для фиксирования точки эквивалентности в йодометрии.
A. Раствор крахмала*
B. Безиндикаторный
C. Тропеолин 00
D. Метиловый оранжевый
E. Дифениламин
18. Подберите соответствующие индикаторы для фиксирования точки эквивалентности в дихроматометрии.
A. Раствор крахмала
B. Безиндикаторный
C. Тропеолин 00
D. Метиловый оранжевый
E. Дифениламин*
19. Подберите соответствующие индикаторы для фиксирования точки эквивалентности в броматометрии.
A. Раствор крахмала
B. Безиндикаторный
C. Тропеолин 00
D. Метиловый оранжевый*
E. Дифениламин
20. Подберите соответствующие индикаторы для фиксирования конечной точки титрования в методе нитритометрии:
|
|
|
A. Раствор крахмала
B. Дифениламин
C. Тропеолин 00 + метиленовый синий*
D. Метиловый оранжевый
E. Метиленовый синий
21. Укажите продукты, которые образуются при взаимодействии натрия нитрита в кислой среде с такими веществами: Ar-NH2
A. Нитрозоамин
B. Нитрозоариленамин
C. Соль диазония*
D. Нитрозоантипирин
E. Азид
22. Какими способами можно приготовить титрованные растворы тиосульфата натрия?
A. Способ приготовленного титра
B. Способ установленного титра*
C. И то, и другое
D. Ни то, ни другое
23. Какими способами можно приготовить титрованные растворы йода?
A. Способ приготовленного титра
B. Способ установленного титра
C. И то, и другое*
D. Ни то, ни другое
24. Какими способами можно приготовить титрованные растворы аммония трисульфатоцеррата (IV)
A. Способ приготовленного титра*
B. Способ установленного титра
C. И то, и другое
D. Ни то, ни другое
25. Реакциями окисления-восстановления называют реакции, идущие:
A. С изменением валентности элементов
B. С отдачей электронов
C. С повышением степени окисления восстановителя
D. С понижением степени окисления окислителя
E. С изменением степени окисления элементов*
26. Подберите подходящий метод определения перекиси водорода прямым способом титрования, содержащей консерванты:
A. Дихроматометрия*
B. Йодометрия
C. Перманганатометрия
D. Нитритометрия
E. Аскорбинометрия
27. Подберите подходящий метод определения Fe(II) в растворе, содержащем HCl:
A. Дихроматометрия*
B. Йодометрия
C. Перманганатометрия
D. Нитритометрия
E. Аскорбинометрия
28. Подберите подходящий метод определения Ca2+
A. Дихроматометрия
B. Йодометрия
C. Перманганатометрия*
D. Нитритометрия
E. Аскорбинометрия
29. Подберите подходящий метод определения C6H5-NH2
A. Дихроматометрия
B. Йодометрия
C. Перманганатометрия
D. Нитритометрия*
E. Аскорбинометрия
30. Подберите подходящий метод определения Na2S2O3
A. Дихроматометрия
B. Йодометрия*
C. Перманганатометрия
D. Нитритометрия
E. Аскорбинометрия
31. Какие титранты можно стандартизировать по мышьяковистому ангидриду?
A. Раствор калия перманганата
B. Раствор йода
C. И то, и другое*
D. Ни то, ни другое
|
|
|
32. Какие титранты можно стандартизировать по первичному стандарту - железо металлическое?
A. Раствор калия перманганата*
B. Раствор йода
C. И то, и другое
D. Ни то, ни другое
33. Какие титранты можно стандартизировать по первичному стандарту - соль Мора?
A. Раствор калия перманганата*
B. Раствор йода
C. И то, и другое
D. Ни то, ни другое
34. Какие титранты можно стандартизировать по первичному стандарту – гидразина сульфату?
A. Раствор калия перманганата
B. Раствор йода
C. И то, и другое*
D. Ни то, ни другое
35. Какие титранты можно стандартизировать по первичному стандарту - калия дихромату?
A. Р-р калия перманганата
B. Р-р йода
C. И то, и другое
D. Ни то, ни другое*
36. На величину скачка титрования на кривой титрования в редокс-методах наиболее существенное влияние оказывает:
A. Редокс-потенциал окислителя
B. Редокс-потенциал восстановителя
C. Разность потенциалов окислителя и восстановителя*
D. Изменение концентраций окислителя и восстановителя
E. Изменение концентрации ионов водорода
37. Укажите, в каких методах окислительно-восстановительного титрования используют для фиксирования конечной точки титрования добавление органического растворителя для извлечения избытка титранта?
A. Перманганатометрия
B. Йодометрия*
C. Цериметрия
D. Броматометрия
E. Нитритометрия
38. Укажите, в каких методах окислительно-восстановительного титрования, для фиксирования конечной точки титрования применяют внешние индикаторы?
A. Нитритометрия*
B. Перманганатометрия
C. Йодометрия
D. Цериметрия
E. Броматометрия
39. Укажите, в каких методах окислительно-восстановительного титрования используют для фиксирования конечной точки титрования специфический индикатор-крахмал?
A. Нитритометрия
B. Перманганатометрия
C. Йодометрия*
D. Цериметрия
E. Броматометрия
40. Укажите, в каких методах окислительно-восстановительного титрования используют для фиксирования конечной точки титрования безындикаторное титрование?
A. Нитритометрия
B. Перманганатометрия*
C. Йодометрия
D. Цериметрия
|
|
|
E. Броматометрия
41. Укажите, какие свойства проявляет йод (в роли какого реагента выступает) в следующей реакции: I2 + I- ------>(I3)-
A. Окислитель*
B. Восстановитель
C. Электрофильный реагент
D. Окислитель и восстановитель
E. Индифферентное вещество
42. Укажите, какие свойства проявляет йод (в роли какого реагента выступает) в следующей реакции:
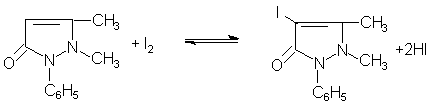
A. Окислитель
B. Восстановитель
C. Электрофильный реагент*
D. Окислитель и восстановитель
E. Индифферентное вещество
43. Какими методами можно определять калия бромат?
A. Йодометрия
B. Нитритометрия
C. И то, и другое*
D. Ни то, ни другое
44. Какими методами можно определять 8-оксихинолин?
A. Йодометрия
B. Нитритометрия
C. И то, и другое
D. Ни то, ни другое*
45. Подберите подходящий метод определения активного хлора в белильной извести.
A. Перманганатометрия через стадию образования труднорастворимых оксалатов
B. Иодометрия*
C. Броматометрия через 8-оксихинолинаты
D. Дихроматометрия
E. Нитритометрия
46. Подберите подходящий метод определения солей Ca2+ и Ba2+
A. Перманганатометрия через стадию образования труднорастворимых оксалатов*
B. Иодометрия
C. Броматометрия через 8-оксихинолинаты
D. Дихроматометрия
E. Нитритометрия
47. Подберите подходящий метод определения солей Mg2+, Al3+ и др
A. Перманганатометрия через стадию образования труднорастворимых оксалатов
B. Иодометрия
C. Броматометрия через 8-оксихинолинаты*
D. Дихроматометрия
E. Нитритометрия
48. Подберите подходящий метод определения стрептоцида белого
A. Перманганатометрия через стадию образования труднорастворимых оксалатов
B. Йодометрия
C. Броматометрия через 8-оксихинолинаты
D. Дихроматометрия
E. Нитритометрия*
49. По какому способу можно приготовить титрованные растворы калия перманганата?
A. Способ приготовленного титра
B. Способ установленного титра*
C. И то, и другое
D. Ни то, ни другое
50. По какому способу можно приготовить титрованные растворы калия дихромата?
A. Способ приготовленного титра
B. Способ установленного титра
C. И то, и другое*
D. Ни то, ни другое
51. По какому способу можно приготовить титрованные растворы калия бромата?
A. Способ приготовленного титра
B. Способ установленного титра
C. И то, и другое*
D. Ни то, ни другое
52. По какому способу можно приготовить титрованные растворы натрия тиосульфата?
A. Способ приготовленного титра
B. Способ установленного титра*
C. И то, и другое
D. Ни то, ни другое
53. Какая окислительно-восстановительная пара содержит наиболее сильный восстановитель?
| A. Fe3+/Fe2+ E0=+0.77 |
| B. Sn4+/Sn2+ E0=+0.15 |
| C. I2/2I- E0=+0.54 |
| Д. S4O62-/2S2O32- E0=+0.09 * |
| E. VO2+/VO2+ E0=+0.99 |
54. Укажите, каким редокс-методом можно определить количественное содержание меди (II) сульфата?
A. Нитритометрия
B. Бромометрия
C. Перманганатометрия
D. Броматометрия
E. Йодометрия*
55. Укажите, каким редокс-методом можно определить количественное содержание активного хлора в хлорамине?
A. Нитритометрия
B. Бромометрия
C. Перманганатометрия
D. Броматометрия
E. Йодометрия*
56. Укажите, каким редокс-методом можно определить количественное содержание фенола?
A. Нитритометрия
B. Бромометрия*
C. Перманганатометрия
D. Цериметрия
E. Йодометрия
57. Укажите, каким редокс-методом можно определить количественное содержание сульфаниловой кислоты?
A. Нитритометрия*
B. Бромометрия
C. Перманганатометрия
D. Броматометрия
E. Йодометрия
58. К редокс-индикаторам относятся:
A. Метиловый оранжевый
B. Фенолфталеин
C. Крахмал
D. Дифениламинсульфокислота*
E. Калия перманганат
59. В какой из редокс-пар окисленная форма является наиболее сильным окислителем?
| А. Сl2/Cl- E0=+1,36 |
| B. Cr2O72-/2Cr3+ E0=+1,33 |
| C. MnO4-/Mn2+ E0=+1,51 * |
| Д. MnO4-/MnО2 E0=+0,60 |
| Е. MnO4-/MnO42- E0=+0,56- |
60. Каким методом редокс-метрии определяют содержание сильных кислот в растворе?
A. Перманганатометрия
B. Йодометрия*
C. Нитритометрия
D. Аскорбинометрия
E. Титанометрия
61. Какими методами редокс-метрии определяют содержание воды в органических соединениях?
A. Перманганатометрия
B. Йодометрия*
C. Нитритометрия
D. Аскорбинометрия
E. Титанометрия
62. Какими методами редокс-метрии определяют содержание новокаина?
A. Перманганатометрии
B. Йодометрии
C. Нитритометрии*
D. Аскорбинометрии
E. Титанометрии
63. Какими методами редокс-метрии определяют содержание формальдегида в формалине?
A. Перманганатометрия
B. Йодометрия *
C. Нитритометрия
D. Аскорбинометрия
E. Титанометрия
64. Подберите первичные стандарты для стандартизации раствора перманганата калия.
A. Мышьяковистый ангидрид
B. Соль Мора
C. И то, и другое *
D. Ни то, ни другое
65. Подберите первичные стандарты для стандартизации раствора йода.
A. Мышьяковистый ангидрид *
B. Соль Мора
C. И то, и другое
D. Ни то, ни другое
66. Подберите первичные стандарты для стандартизации раствора тиосульфата натрия.
A. Мышьяковистый ангидрид
B. Соль Мора
C. И то, и другое
D. Ни то, ни другое*
67. Подберите первичные стандарты для стандартизации раствора церия сульфата.
A. Мышьяковистый ангидрид
B. Соль Мора
C. И то, и другое *
D. Ни то, ни другое
68. Подберите первичные стандарты для стандартизации раствора нитрита натрия
A. Мышьяковистый ангидрид
B. Соль Мора
C. И то, и другое*
D. Ни то, ни другое
69. Подберите подходящий способ титрования при определении восстановителей методом йодометрии
A. Способ прямого титрования
B. Способ обратного титрования
C. И то, и другое*
D. Ни то, ни другое
70. Подберите подходящий способ титрования для определения солей кальция методом перманганатометрии
A. Способ прямого титрования
B. Способ обратного титрования*
C. И то, и другое
D. Ни то, ни другое
71. Подберите подходящий способ титрования для определения окислителей йодометрически
A. Способ прямого титрования
B. Способ обратного титрования
C. И то, и другое
D. Ни то, ни другое*
72. Подберите подходящий способ титрования для определения окислителей методом перманганатометрии.
A. Способ прямого титрования
B. Способ обратного титрования*
C. И то, и другое
D. Ни то, ни другое
73. Укажите тип реакции, которая протекает при определении аскорбиновой кислоты в препарате йодометрическим методом:
А. Окисления-восстановления.*
В. Ацилирования.
С. Нейтрализации.
Д. Осаждения.
Е. Комплексообразования.
74. Сульфаниламидные препараты содержат первичную ароматическую аминогруппу. Укажите метод количественного определения этих соединений:
А. Нитритометрия.*
В. Йодометрия.
С. Дихроматометрия.
Д. Перманганатометрия.
Е. Цериметрия.
75. В какой среде чаще всего проводят перманганатометрическое титрование солей железа (II)?
А. В сернокислой.*
В. В спиртовой.
С. В азотнокислой.
Д. В щелочной.
Е. В солянокислой.
76. При йодометрическом определении формальдегида в формалине используют обратное титрование. Избыток раствора йода оттитровывают стандартным раствором:
А. Натрия тиосульфата.*
В. Натрия нитрата.
С. натрия сульфата.
Д. натрия карбоната.
Е. Натрия фосфата.
77. Для йодометрического определения окислителей в качестве титранта можно использовать:
A. Рабочий раствор КОН
B. Рабочий раствор NaOH
C. Рабочий раствор КМnО4
D. Рабочий раствор K2Cr2O7
E. Рабочий раствор Na2S2O3*
78. По какому веществу проводят стандартизацию раствора перманганата калия?
A. Калия йодид
B. Натрия тетраборат
C. Натрия нитрит
D. Калия бихромат
E. Кислота щавелевая*
79. Методами редоксиметрии проводят количественное определение окислителей и восстановителей. Количественное определение, какого вещества можно провести этими методами:
A. Калия хлорид
B. Натрия гидроксид
C. Натрия гидрокарбонат
D. Магния сульфат
E. Пероксид водорода*
80. Натрия салицилат содержит фенольный гидроксил. Предложите метод количественного определения этой соли.
A. Аргентометрия
B. Алкалиметрия
C. Меркуриметрия
D. Комплексонометрия
E. Броматометрия*
81. Натрия тиосульфат определяют методом прямого йодометрического титрования. В качестве индикатора используют крахмал. Как определяют конечную точку титрования?
A. По обесцвечиванию раствора
B. По появлению синего окрашивания *
C. По появлению красного окрашивания
D. По выпадению белого осадка
E. По выпадению бурого осадка
82. Необходимо определить количество салицилата натрия в растворе. Какой метод титриметрического анализа можно использовать для количественного определения ароматических соединений?
A. Метод бромометрии *
B. Метод аргентометрии
C. Метод меркуриметрии
D. Метод комплексонометрии
E. Метод цериметрии
83. В окислительно-восстановительных реакциях перманганат калия KMnO4 является только окислителем. При протекании реакции в кислой среде малиновый раствор обесцвечивается. Укажите продукт восстановления MnO4–-иона в кислой среде.
A. Mn(OH)2
B. MnO42–
C. Mn2+ *
D. Mn(OH)
E. MnO2
84. В йодометрии применяют титрованные растворы йода и Na2S2O3. Какое вещество применяют для стандартизации раствора натрия тиосульфата?
A. NaCl
B. K2Cr2O7 *
C. As2O3
D. K2CO3
E. Na2B4O7
85. Определение солей Fe(II) методом перманганатометрии в присутствии С1-ионов можно проводить, если их сопряженное влияние устранить добавлением:
A. Смеси MnSO4, H3РО4, H2SО4 *
B. Фосфатной буферной смеси
C. Ацетатной буферной смеси
D. Бромат-бромидной смеси
E. Смеси MgCI2, NH4CI, NH4OH
86. Укажите условие, при котором окислительно-восстановительная реакция протекает в прямом направлении:
A. Еok0 < 0
B. Еok0 = Евос0
C. Еok0 > Евос0 *
D. Еok0 > 0
E. Еok0 < Евос0
87. Для определения содержания анальгина в препарате использовали метод прямого йодометрического титрования. Титрантом данного метода является:
А. Раствор йода в растворе калия йодида.*
В. Раствор натрия тиосульфата.
С. Раствор калия йодида.
Д. Раствор калия дихромата.
Е. Раствор калия йодата.
88. Метод нитритометрии основан на диазотировании первичных ароматических аминов. Количественное определение, какого из приведенных веществ можно провести этим методом.
А. Стрептоцид.*
В. Кислота щавелевая.
С. Кислота аскорбиновая.
Д. Кислота ацетилсалициловая.
Е. Глюкоза.
89. Укажите, как определяют конечную точку титрования в методе перманганатометрии?
А. По появлению окраски раствора от избыточной капли титранта.*
В. По образованию комплексного соединения индикатора с титрантом
С. По образованию малорастворимого соединения индикатора с титрантом
Д. По образованию малорастворимого соединения индикатора с определяемым веществом
Е. По разрушению комплексного соединения титранта с определяемым веществом
90. Методом прямого йодометрического титрования определяют:
А. KMnO4
В. K2Cr2O7
С. H2O2
Д. Na3AsO3*
Е. Ca(OCl)2
91. Укажите, какие из приведенных факторов оказывают наибольшее влияние на скорость редокс-реакций, применяемых в титриметрическом анализе.
А. Природа и концентрация реагирующих веществ, катализаторы, температура. *
В. Редокс-потенциал системы.
С. Комплексообразующие добавки, pH.
Д. Концентрация ионов водорода.
Е. Природа реагирующих веществ.
92. Какой метод редоксметрии можно применить для количественного определения 8-оксихинолина?
А. Бромометрия *
В. Йодометрия
С. Нитритометрия
D. Йодхлорметрия
Е. Дихроматометрия
93. Назовите один из методов редокс-метрии, с помощью которого можно количественно определить указанные вещества Н2О2, NaNO2, FeSO4?
А. Перманганатометрия *
В. Йодиметрия
С. Йодометрия
D. Аскорбинометрия
Е. Феррометрия
94. Какой индикатор применяют для установления точки конца титрования при количественном определении оксида мышьяка (III) As2O3 методом броматометрии?
А. Метиловый красный *
В. Крахмал
С. Ферроин
D. Эозин
Е. Тропеолин 00
95. Укажите способ титрования при количественном определении окислителей методом йодометрии?
А. Заместительное *
В. Прямое
С. Обратное
D. Обратное с йодометрическим окончанием
Е. Реверсивное
Осадительное и комплексометрическое титровани е
1. Осадительное титрование - это:
А. Метод анализа, основанный на реакции образования труднорастворимых соединений
В. Метод анализа, основанный на измерении объема титранта-осадителя, затраченного на количественное осаждение определяемого компонента*
С. Метод анализа, основанный на измерении объема титранта, затраченного на количественное взаимодействие с определяемым компонентом
Д. Метод анализа, основанный на точном измерении массы определяемого вещества в виде осадка
2. Кривая осадительного титрования - это:
A. Графическая зависимость концентрации ионов водорода от объема титранта
B. Графическая зависимость изменения растворимости при титровании*
C. Графическая зависимость изменения концентрации определяемого иона в процессе титрования от объема титранта
D. Графическая зависимость величины редокс-потенциала от объема титранта
E. Графическая зависимость изменения концентрации титранта от объема определяемого иона в процессе титрования
3. Точка конца титрования в осадительном титровании фиксируется
A. визуально, с помощью рН-индикаторов
B. визуально, с помощью редокс-индикаторов
C. визуально, с помощью осадительных индикаторов*
D. только инструментальными методами
E. всеми перечисленными способами
4. Вещества можно оттитровать методом осадительного титрования (продукт реакции бинарный труднорастворимый электролит), если:
А.растворимость осадка 10-4
В. ПР осадка 10-5
С. ПР осадка 10-7
Д. ПР осадка < 10-10 *
С. ПР осадка 10-8
5. Титрованный раствор нитрата серебра готовят по способу:
А. установленного титра*
В. приготовленного титра
С. и то, и другое
Д. ни то, ни другое
6. Титрованный раствор тиоцианата аммония готовят по способу:
A. установленного титра*
B. приготовленного титра
C. и то, и другое
D. ни то, ни другое
7. В качестве первичных стандартов в аргентометрии используют:
A. натрия хлорид
B. калия хлорид
C. и то, и другое*
D. ни то, ни другое
8. В методе аргентометрии для фиксирования точки конца титрования используют индикаторы
A. осадительные
B. адсорбционные
C. металлохромные
D. все названные*
E. ни один из названных.
9. Определение по методу Мора проводят в области рН:
A. 1,5 - 10,5
B. 2 - 8
C. 0 - 14
D. 6,5 - 10,3 *
E. 6,5 - 7,5
10. В качестве индикатора при определении по Мору применяют:
A. железо-аммонийные квасцы
B. хромат калия *
C. дифенилкарбазон
D. эозин
E. натрия нитропруссид
11. Методом Мора количественно определяют:
A. Cl-, Вr-, I-, SCN-
B. Br-, I-
C. Cl-, Br- *
Д. Cl-, Br-, I-
12. Галогениды определяют по методу Фольгарда способом:
A. прямого титрования
B. обратного титрования *
C. заместительного титрования
D. реверсивного титрования
E. всеми перечисленными способами
13. Для создания кислой среды при определении галогенидов по Фольгарду используется:
A. серная кислота
B. хлороводородная кислота
C. уксусная кислота
D. азотная кислота *
E. все названные кислоты
14. В меркурометрии для фиксирования точки конца титрования в качестве индикаторов применяют:
A. флуоресцеин
B. дифенилкарбазон*
C. эозин
Д. мурексид
Е. калия хромат
15. В комплексонометрии в качестве титрантов чаще используют:
A. монодентатные лиганды
B. полидентатные лиганды*
C. и то, и другое
D. ни то, ни другое
16. Титрованный раствор трилона Б готовят по способу
A. установленного титра *
B. приготовленного титра
C. и то, и другое
D. ни то, ни другое
17. Кривая комплексиметрического титрования - это графическая зависимость
A. -lg[Me] от объема титранта *
B. рМ от объема титранта
C. и то, и другое
Д. ни то, ни другое
18. Фиксирование точки конца титрования в комплексонометрии проводят при помощи:
A. осадительных индикаторов
B. редоксиндикаторов
C. металлохромных индикаторов *
Д. безындикаторного титрования (по избыточной капле окрашенного титранта)
Е. всего названного
19. Выбрать способ определения Мg2+, Са2+, Zn2+, если они реагируют с трилоном Б стехиометрически, с достаточной скоростью, легко подобрать индикатор
A. способ обратного титрования
B. способ заместительного титрования
C. способ прямого титрования*
D. реверсивное титрование
E. всеми перечисленными способами
20. Выбрать способ титрования для определения катиона Меn+, если он реагирует с трилоном Б достаточно быстро, невозможно подобрать индикатор
A. способ обратного титрования
B. способ заместительного титрования*
C. способ прямого титрования
Д. реверсивное титрование
D. всеми перечисленными способами
21. Выбрать способ для определения солей серебра по Фольгарду
A. способ обратного титрования
B. способ заместительного титрования
C. способ прямого титрования*
Д. реверсивное титрование
22. В качестве индикаторов при комплексонометрических титрованиях применяют
A. эриохром черный Т *
B. эозин
C. метиловый оранжевый
D. Железо-аммонийные квасцы
E. дифенилкарбазон
30. В качестве первичных стандартов в меркурометрии используют
A. натрия хлорид
B. калия хлорид
C. и то, и другое*
D. ни то, ни другое
31. Методом прямой комплексонометрии определяют концентрацию:
А. Катионов металлов.*
В. Анионов сильных кислот.
С. Анионов слабых кислот.
Д. Гидроксид-ионов.
Е. Ионов водорода.
32. Для количественного определения серебра в фармацевтическом препарате методом Фольгарда для фиксирования конечной точки титрования используют индикатор:
А. Железо-аммонийные квасцы.*
В. Натрия эозинат.
С. Калия хромат.
Д. Крахмал.
Е. Дифенилкарбазон.
33. Анализируемый препарат содержит калия нитрат и калия хлорид. Предложите метод количественного определения калия хлорида:
А. Аргентометрия.*
В. Нитритометрия.
С. Перманганатометрия.
Д. Иодометрия.
Е. Йодхлорметрия.
34. Для количественного определения магния сульфата в растворе можно использовать метод:
А. Комплексонометрии.*
В. нитритометрии.
С. Аргентометрии.
Д. Тиоцианатометрии.
Е. Ацидиметрии.
35. Количественное содержание калия хлорида определяют методом Мора. Какой индикатор применяют для фиксирования конечной точки эквивалентности?
A. Хромат калия *
B. Нитропруссид натрия
C. Тиоционат железа
D. Метиловый оранжевый
E. Дифенилкарбазон
36. Раствор калия йодида титруют стандартным раствором серебра нитрата. В качестве индикатора пригоден:
A. Железо-аммонийные квасцы *
B. Калия хромат
C. Натрия эозинат
D. Флуоресцеин
E. Мурексид
37. Какой рабочий раствор (титрант) используют в методе Мора?
А. Раствор серебра нитрата *
В. Раствор ртути (II) нитрата
С. Раствор железа (III) нитрата
Д. Раствор ртути (I) нитрата
Е. Раствор серебра ацетата
38. Для определения массовой доли хлорид-ионов в поваренной соли приготовили раствор и оттитровали его раствором серебра нитрата в присутствии индикатора калия хромата. Какой метод анализа при этом был использован?
А. Метод Мора.*
В. Метод Фольгарда.
С. Метод Фаянса-Ходакова.
Д. Меркурометрическое титрование.
Е. Трилонометрия.
39. Для стандартизации титрованного раствора трилона Б используют стандартный раствор:
А. Цинка сульфата.*
В. Натрия тетрабората.
С. натрия хлорида.
Д. Калия дихромата.
Е. Щавелевой кислоты.
40. Для определения массовой доли натрия хлорида в лекарственном препарате используют метод Фаянса-Ходакова. Титрование проводят в присутствии раствора индикатора:
А. Флуоресцеина.*
В. Метилового красного.
С. Калия хромата.
Д. Аммония железа (III) сульфата.
Е. Фенолфталеина.
41. Титрант метода комплексонометрии – раствор трилона Б – образует с катионами металлов независимо от их валентности комплексные соединения в соотношении:
А. 1:1*
В. 1:3
С. 1:2
Д. 2:1
Е. 3:1
42. Выберите титриметрический метод количественного определения магния сульфата в растворе для инъекций:
А. Комплексонометрия.*
В. Цериметрия.
С. Кислотно-основное титрование.
Д. Йодхлорметрия.
Е. Нитритометрия.
43. Общую жесткость воды определяют прямым титрованием стандартным раствором трилона Б в присутствии индикатора:
A. Раствор натрия нитропруссида
B. Флуоресцеин
C. Калия хромат
D. Эриохром черный Т*
E. Дифенилкарбазон
44. Калия йодид определяют по методу Фаянса. Какой индикатор используют для фиксирования конечной точки титрования?
A. Калия хромат
B. Эозин *
C. Фенолфталеин
D. Метиловый оранжевый
E. Тропеолин-00
45. При комплексометрическом определении многих неорганических лекарственных средств, содержащих металлы, используют раствор динатриевой соли этилендиаминтетраацетатной кислоты (трилон Б), который образует устойчивые хелатные соединения с катионами металлов. К какому типу лигандов принадлежит трилон Б?
A. Полидентантные
B. Дидентантные
C. Монодентантные
D. Бидентантные*
E. Тридентантные
46. К 10,20 дм3 0,1000 моль/дм3 раствора натрия хлорида добавили 10,20 дм3 0,1 моль/дм3 раствора серебра нитрата в присутствии калия хромата. Какую окраску приобретет осадок?
A. Черную
B. Бледно-желтую
C. Красной
D. Красно-коричневую
E. Осадок останется белым *
47. Химику-аналитику необходимо определить количественное содержание хлороводородной кислоты в смеси, которая содержит азотную кислоту. Какой титриметрический метод анализа может быть использован?
А. Аргентометрия.*
В. Иодометрия.
С. Комплексонометрия.
Д. Кислотно-основное титрование.
Е. Перманганатометрия.
|
|
|
|
|
Дата добавления: 2014-11-09; Просмотров: 987; Нарушение авторских прав?; Мы поможем в написании вашей работы!