
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекція №4. Біологічне окисНення. 1 страница
|
|
|
|
План лекції:
1. Розвиток уявлень про біологічне окиснення.
2. Відмінність біологічного окиснення від окиснення у неживій природі.
3. Ферменти, що каталізують біологічне окиснення.
Література: [1] с. 130-147.
В процесі життєдіяльності організми поглинають з навколишнього середовища енергію в адекватній формі, а потім повертають її еквівалентну кількість, але вже в іншому виді.
Основним носієм енергії є електрон (е -). Одержавши визначену кількість енергії, він збуджується: переходить на більш високий енергетичний рівень. Роблячи зворотний шлях на нижню орбіту, електрон вивільняє таку ж кількість енергії.
Для всіх організмів, що живуть на Землі, основним джерелом енергії служить сонячне випромінювання. Існує дві групи організмів, що розрізняються за способом харчування - аутотрофи і гетеротрофи.
Аутотрофи (зелені рослини) здатні безпосередньо уловлювати сонячну енергію і використовувати її для створення органічних сполук.
Гетеротрофи – це організми, що асимілюють готові органічні речовини, які мають визначений запас потенційної енергії. У процесі їхньої життєдіяльності енергія вивільняється.
Великий художник, вчений і натураліст епохи ренесансу Леонардо Да Вінчі писав: «Життя можливе там, де може горіти вогонь». Іншими словами, процеси життєдіяльності здійснюються тільки при наявності енергії, отриманої при окиснюванні.
У живих організмах енергія, що вивільняється при окиснюванні, запасається, в основному, у виді хімічної енергії, що після використання переходить у теплоту.
При окиснюванні в неживій природі відбувається пряме приєднання Оксигену:
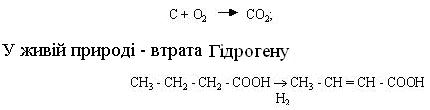
Такий процес можливий лише в тому випадку, якщо в реакційній суміші міститься речовина, що з'єднується з Гідрогеном, який вивільнився. Цю речовину називають акцептором Гідрогену, а сполуку, що є джерелом Гідрогену, – донором цього елемента. Універсальним акцептором Гідрогену виступає Оксиген повітря.
Загальна умова окиснювання – віддача електрона:
Fe2+ → Fe3+
–e
Процес вивільнення енергії в живому організмі забезпечує усі форми життєдіяльності (у тому числі перетворення речовин їжі в компоненти клітини), а також підтримку організму в стані динамічної рівноваги, незважаючи на постійні зміни умов зовнішнього середовища.
Типовим прикладом окиснювання в неживій природі є горіння. Воно супроводжується значним підвищенням температури. При горінні виділяється величезна кількість енергії, утворюється суміш різноманітних речовин непостійного складу. Характер виділення енергії, що з'являється при горінні, можна порівняти з нищівною силою водоспаду, що падає з високої гори. Якщо розділити його на кілька водоспадів, що падають з невеликої висоти, то кожний з них буде мати менший напір.
У процесі еволюції в живих організмах виробилися механізми перетворення могутнього потоку енергії, що вивільняється при повному окиснюванні харчових речовин, у невеликі порції, що запасаються, приблизно на 50 %, у виді хімічної енергії, використовуваної для процесів синтезу, інші 50% виділяються у виді теплоти.
Встановлено, що універсальним резервом хімічної енергії, що утворюється в процесі окиснювання органічних речовин у клітинах, є аденозинтрифосфат (АТФ). Ця сполука складається з аденіну, рибози і трьох залишків фосфорної кислоти. Таким чином, вивільнення енергії при окиснюванні органічних речовин, на відміну від горіння, відбувається поступово. При цьому не виникають ті значні перепади температури, що характерні для горіння. Незалежно від окремих етапів окисного розщеплення органічних речовин у кінцевому рахунку утворюються ті ж продукти розпаду (СО2 і Н2О) і виділяється стільки ж енергії.
Оксиген з повітря надходить в організм через дихальні шляхи в легені і кров, що транспортує його до всіх клітин. Однак Оксиген у тканинах не приєднується безпосередньо до вихідного джерела енергії – будь то Карбоген, амінокислота або жирна кислота. Ці сполуки поступово деградують, втрачаючи гідроген, електрони, що реагують з Оксигеном.
Таким чином, джерелом енергії в організмі стає реакція між Гідрогеном і Оксигеном, у результаті чого утворюється вода.
Оксид Карбогену, що є обов'язковим продуктом окиснювання, відщеплюється тканинними ферментами від кислотних груп – СООН, амінокислот, жирних кислот і ін.
На вивчення шляхів взаємодії органічних речовин і оксигену в клітинах були спрямовані зусилля багатьох дослідників, що висували гіпотези, які часом заперечували одна одній. Роль Оксигену для життя не викликала сумнівів. Задача полягала в тому, щоб з'ясувати, чому Оксиген повітря не окиснює організм і сам процес окиснювання відбувається тільки в тканинах, а не на шляху до них. Виявилося, що в тканинах відбувається активація Оксигену, яку потребує цей елемент для швидкої взаємодії з речовинами, що окиснюються (те ж спостерігається і поза організмом).
На рубежі XІ і XX ст. російський вчений А. Н. Бах і незалежно від нього в Німеччині К. Емглер і В. Вілд висунули гіпотезу про утворення пероксидів органічних сполук як початкового етапу біологічного окиснювання. Відповідно до цієї гіпотези молекула Оксигену переходить в активний стан за рахунок розриву в ній подвійного зв'язку за допомогою "внутрішньої коливальної енергії" самої сполуки, що окиснюється і при участі ферментів-оксидаз.
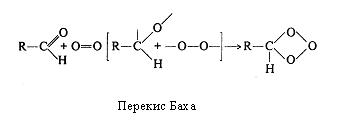
На початку XX сторіччя склалися дві концепції: біологічного активування Оксигену і активування Гідрогену. Однак протистояння їхніх прихильників продовжувалося недовго. У 1925 р. Д. Кейлін відкрив в аеробних біологічних об'єктах цитохроми, тобто ферменти, що дозволило вченим декількома роками пізніше зв'язати активування Оксигену і Гідрогену воєдино. Цьому сприяло виявлення О.Варбургом (1928 р.) цитохромоксидази, що називають "дихальним ферментом Варбурга". Саме цитохромоксидаза виявилася тим ферментом, що безпосередньо активує Гідроген, а цитохроми - ферментами, що "знімають" електрони у Гідрогену і передають їх цитохромоксидазі.
Сучасна теорія біологічного окиснювання об'єднала теорії Баха-Варбурга і Паладіна-Віланда на новому рівні розвитку досліджень цієї наукової проблеми. Отже, біологічне окиснювання – це процес відщіплення атомів Гідрогену або електронів від субстрату і передача їх через ряд проміжних етапів на молекулярний Оксиген. У цьому процесі беруть участь ферменти: пирідинозалежні дегідрогенази (їх коферментну функцію виконує нікотинамідаденіндинуклеотид-НАД або нікотинамідаденіндинуклеотидфосфат - НАДФ), флавінозалежні дегідрогенази – флавінові ферменти (до складу їхньої простетичної групи входить флавінаденіндинуклеотид – ФАД або флавінаденінфосфат – ФАДФ); цитохроми (містять у якості простетичної групи залізопорфіринову кільцеву систему), а також убіхінон (коензим Q) і білки, що містять негемінове залізо.
Роль окисНювально-відновних ферментів У біологічно-му окисНюванні.
Пірідинозалежні дегідрогенази. До цієї групи каталізаторів відносяться складні ферменти, небілковою частиною яких є НАД і НАДФ (рис.3). Останній відрізняється від НАД наявністю ще однієї молекули фосфорникотинамідаденіннуклеотидної кислоти.

Рис. 3. Будова никотинамідаденіндинуклеотиду.
У клітинах НАДзалежні дегідрогенази беруть участь переважно в процесах, зв'язаних з переносом електронів від органічних субстратів до Оксигену.
НАД містить два залишки азотистих основ, залишки двох рибоз і двох фосфорних кислот. Однією азотистою основою є аденін, другою – амід нікотинової кислоти, якому властива функція вітаміну РР (антипелагричного). З назв азотистих основ і виникла абревіатура НАД.
Акцептором Гідрогену в НАД і НАДФ є нікотинамід в окисненій формі. В окисненій формі ця сполука містить у кільці п’ятивалентний Нітроген. Після відновлення один атом Гідрогену приєднується до Карбогену, у результаті чого розривається його подвійний зв'язок із сусіднім атомом. Електрон другого атома Гідрогену гасить заряд п’ятивалентного Нітрогену і той перетворюється в тривалентний. Приєднання електрону і зниження валентності є відбудовним процесом. Протон, що залишився, переходить у середовище.
Забираючи атоми Гідрогену від субстрату, нікотинамід переходить з окисненої форми у відновлену, і з акцептора Гідрогену стає його донатором.
Флавінозалежні ферменти ( флавінові ферменти). Наступним акцептором атомів Гідрогену виступає група флавінових ферментів, що здійснюють його перенос (електронів і протонів) від відновленої форми НАД (НАДН2) до цитохромів. До флавінових дегідрогеназ відносяться складні ферменти, небілковою частиною яких є флавінаденіндинуклеотид (ФАД) (рис. 4). На відміну від нікотинамідаденін-динуклеотиду ФАД містить замість аміду нікотинової кислоти залишок вітаміну В2. Він з'єднаний з похідними рибози (рибітолом), двома залишками фосфорної кислоти, рибозою і аденіном.
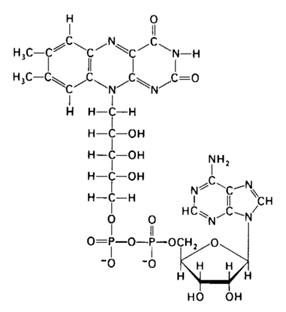
Рис. 4. Будова флавінаденіндинуклеотиду.
Гетероциклічне ядро вітаміну В2 є ізоалоксазином. Його сполуки називають флавінами, а білки, з'єднані з флавінами, – флавопротеїнами. До них відноситься фермент, що є дегідрогеназою, що реагує з НАДН2. Отже, цей флавопротеїн, як правило, не вступає в реакцію безпосередньо з органічними сполуками, що окиснюються, тому його називають вторинною дегідрогеназою. Разом з тим, є субстрати, що безпосередньо окиснюються флавопротеїнами. Вони транспортують відщиплені протони і електрони на Оксиген, і в результаті утворюється не вода, а оксид Гідрогену. Під впливом ферменту каталази він розщеплюється на воду і молекулярний Оксиген.
Крім ФАД, в окиснювально-відновних реакціях бере участь його фосфоролюване похідне – ФАДФ, що містить додатковий залишок фосфорної кислоти, приєднаний до рибози. В усіх цих сполуках вихідними речовинами є вітаміни, що повинні надходити в організм у складі їжі, щоб не порушився фундаментальний процес біологічного окиснювання – основне джерело енергії для процесів життєдіяльності.
Наступним ферментом, який каталізує перенос атомів Гідрогену від відновлених флавонуклеотидів, є кофермент Q, або убіхінон, сполука близька до вітаміну К.
Кофермент Q виступає посередником між ФАДН2 і цитохромами. Він являє собою похідне бензохінону з довгим бічним ланцюгом, що складається з 10 ізопреноїдних одиниць.
Відновлена форма флавінових дегідрогеназ у ланцюзі дихальних ферментів передає атоми гідрогену (електрони і протони) до Q. Приєднуючи гідроген, убіхінон з окисненої форми перетворюється у відновлену.
Подальший перенос електронів від відновленої форми убіхінону на Оксиген здійснює система цитохромів.
Цитохроми. Цитохроми (від грец. cytos – клітина, chroma – колір) –пігменти, пофарбовані в червоний колір завдяки наявності в їхній молекулі заліза. Встановлено, що в ланцюзі окиснювання ланка цитохромів включається у визначеній послідовності між убіхіноном і Оксигеном.
цит В → цит С1 → цит С → цит А → цит А3
Причому цитохроми В, С1, А1 виконують роль проміжних переносників електронів, а цитохром А3 (цитохромоксидаза) є кінцевим дихальним ферментом, що вступає в безпосередній контакт із Оксигеном. Усі цитохроми мають простетичну гемінову групу, ідентичну гему гемоглобіну.
Цитохроми відрізняються одне від одного не тільки простетичними групами. Розходження у властивостях окремих їхніх видів обумовлено будовою білкової частини. Так, у цитохромах В і С гем прикритий "ширмою" з пептидів, що перешкоджає їхній безпосередній реакції з Оксигеном. У ході каталітичного процесу валентність Феруму, що міститься в цитохромах, зворотно міняється (Fe2+ > Fe3+).
Окислена форма цитохромоксидази (Fe3+) приймає електрони від відновленого цитохрому С, переходячи у відновлену форму (Fe2+), що потім знову окиснюється в Fe3+ молекулярним Оксигеном на етапі цитохрому А3. При цьому утворюється активний Оксиген, що приєднує два протони з навколишнього середовища, у результаті чого і виникає молекула води.
У такий спосіб цитохроми завершують транспорт електронів від субстрату, що окиснюється, на Оксисен.
Лекція №5. Вуглеводи. будова, біологічна роль. Класифікація.
План лекції:
1. Загальна характеристика хімічної природи та біологічної ролі вуглеводів.
2. Класифікація вуглеводів, роль триоз та пентоз у живому організмі.
3. Основні гексози, олігосахариди. Будова, властивості та функції.
4. Будова, властивості та функції полісахаридів.
Література: [1] с. 80-102.
Вуглеводи – біохімічні сполуки, що утворюються в рослинах як первинні продукти фотосинтезу. Їхня назва походить від загальної формули цієї групи речовин – Сn(Н2О)n. У їх склад входять Карбоген, Гідроген і Оксиген (співвідношення атомів Гідрогену і Оксигену в них таке ж, як у воді).
По хімічному складу вуглеводи є альдегідами і кетонами багатоатомних спиртів, з яких вони утворюються при окисненні первинної або вторинної спиртової групи.
У рослинах вуглеводи становлять 80…90 % маси, причому в різних час-тинах вміст їх різний. Так, у зелених частинах рослин він становить 2,5…6 %, у бульбах картоплі і коренеплодах – 10…20 %, у зернах злаків – до 70 %.
У складі організму людини і тварин вуглеводи присутні в меншій кількості, ніж білки та ліпіди і становлять приблизно 2 % від маси сухих речовин.
Однак для людини їхнє значення дуже велике. Про це свідчать різноманітні функції, які виконують вуглеводи.
Енергетична функція. Вуглеводи на 60 % забезпечують організм енергією. При окиснюванні 1 г вуглеводів виділяється близько 4 ккал енергії.
Пластична функція. Вуглеводи беруть участь у синтезі багатьох речовин, необхідних для життєдіяльності організму, таких, як нуклеопротеїlи, липоїди, складні ферменти, мукополісахариди та ін.
Функція поживних речовин. Вуглеводи мають здатність відкладатися в організмі у вигляді глікогену – запасного вуглеводу, що витрачається в міру необхідності. Глікоген, в основному, зосереджений у печінці і м'язах. При повноцінному харчуванні в печінці може накопичуватися до 10 % глікогену від маси печінки, у м'язах – до 2 %. При голодуванні запаси глікогену знижуються до 0,2 %.
Захисна функція. Густі секрети (слизи), виділювані різними залозами, багаті на мукополісахариди. Вони охороняють стінки порожніх органів від механічних ушкоджень, а також від проникнення патогенних бактерій і вірусів.
Регуляторна функція. Представник вуглеводів – клітковина має грубу структуру. Потрапляючи з їжею в шлунково-кишковий тракт, вона викликає механічне роздратування стінок шлунка і кишечнику, підвищує їхню активність і сприяє спорожнюванню.
Специфічна функція. Окремі представники вуглеводів виконують особливі функції в організмі, наприклад, беруть участь у проведенні нервових імпульсів, утворенні антитіл, забезпеченні специфічності груп крові, нормальної діяльності центральної нервової системи.
За сучасною класифікацією вуглеводи підрозділяються на три основні групи залежно від їхнього складу, структури й властивостей: моносахариди, олігосахариди і полісахариди.
Моносахариди. Вуглеводи цієї групи мають карбонільну групу (альдегідну або кетонну). Вони є похідними багатоатомних спиртів і мають склад CnН2nOn.
Моносахариди відрізняються різним характером будови і просторовим розташуванням функціональних груп. За характером останніх вони підрозділяються на альдози і кетози.
Моносахариди можуть існувати у двох формах: лінійній (ациклічній) з відкритим карбогеновим ланцюгом і циклічній (кільцевій). Обидві форми перебувають у динамічній рівновазі.
Сполуки, що діють на напівацетальний гідроксил моносахариду, називається агліконом, а продукт реакції – глікозидом. Глікозиди – фізіологічно активні речовини, a- і b-ізомерам моносахаридів відповідають a- і b-глікозиди.
O-глікозиди утворюються при реакції зі спиртами й фенолами (зв'язок здійснюється через Оксиген); N-глікозиди – глікозидний зв'язок здійснюється через Нітроген з радикалом органічної сполуки, що не є вуглеводом.
Глікозиди відіграють важливу роль в обміні речовин. Вони є продуктами розщеплення нуклеїнових кислот і нуклеопротеїдів (нуклеотиди і нуклеозиди), АТФ, НАД, НАДФ; до них відносяться деякі антибіотики, рослинні пігменти, алкалоїди й ін.
D-глюконова й D-галактонова кислоти утворюються при перетворенні альдегідної групи в положенні С-1 у карбоксильну. Фосфорильована форма D-глюконової кислоти – важливий проміжний продукт вуглеводного обміну. З D-глюкози при окиснюванні шостого карбогенного атома утворюється D-глюкуронова кислота, з D-галактози – D-галактуронова кислота.
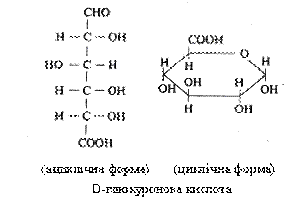
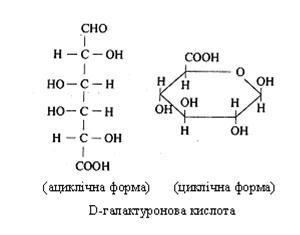
Уронові кислоти – біологічні сполуки, що входять до складу полісахаридів. Так, D-глюкуронова кислота перебуває в складі полісахаридів сполучної тканини, ксиланів, камедів, глюкопротеїдів крові. У вільному стані вона виконує важливу захисну функцію – взаємодіє з токсичними речовинами, що утворюються в товстому кишечнику з амінокислот; при цьому утворюються ефіри, які виділяються з організму із сечею. Аналогічним чином за допомогою глюкуронової кислоти знешкоджуються і виводяться з організму деякі лікарські речовини. Галактуронова кислота входить до складу пектинових речовин та інших полісахаридів. α-Гулуронова і D-мануронова кислоти містяться в полісахариді бурих водоростей – альгіновій кислоті.
Моносахариди легко гідруються за зв'язком С–О, перетворюючись при цьому в багатоатомні спирти. Так, з D-глюкози і D-фруктози утворюється сорбіт, що застосовується в лікувальному харчуванні як замінник цукру.
Важливою властивістю моносахаридів є їхня здатність етерифікуватися під дією фосфорної кислоти. Фосфорні ефіри цукрів беруть активну участь в обміні речовин.
При заміщенні ОН-групи моносахариду NH2-групою утворюється відповідний аміноцукор. Аміноцукри мають властивості амінів, моносахаридів, а також специфічні властивості. Найбільш важливими є D-глюкозамін й D-гaлактозамін.
Аміноцукри входять до складу мукополісахаридів різного походження, вони є також вуглеводними компонентами різних глікопротеїдів і гліколіпідів.
За числом атомів у ланцюзі моносахаридів розрізняють: біози, тріози, тетрози, пентози, гексози та ін. Найбільше значення в організмі людини і тварин мають тріози, пентози і гексози.
В обміні вуглеводів у тканинах беруть участь дві тріози (гліцериновий альдегід і диоксіацетон), що є продуктами окиснювання відповідних первинних і вторинних спиртових груп триатомного спирту гліцерину. Загальна їхня формула С3Н6О3. Тріози утворюються в організмі у вигляді фосфорних ефірів у реакціях гліколізу, спиртового бродіння, а також із гліцерину, що входить до складу ліпідів.
Загальна формула пентоз – С5Н10О5. Вони синтезуються рослинами і входять до складу багатьох сполук організмів тварин. Найбільш важливими є арабіноза, ксилоза, рибоза і дезоксірибоза.
Арабіноза (L і D) міститься в рослинних слизах, пектинових речовинах, геміцелюлозі, гумміарабіці, вишневому клеї та ін.

D-ксилулоза і D-рибулоза утворюються в організмі людини і тварин у пентозофосфатному циклі окиснювання глюкози. Вони беруть участь у біосинтезі нуклеїнових кислот.

D-ксилоза входить до складу рослинних полісахаридів, особливо багато її в деревині, соломі, кукурудзяних качанах, оболонках зерна.
Ця пентоза має солодкий смак, тому її використовують у кондитерській промисловості і при вирощуванні кормових дріжджів. При окиснюванні з неї утворюється ксиланова кислота, а потім триоксіксилолглутарова, використо-вувана в харчовій промисловості як замінник лимонної кислоти. Із ксилози одержують п‘ятиатомний спирт ксиліт, застосовуваний у дієтичному харчуван-ні хворих ожирінням і цукровим діабетом для заміни солодких вуглеводів.
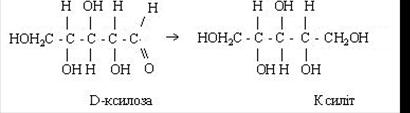
D-рибоза може перебувати в розчинах у циклічній формі:

Рибоза міститься в рибонуклеїнових кислотах, вільних нуклеотидах, деяких коферментах. Фосфорні ефіри рибози утворюються в організмі при окиснюванні глюкози в пентозофосфатному циклі. При відновленні рибози виділяється п‘ятиатомний спирт рибітол, що входить до складу деяких вітамінів (наприклад, вітаміну В2 і коферментів (ФАД).
D-дезоксирибоза є вуглеводним компонентом ДНК і нуклеотидів. Вона може перебувати в ациклічній і циклічній формах.
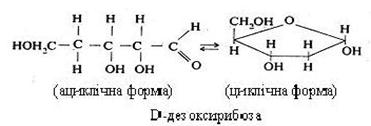
Загальна формула гексоз – С6Н12О6. Вони зустрічаються у вільному стані та в оліго- і полісахаридах. До них відносяться глюкоза, фруктоза, маноза, галактоза.
a-D-глюкоза (декстроза, виноградний цукор) зустрічається в ациклічній і циклічної формах.
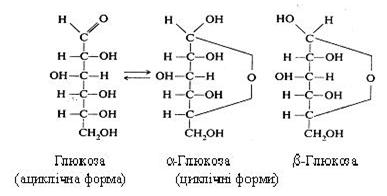
Глюкоза міститься в крові, лімфі, церебральній рідині. Вона широко поширена в продуктах рослинного походження, у великій кількості знаходиться в плодах, насінні, листі і квітах рослин, особливо її багато (17…20 %) у плодах винограду. Глюкоза входить до складу полісахаридів (глікогену, крохмалю, клітковини), дисахаридів (мальтози, сахарози, лактози, целобіози). При окиснюванні первинної спиртової групи із глюкози утворюється глюкуронова кислота, а при відновленні – шестиатомний спирт D-сорбіт. Цю реакцію використовують при промисловому виробництві сорбіту – замінника солодких вуглеводів у харчуванні людей, що страждають на ожиріння та цукровий діабет. Із глюкози одержують також препарати аскорбінової кислоти.
D-фруктоза (левулоза, плодовий цукор) має ациклічну і циклічну форми.

Фруктоза відноситься до солодких вуглеводів: вона в 2,5 рази сладша за глюкозу і в 1,7 рази – за сахарозу. У вільному виді фруктоза зустрічається в плодах, бджолиному меді (45 %); є складовою частиною дисахариду сахарози і полісахариду інуліну.
При нагріванні, дії кислот і лугів фруктоза піддається деструкції з утворенням 5-оксиметилфурфурола. Відновлення фруктози приводить до утворення маніту й сорбіту.
В організмі людини більшу роль грають фосфорні ефіри фруктози, що є проміжними продуктами вуглеводного обміну. Фруктозу використовують у харчуванні хворих цукровим діабетом і людей, що страждають на ожиріння.
D-манноза може перебувати в ациклічній і циклічній формах.
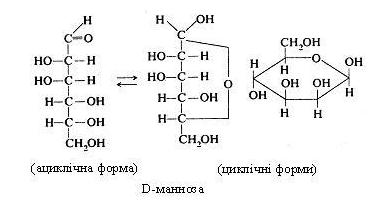
У вільному виді вона рідко зустрічається (наприклад, у шкірці апельсинів) і, звичайно, входить до складу складних вуглеводів – мананів. В організмі людини і тварин міститься в сироватці крові, слині, слизу кишечнику, у суглобній рідині.
D-галактоза (цереброза) зустрічається в ациклічній і циклічній формах.
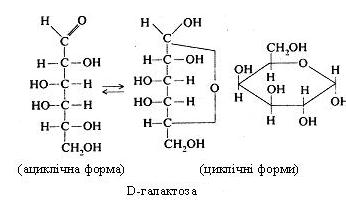
Ця гексоза є складовою частиною дисахариду лактози і трисахариду рафінози.
Галактоза міститься в ліпідах нервової тканини людини і тварин. Вона є фрагментом полісахариду агар-агару, гумміарабіка, галактанів, слизів, глікозидів.
Під дією ферментів галактоза може перетворюватися в глюкозу. Її використовують як поживне середовище для деяких мікроорганізмів, а також у кондитерській промисловості.
Олігосахариди. У складі молекул олігосахаридів перебуває від 2 до 10 залишків моносахаридів, з'єднаних глікозидними зв'язками. У цю групу входять дисахариди, трисахариди і т.п.
Дисахариди – складні цукри, кожна молекула яких при гідролізі розпадається на дві молекули моносахаридів. Емпірична формула С12Н22О11. Серед дисахаридів найбільше значення мають мальтоза, лактоза, сахароза, целобіоза. Поряд з полісахаридами дисахариди є основними вуглеводами в їжі людини і тварин.
Мальтоза – солодовий цукор – містить два залишки a-D-глюкози. Мальтоза утворюється як проміжний продукт при дії амілаз на крохмаль або глікоген. Наявність вільного напівацетального гідроксилу в другому залишку глюкози, що входить до скла-ду мальтози, дозволяє віднести цей дисахарид до цукрів, що відновлюються.
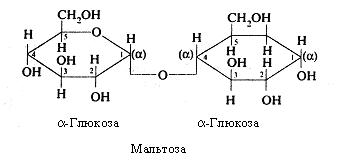
Сахароза – найбільш важливий і широко розповсюджений дисахарид. Сахароза складається з a-D-глюкози і b-D-фруктози. У зв'язку з відсутністю вільного напівацетального гідроксилу цей дисахарид не має редукуючих властивостей.

Сахарози багато в стеблах, коріннях, бульбах і плодах рослин. У цукровому буряку її накопичується до 24 %, у стеблах очерету – до 20 %. Процес розщеплення сахарози на глюкозу й фруктозу називається інверсією цукру, а гідролізована сахароза – інвертним цукром.
Сахароза піддається спиртовому, кисломолочному і маслянокислому бродінню.
Лактоза – молочний цукор – складається з β-галактози і a-глюкози. Вона міститься в молоці та молочних продуктах.

Лактоза добре засвоюється організмом після розщеплення в тонкому кишечнику під дією ферменту лактази (β-галактозидази). При вродженому або придбаному дефіциті цього ферменту виникає нестерпність організмом молока, що проявляється здуттям кишечнику за рахунок підвищеного газоутворення, порушенням функції кишечнику.
Целобіоза – утворюється при ферментативному гідролізі целюлози під дією ферменту, що синтезується мікроорганізмами, β- целюлази.
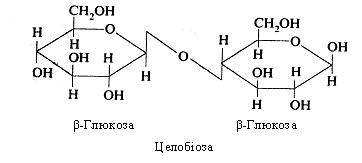
Серед природних трисахаридів найбільше значення має рафіноза, що містить фруктозу, глюкозу і галактозу. У значній кількості вона перебуває в цукровому буряку, насінні бавовни, морських водоростях, грибах і інших рослинах. Рафіноза піддається гідролізу під дією сахарази і галактозидази.
Типовим представником тетрасахаридів є стахіоза, що складається із двох залишків галактози, однієї молекули глюкози і однієї – фруктози. У більших кількостях міститься в цибулинах і коріннях деяких рослин, у насінні бобових.
Полісахариди. Це високомолекулярні вуглеводи, що складаються з великого числа моносахаридів. Вони мають гідрофільні властивості і при розчиненні у воді утворюють колоїдні розчини. Полісахариди підрозділяються на гомо- і гетерополісахариди.
Гомополісахариди. До їхнього складу входять моносахариди одного типу. Наприклад, крохмаль і глікоген побудовані тільки з молекул глюкози, інулін – із фруктози.
Найбільш важливими гомополісахаридами є крохмаль, глікоген, клітковина (целюлоза), що складаються із залишків молекул глюкози, а також пектинові речовини. Із залишків молекул фруктози побудований полісахарид інулін, манани – містять залишки молекул манози, галактани – галактози.
Крохмаль являє собою суміш лінійного полісахариду – амілози (10...30 %) і амілопектину (70…90 %), загальна формула яких – (С6Н10О5)n. Цей полісахарид побудований із залишків глюкози, з'єднаних в амілозі і лінійних ланцюгах амілопектину a-1,4-зв'язками, у точках розгалуження амілопектину –міжлан-цюговими a-1,6-зв'язками. Крохмаль є продуктом фотосинтезу і основною поживною речовиною рослин. Він накопичується у вигляді крохмальних зерен у листі, бульбах, плодах. Великий вміст крохмалю в насін-нях пшениці (75…80 %), значно нижче в рисі (30 %), бульбах картоплі (25%).
Різне відношення фракцій крохмалю до йоду: амілоза дає в реакції з йодом синє забарвлення, амілопектин – фіолетове. Гідролітичне розщеплення крохмалю відбувається поступово, з утворенням проміжних продуктів – декстринів і мальтози, при повному гідролізі виділяється глюкоза.
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 811; Нарушение авторских прав?; Мы поможем в написании вашей работы!