
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Связующие материалы 1 страница
|
|
|
|
КОКС
ГРАФИТ
Графиты применяют в производстве большинства углеграфитовых материалов. Роль, которую они выполняют в технологии этих материалов, различна. При производстве электродов введение графита в массу улучшает ее пластичность, снижает внутреннее трение массы, а также трение о стенки контейнера и мундштука, что обеспечивает получение более плотных изделий. В этом случае вводится небольшое количество графита (4 – 6 %), но даже такое количество влияет на увеличение электропроводности, теплопроводности и термостойкости электродов.
Главным показателем качества промышленных марок графита служат зольность и гранулометрический состав. Эти показатели достаточны только в том случае, если речь идет о графите определенного месторождения и способа изготовления, так как при одинаковом их значении графиты разного происхождения могут сильно отличаться по другим свойствам.
Натуральные графиты содержат примесь минералов, не полностью удаленных при обогащении руд. Этими минералами являются силикаты, кварц и кальцит. Из примесей, вносимых при обогащении графитовых руд, следует назвать флотационные реагенты – главным образом масло, металлическое и окисленное железо, попадающее в графит во время размола в мельницах. Эти примеси заметно влияют на такие свойства графитовых материалов, как электропроводность и способность пластифицировать электродную массу.
Кокс – один из важнейших видов сырья для электродного и электроугольного производства, особенно для графитовых изделий и электроуглей.
Производится два вида малозольных коксов: нефтяные и пековые. Первые получают коксованием нефтяных остатков, вторые – переработкой на кокс каменноугольного пека.
Нефтяные коксы получаются при коксовании различных нефтяных остатков. Свойства нефтяных коксов зависят главным образом от вида исходного сырья. Поэтому нефтяные коксы разделяют по роду нефтяных остатков, из которых они получаются, на две группы: крекинговые и пиролизные. В пределах каждой из этих групп приходится различать еще некоторые разновидности, т.к. пиролиз и крекинг производятся различными способами с применением различной аппаратуры и различном температурном режиме, что в значительной степени влияет на свойства и состав полученных остатков.
Различная микроструктура пиролизного и крекингового коксов существенно влияет на технологические условия производства изделий из этих коксов. Большое количество закрытых микропор в крекинговом коксе осложняет прессование, ведет а образованию в изделиях трещин после снятия нагрузки.
В настоящее время производство нефтяных коксов осуществляется в основном двумя способами: коксование в металлических обогреваемых кубах и замедленное коксование в необогреваемых камерах.
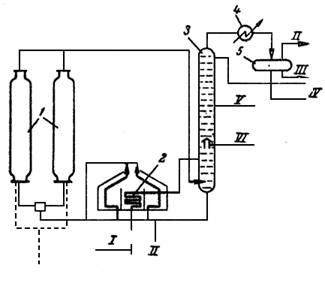
Рис. 2 Принципиальная схема установки замедленного коксования: 1 – коксовые камеры; 2 – нагревательная печь; 3 – ректификационная колонна; 4 – холодильник – конденсатор; 5 – газосепаратор; I – сырье; II – газ; III – вода; IV – бензин; V – легкий газойль; VI – тяжелый газойль; VII – кокс
В настоящее время более широкое применение нашел способ замедленного коксования. Сущность процесса заключается в том, что предварительно нагретое до высокой температуры (500 0С) сырье закачивается в необогреваемые изолированные снаружи реакторы, где производится коксование за счет аккумулированного сырьем тепла.
Первичное сырье после нагрева в печи 2 до 400—405°С смешивается с циркулирующим продуктом в нижней части ректификационной колонны 3, в которой осуществляется выделение газойлевых фракций. Часть их после охлаждения в холодильнике – конденсаторе 4 до 80°С возвращается через сепаратор 5 в колонну в качестве орошения.
В одном блоке по разным схемам устанавливают два или четыре реактора. В нагревательной печи обычно бывает два сырьевых потока. Ректификационные колонны могут быть использованы и для разделения газойля на легкий и тяжелый.
После ректификации смесь исходного сырья при температуре 380-400 °С подается снова в печь для нагрева до 475-510 °С. Нагретое сырье через распределитель, оборудованный четырехходовыми кранами, поступает снизу в один из реакторов.
После заполнения реактора коксом горячий поток сырья переключают в следующий подготовленный реактор. Температура в реакторе 470—480 °С, давление в камерах (избыточное) до 1,7ат. Аппарат рассчитан на заполнение в течение 24 ч. Заполненный коксом аппарат после отключения пропаривают с целью отгона от кокса дистиллятных нефтяных фракций, которые направляются в ректификационную колонну 3.
Затем кокс охлаждают водой и после охлаждения производят выгрузку, осуществляемую гидравлическим методом, т.е. струей воды, вводимой специальными устройствами (резаками) в пробуренную центральную скважину под давлением 150 кг/см2. Кокс вместе с водой попадает в передвижной бункер-дробилку, где дробится до кусков размерами 100—200 мм и падает в приемник. Смесь кокса и воды (1:6) поступает в бункеры, откуда обезвоженный кокс грузят в вагоны или в автомашины.
Кокс замедленного коксования непрочен, образуется большое количество мелких фракций, которое зимой легко смерзаются; при транспортировке кокс сильно измельчается.
В качестве связующих материалов могут применяться материалы, которые в процессе обжига коксуются и, оставляя достаточное количество прочного кокса, придают изделиям необходимую прочность и однородность, а также сообщить связность формуемой массе.
Наилучшими связующими материалами, которые в настоящее время приняты для производства всех видов изделий электродной и электроугольной промышленности, являются продукты, получаемые при коксовании угля в виде пека и смолы.
кристаллический гексагональный графит антрацит смола
Основные модификации углерода
Углерод известен человечеcтву с древнейших времен, прежде всего как уголь и алмаз. Как индивидуальный химический элемент углерод был признан Лавуазье в конце XVIII в. и получил свое название (Carboneum) от латинского carbo - уголь. Ни один элемент Периодической системы Менделеева не обладает тем разнообразием свойств, иногда прямо противоположных, которое присуще углероду. Столь уникальные свойства - причина того, что и чистый углерод, и содержащие его материалы служат объектами фундаментальных исследований и применяются в бесчисленных технических процессах. Все это ярко свидетельствует о его огромной важности для цивилизации. Еще несколько десятилетий назад были известны три основных аллотропных формы углерода: алмаз, графит и карбин. Однако в последнее время были открыты новые модификации углерода, обладающие уникальными свойствами – фуллерены и углеродные нанотрубки.
Каждый атом углерода в структуре алмаза расположен в центре тетраэдра, вершинами которого служат четыре ближайших атома. Соседние атомы связаны между собой ковалентными связями (sp3-гибридизация). Такая структура определяет свойства алмаза как самого твердого вещества, известного на Земле. Графит находит широкое применение в самых разнообразных сферах человеческой деятельности, от изготовления карандашных грифелей до блоков замедления нейтронов в ядерных реакторах. Атомы углерода в кристаллической структуре графита связаны между собой прочными ковалентными связями (sp2- гибридизация) и формируют шестиугольные кольца, образующие, в свою очередь, прочную и стабильную сетку, похожую на пчелиные соты. Сетки располагаются друг над другом слоями. Расстояние между атомами, расположенными в вершинах правильных шестиугольников, равно 0,142 нм., между слоями – 0,335 нм. Слои слабо связаны между собой. Такая структура - прочные слои углерода, слабо связанные между собой, определяет специфические свойства графита: низкую твёрдость и способность легко расслаиваться на мельчайшие чешуйки. В карбине наблюдается линейное расположение атомов, в виде цепочек. Он подразделяется на две модификации: с кумулированными связями =С=С=С= и полииновыми -С≡С-С≡С- связями. Известны и другие формы углерода, такие как аморфный углерод, белый углерод (чаоит) и т.д. Но все эти формы являются композитами, то есть смесью малых фрагментов графита и алмаза. Ниже представлена диаграмма состояния углерода, в которой выделяются алмаз (1), карбин (2), жидкость (3), графит (4), пар (5):
Алмаз и графит, известные человечеству с давних времен, нашли широкое практическое применение задолго до расшифровки их структуры, которая была окончательно установлена только после разработки соответствующих физико-химических методов анализа (рентгенографии, электронографии и т.п.). В отношении карбина и фуллеренов картина обратная: их структуры установлены, а области применения могут пока только планироваться на основании возможных технологических свойств.
Материалы на основе графита
Графит, если рассматривать его идеализированную структуру, представляет собой непрерывный ряд слоев, параллельных основной плоскости и состоящих из гексагонально связанных друг с другом атомов углерода (рис. 1). По взаимному смещению этих слоев в плоскости различают гексагональную и ромбоэдрическую формы. В гексагональной форме слои чередуются по схеме А-В-А-В-..., а в ромбоэдрической по схеме А-В-С-А-В-С-... Содержание ромбоэдрической формы может достигать в природных графитах 30 %, в искусственных она практически не встречается. Расстояние между любыми соседними атомами углерода в плоскости слоя равно 0,142 нм, между соседними слоями 0,335 нм. Каждый атом в слое связан с тремя соседними, и углы между связями составляют 120°. В связях участвуют три валентных электрона из четырех, оставшиеся электроны образуют общее электронное облако, аналогичное имеющемуся у металлов. Такое строение приводит к анизотропии физических свойств графита в направлениях параллельном и перпендикулярном слоям. Графит - вещество темно-серого цвета с металлическим блеском. Это один из самых мягких минералов. Описанная структура характерна для монокристалла графита. Реальные тела состоят из множества областей упорядоченности углеродных атомов, имеющих конечные размеры, отличающиеся на несколько порядков для различных образцов углеродистых тел графитовой или графитоподобной структуры. Структура этих областей может приближаться к идеальной решетке графита или отличаться от нее за счет искажений как внутри слоев, так и за счет неправильностей их чередования. Такие области упорядоченности называются кристаллитами и имеют собственные геометрические характеристики: La - средний диаметр, Lc - средняя высота кристаллита и d002 - среднее расстояние между слоями в кристаллите. Эти величины определяются с помощью рентгенографического анализа. Кроме того, в реальных графитовых телах имеется некоторое количество неупорядоченных атомов (аморфный углерод), занимающих пространство между кристаллитами или внедренных между слоями. Эти атомы могут находиться в sp, sp2 или sp3-гибридном состоянии.
Материал, состоящий главным образом из атомов углерода, может быть получен разными путями. Все они связаны с высокотемпературной обработкой различных углеродсодержащих веществ как в конденсированной, так и в газовой фазах. Из газовой фазы возможно получение сажи, фуллеренов, пироуглерода (пирографита), алмазов. Сажа и фуллерены получаются в результате процессов, протекающих в реакционном объеме. Пироуглерод и алмазы образуются при отложении атомов углерода на твердой подложке. В зависимости от происхождения различают три основных вида графита с почти идеальной структурой: природный графит; графит, кристаллизующийся в процессе выплавки чугуна (спелевый, или киш-графит, доменный графит); синтетический графит, образующийся при дегидрогенизации и полимеризации углеродов из конденсированной или газовой фазы.
Среди материалов, построенных из атомов углерода, особое место занимает так называемый активный углерод. Его можно представить как конструкцию, построенную из слоев атомов углерода, образующих структуру, подобную графиту. Отличие от графита обусловлено различной степенью внутри- и межслоевой разупорядоченности атомов. Благодаря такой конструкции активный углерод имеет так называемое пористое пространство, объем и размер пор которого определяются размером первичных кристаллитов, характером их упаковки и взаимной ориентацией. В связи с этим другим часто встречающимся в литературе названием активного углерода является название "пористый углеродный материал" (ПУМ).
Поры различают по размерам на микропоры (<2 нм), мезопоры (2-50 нм) и макропоры (>50 нм). Благодаря наличию пор ПУМ имеют развитую поверхность и способны адсорбировать жидкости и газы. Способность ПУМ к адсорбции определяется строением поверхности и природой и концентрацией поверхностных реакционноспособных групп (обычно кислородсодержащие группы, образующиеся в результате окисления поверхности).
В настоящее время ПУМ представляют собой важнейший класс адсорбентов, катализаторов и носителей, промышленное производство которых приближается к миллиону тонн. Традиционной схемой получения ПУМ является высокотемпературный пиролиз (карбонизация) твердого углеродсодержащего сырья (древесина, природные угли, полимерные материалы) с последующей обработкой продукта карбонизации парами воды, двуокисью углерода и другими веществами, окисляющими углерод (стадия активации).
При своей достаточной простоте и дешевизне, этот способ имеет 2 основных недостатка: углеродные кластеры и кристаллиты образуются в результате твердофазных плохо контролируемых превращений исходного углеродсодержащего сырья, минеральные примеси, содержащиеся в исходном сырье, переходят в состав конечного углеродного материала.
Этих недостатков лишен 2 метод получения ПУМ – способ каталитического разложения газообразных углеводородов. Этот способ принципиально отличается от первого. Так, в традиционном синтезе идет карбонизация твердого образца, сопровождающаяся удалением части углерода, поэтому с течением синтеза пористость возрастает. Во втором же случае идет рост углеродного каркаса, поэтому с течением времени поры уменьшаются или даже полностью зарастают.
Из-за более высокой молекулярной "однородности" газообразного углеводородного сырья и гораздо меньшего содержания в нем неуглеродсодержащих примесей ПУМ, полученные по второй схеме, отличаются гораздо более низким содержанием минеральных примесей, более высокой однородностью, узким распределением характеристик текстуры. В целом они обладают повышенной механической прочностью и химической стойкостью в агрессивных средах. Благодаря этим положительным свойствам ПУМ, полученные по каталитическому методу рассматриваются как чрезвычайно перспективные сорбенты и носители для современных адсорбционно-каталитических технологий.
Ключевым моментом в формировании твердой углеродной фазы является образование плоских полиароматических молекул. Эти молекулы рассматриваются как первичные структурные элементы большинства ПУМ. В литературе для их обозначения используются разные названия, чаще всего их называют графенами. Атомы углерода на периферии графенов ненасыщенны, обладают повышенной химической активностью и для компенсации свободной валентности могут связываться с фрагментами СН2, СН и др. Такие фрагменты могут приводить к образованию углеродных мостиков между торцами соседних графенов, приводя их к химической "сшивке" под разными углами. В то же время плоская форма графенов способствует их самопроизвольной ориентированной агрегации в плотноупакованные пачки (рис. 4), которые обычно называются графеновыми кластерами. При этом с точки зрения термодинамики наиболее выгодным является плоская упаковка графенов.
Хаотическое "сращивание" графеновых кластеров в ассоциаты, происходящее в газовой фазе, приводит к образованию сфероидальных частиц аморфного углерода (различного типа саж). В таких ассоциатах графеновые кластеры связаны друг с другом многочисленными связями, но при очень высоких температурах (-3000 К) имеют достаточную подвижность, чтобы из разупорядоченной ориентации относительно друг друга (возникшей при их хаотическом "слипании" и "сшивке" в газовой фазе) перейти в более термодинамически выгодную упорядоченную ориентацию, при которой ассоциат графеновых кластеров превращается в микрокристаллит графита.
Государственный стандарт требует называть cажу "углерод технический", однако, как правило, этот термин применяется только в технической литературе и документации. В научной литературе чаще используется термин "сажа". Частица сажи представляет собой набор отдельных кристаллитов, состоящих обычно из 3-5 параллельных слоев гексагонов. Структура кристаллитов сажи отличается от графитовой тем, что параллельные слои в ней смещены друг относительно друга не регулярно, как в графите, а хаотически, придавая кристаллитам не упорядоченную трехмерно структуру. Такая кристаллическая решетка называется двухмерно упорядоченной или турбостратной, в которой слои развернуты вокруг вертикальной оси на некоторый угол.
Атомы углерода, находящиеся на краях плоскостей кристаллических решеток, имеют свободные валентности. По этим валентностям к ним присоединяются атомы отдельных плоских решеток углерода (одиночные слои, не входящие в кристаллит) и цепи атомов углерода, не ориентированные в кристаллическую систему. Эти цепи заполняют промежутки между кристаллитами, цементируя их в одно целое. Кроме того, к свободным валентностям атомов углерода присоединяются атомы Н, О и S. Форма частиц сажи обычно близка к шарообразной, причем поверхность их может быть как гладкой, так и шероховатой. Кристаллиты, расположенные в глубине сажевой частицы, ориентированы беспорядочно друг относительно друга, а находящиеся вблизи поверхности формируют сферическую оболочку.
Сажевые частицы объединяются в сажевые структуры, которые представляют собой более или менее разветвленные цепочки. Различают два вида структур сажи: первичные, очень прочные, связанные валентными связями, и вторичные, связанные сорбционными силами. Величина частиц сажи, а также удельная поверхность и степень структурности (разветвленность сажевых цепочек) зависят от условий их образования. Свойства сажи определяются главным образом этими характеристиками. Сажа является полидисперсным веществом: в образце сажи одного и того же вида имеются частицы различной величины. От степени дисперсности зависят многие свойства саж, в частности, удельная поверхность и цвет. Чем выше дисперсность саж, тем она имеет более черный цвет и бульшую удельную поверхность. Сажа с более высокой структурностью имеет более высокую электропроводность и меньшую кажущуюся плотность, чем сажа, не имеющая сложных структур.
Получение сажи основано на разложении углеводородов под действием высокой температуры. Образование сажи может происходить в пламени горящего сырья при ограниченном доступе воздуха, а также при термическом разложении сырья в отсутствие воздуха. Углерод при этом выделяется в виде твердой фазы. Реакция является эндотермической, поэтому в процесс необходимо вносить тепло сжиганием либо части сырья, либо газообразного или жидкого топлива. Основное количество углеводородов разлагается с образованием сажи в реакционном объеме при температуре выше 1000°С. Скорость термического разложения углеводородов зависит от температуры процесса. Чем она выше, тем большее количество сажевых частиц будет сформировано за данный промежуток времени и, соответственно, меньше их диаметр при ограниченном количестве сырья. Следовательно, более дисперсная сажа будет получаться при более высокой температуре. Рост сажевых частиц может быть предотвращен также за счет снижения концентрации разлагаемого углеводорода и времени пребывания частиц в реакционной зоне.
Анизотропия различных графитов характеризуется отношением коэффициентов расширения образца в параллельном и перпендикулярном слоям направлениях. Это отношение меняется для различных графитов от 1 до 30. При атмосферном давлении и высоких температурах графит сублимирует, не переходя в жидкое состояние, но в области высоких давлений и температур он плавится, что было установлено по скачку электросопротивления примерно при Т=4000К и р=10МПа. Точка равновесия графит-алмаз-расплав находится в области Т=4000-4200К и р=12,5-13,5ГПа.
Пластическая деформация кристаллитов в ряде случаев сопровождается появлением видимых линий сдвигов и следов скольжения. Деформация осуществляется в определенных направлениях, а именно в плоскостях и направлениях с наименьшим сопротивлением сдвигу, то есть по плоскостям, образованным гексагонально связанными атомами углерода, в направлении параллельном этим плоскостям. Особенности кристаллической структуры графита и малая величина сил связи между его слоями обусловливают скольжение слоев относительно друг друга даже при малых значениях напряжений сдвига в направлении скольжения. Это позволяет использовать многие углеграфитовые материалы в качестве антифрикционных, работающих без смазки за счет низких сил сцепления между соприкасающимися поверхностями. С другой стороны, отсутствие прочных межслоевых связей в графите облегчает отделение его частиц от трущихся деталей, что приводит к увеличению их износа.
В направлении им перпендикулярном графит ведет себя как полупроводник, проводимость которого определяется положительными дырками. Естественно поэтому, что электропроводность графита в параллельном слоям направлении примерно на два-три порядка превышает проводимость в направлении ему перпендикулярном. В поликристаллических углеродных материалах общая проводимость определяется двумя составляющими: электропроводностью кристаллитов, металлической по своему типу, и проводимостью аморфного углерода - полупроводника. Этим обусловлена экстремальная зависимость электропроводности многих углеграфитовых материалов от температуры: электросопротивление полупроводника с ростом температуры падает, а металла растет. Поэтому существует минимум температурной зависимости сопротивления, причем его положение смещается в область более низких температур при совершенствовании кристаллической структуры образца. Таким образом, по положению экстремума можно судить о степени приближения структуры к идеальной графитовой.
В настоящее время синтезировано большое число СВГ, которые интенсивно исследуются. СВГ делятся на два широких класса: донорные и акцепторые. Перераспределение электронной плотности между молекулами интеркалята и атомами углерода в СВГ акцепторного типа приводит к появлению дополнительного количества делокализованных дырок в графитовых слоях. В донорных соединениях внедренные вещества отдают свои валентные электроны, и проводимость осуществляется избыточными электронами в углеродных слоях. Акцепторные соединения образуются при внедрении таких веществ, как галогены, галогениды металлов, кислоты. Донорные соединения образуются при внедрении щелочных или щелочноземельных металлов в графитовую матрицу. Примерами соединений донорного типа являются С4К, C8Li, C8Ca и другие. Акцепторые соединения имеют более сложный состав, например C16Br2, C20FeCl3, C16ICl, C+24HSO4-2H2SO4 и другие.
Кроме того, известны СВГ, в которых межслоевые пространства попеременно заняты двумя интеркалирующими агентами. Это так называемые гетеросоединения, типичным примером которых является СВГ с СuС12 и ICl. Они еще более расширяют возможности получения новых материалов с уникальным набором физико-химических характеристик. При интеркалировании всегда происходит значительное (в 2—3 раза) увеличение расстояния между графитовыми слоями и может нарушиться порядок чередования слоев, характерный для монокристаллического графита. Отличительной особенностью СВГ является наличие целого спектра соединений одного и того же интеркалята, различающихся составом и строением. Они называются ступенями. Номер ступени N равен числу графитовых сеток между ближайшими слоями внедренного вещества (рис. 8). Наиболее полно описан синтез интеркалята азотной кислоты. Процесс внедрения HNO3 в графит можно представить в следующем виде:
HNO3газ -> HNO3адс граф
2HNO3адс -> H2O + NO3- + NO2+адс
NO2+адс + С -> NO2адс + С+
NO2адс -> NO2газ
nC+ + NO3- + xHNO3 -> Cn+NO3-xHNO3
Как можно видеть, протекание реакций внедрения HNO3 в графит обусловлено образующимися в системе ионами нитрония NO2, которые выступают в роли окислителя графитовой матрицы, а в межслоевые пространства макрокатиона графита внедряются нитрат-ионы NO3- и молекулы HNO3.
Практически эксперимент достаточно прост: к чешуйчатому графиту добавляется азотная кислота, в течение 10-600 минут производится перемешивание и периодическое удаление NO2. При этом в зависимости от концентрации азотной кислоты, от отношения количества графита к количеству кислоты и от времени синтеза образуются соединения различных ступеней. (табл. 1,2) Нужно сказать, что условия синтеза для получения интеркалята нужной ступени подбираются экспериментально. Интеркаляты графита обнаруживают типично металлические свойства, обладают высокой электропроводностью, а некоторые из них являются сверхпроводниками. При этом монокристаллы обнаруживают анизотропию электропроводности (если в графите отношение проводимостей вдоль и перпендикулярно слоям составляет ~ 104, то в СВГ - ~105 – 106).
Своеобразие физических и химических свойств этих веществ позволяет найти им широкое практическое применение (СВГ используются для производства инфракрасных поляризаторов, монохроматоров для низкоэнергетических нейтронов, оптических фильтров, настраиваемых на определенную длину волны, электрохимических устройств в оптических дисплеях, систем теплозащиты). Помимо прочего, СВГ (в особенности, нитраты и сульфаты) используются для получения пенографита.
Соединения интеркалирования графита неустойчивы на воздухе и постепенно превращаются в так называемые остаточные соединения. Концентрация интеркаланта в таких соединениях очень низка и зависит от температуры десорбции. Если СВГ подвергнуть быстрому нагреванию (термоудару), то испарение, а также разложение интеркаланта приводит к сильному «разбуханию» частиц графита. Этот эффект наблюдается для СВГ с разнообразными интеркалантами — кислотами, хлоридами металлов, галогенами, однако наиболее сильно он выражен для солей графита с анионами минеральных кислот, молекулы которых легко образуют газо- и парообразные продукты. Условия и продукты превращения СИГ таковы: (рис. 10)
Пенографит (ПГ) является хорошо изученным материалом применяемым в промышленности и технике. Получают его очень быстрым нагреванием (термоудар) соединений внедрения в графит (СВГ) различной природы. В массовом промышленном производстве используются соединения внедрения с серной и азотной кислотами, которые получают химическим или электрохимическим окислением порошка природного графита. После термоудара образуется продукт, состоящий из червеобразных частиц углерода, своеобразный “черный снег” Одним из важнейших свойств данного продукта, является способность прессоваться без связующего, что позволяет изготовлять на его основе графитовые материалы различной плотности: от низкоплотных препрегов, до высокоплотных фольг. Оба типа материалов имеют ряд действительных и потенциальных применений: уплотнители, сорбенты, экранирующие электромагнитные волны материалы, термоизоляторы и т.д.
Как и другие слоистые вещества, например вермикулит, некоторые халькогениды переходных металлов, графит обладает способностью к вспенивению. Для этого в его межслоевом пространстве должно содержаться какое либо внедренное вещество, поэтому корректнее говорить о способности к вспениванию соединений внедрения в графит. Нагревание СВГ приводит к закипанию вещества в межслоевом пространстве и его испарению. Испарение происходит в ограниченном размерами образца объеме, давление в межслоевом пространстве в какой-то момент превышает критическое и образец “взрывается” как перегретый паровой котел. В силу слоистой структуры расширение образца происходит вдоль оси “c”, поэтому частицы ПГ имеют червеобразную форму.
Процесс вспенивания часто характеризуется коэффициентом термовспенивания, который принимается как отношение плотности исходного графита к плотности пенографита. Коэффициент термовспенивания увеличивается с ростом температуры и при некотором её значении выходит на насыщение (для СВГ с серной кислотой температура насыщения ~1100°С). Степень вспенивания увеличивается с понижением номера ступени. исходного СВГ. Существует термодинамическая модель вспенивания, согласно которой существует некая критическая температура ниже которой вспенивание не наблюдается при любой скорости нагрева, выше данной температуры интеркалат в СВГ становится нестабильным по сравнению с чистым интеркалатом. Установлено, что критические температуры термического вспенивания уменьшаются с понижением номера ступени и максимальный эффект термического вспенивания достигается при высоких температурах.
Все СВГ обладают способностью к вспениванию, однако вследствие низкой цены и эффективности производства в промышленности ПГ в основном получают на основе СВГ с серной кислотой, так называемого бисульфата графита. Также используют СВГ с азотной кислотой, коинтеркалированные СВГ с серной и уксусной кислотами. На рисунке 1 представлены основные стадии получения графитовых материалов. На первой стадии происходит окисление графитовой матрицы сильным окислителем, например концентрированной азотной, хромовой кислотой, перманганатом калия, электрическим током.
|
|
|
|
|
Дата добавления: 2014-11-18; Просмотров: 1950; Нарушение авторских прав?; Мы поможем в написании вашей работы!