
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Технологічні основи отримання порошків металів електролізом розплавлених середовищ
|
|
|
|
Із технологічного погляду процес отримання металів електролізом розплавлених середовищ можна розділити на чотири етапи:
– безпосередньо електроліз;
– попереднє відокремлення отриманого порошку від застигнутого електроліту;
– вакуумне рафінування отриманого продукту;
– розмелювання та розсіювання.
Для електролізу можна використовувати електролізери двох типів. Так для отримання порошку танталу використовують електролізер, схему якого показано на рис. 5.12. Такий електролізер має катод у вигляді тигля, виготовленого зі сталі або сплаву ніхрому. Як анод застосовують полий перфорований графітовий стрижень, у який завантажують джерело металу (табл. 5.7) – прості та складні комплексні солі, оксиди, сполуки у вигляді кусків розмірами 5...20 мм, гранул або брикетів. Порошок, який виділяється в процесі електролізу, осідає на дні та стінках тигля-катода. Процес провадять до заповнення тигля на 2/3 його об’єму. Потім процес електролізу зупиняють, виймають анод, а розплав охолоджують разом з тиглем. Закристалізований розплав солей з вкрапленими в нього частинками порошку підлягає подальшій переробці.
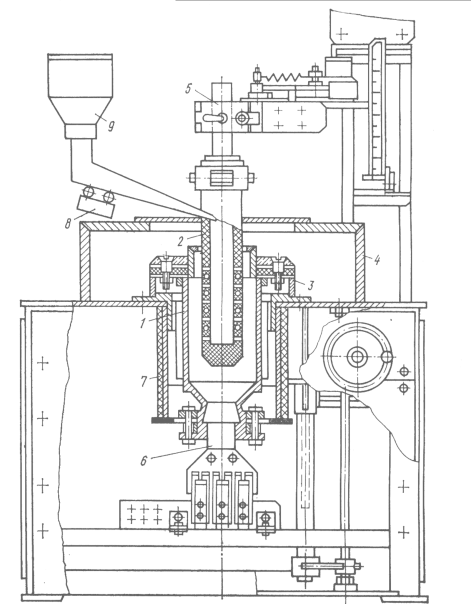
Рис. 5.12 Схема електролізера з трубчастим графітовим анодом:
1 – тигель-катод; 2 – трубчастий перфорований графітовий анод;
3 – теплоізоляційний кожух; 4 – кришка; 5 – кронштейн для закріплення анода; 6 – нижній струмопідвід; 7 – теплоізоляційний стакан;
8 – електромагнітний вібратор; 9 – завантажувальний бункер
Інший варіант електролізу процес з використанням електролізерів, у яких анодом слугує графітовий тигель, а катод виготовляють зі сталі або нікелю (рис. 5.13). Для отримання порошків у таких електролізерах вихідну сировину, наприклад двооксид титану, засипають безпосередньо в електроліт, основу якого складає CaCl2. У процесі електролізу на металевому катоді разом з електролітом створюється катодна «груша». У міру накопичення катодної «груші» її виймають з електролізера і охолоджують в соляній ванні.
У процесі електролізу розплавлених соляних середовищ для підтримання заданих умов коригують склад електроліту, добавляючи в нього матеріал – джерело основного металу.
Отриманий електролізний продукт у вигляді закристалізованих солей-розчинників із вкрапленими частинками порошку розміром 50...70 мкм, наприклад танталу, розмелюють в млинах, які працюють у замкнутому циклі з повітряними сепараторами. Унаслідок цього частина електроліту відділяється і може використовуватись повторно в процесі електролізу. Після розмелювання продукт для більш повного видалення електроліту промивають на концентраційних столах водою. Для зменшення в порошку вмісту домішок металів (заліза, молібдену) та стабілізації поверхні частинок його обробляють гарячим розчином азотної та соляної кислот. Потім порошок промивають водою і сушать у вакуумі.
Можливий інший варіант очищення катодних осадів з використанням вакуумно-термічних установок (рис. 5.14). У них порошок металу відділяють від соляного електроліту його виплавленням у середовищі аргону в спеціальних ретортах, виготовлених з жаростійкого матеріалу. Для цього в реторті (1) розміщують тигель (7) з катодним осадом. Потім реторту вакуумують, заповнюють аргоном і нагрівають до температури 1000 ºС за допомогою електропечі (2), Соляний електроліт плавиться і через гратку в нижній частині тигля стікає в стакан (4). У кінці процесу реторта знову вакуумується для більш повного видалення солей випаровуванням. Унаслідок такого процесу отримують порошок металу у вигляді злегка спечених дендритів, які розмелюють. Таким чином, можна отримувати порошок танталу з умістом основного компонента 99,8…99,9 %.
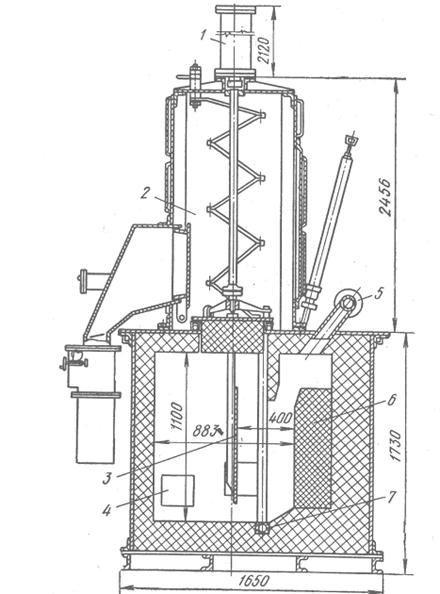
Рис. 5.13 Схема електролізера з графітовим анодом-тиглем:
1 – гідроциліндр; 2 – камера; 3 – катод; 4 – електрод; 5 – газовідвідна трубка;
6 – графітовий анод; 7 – підвід тетрахлориду титану

Рис. 5.14. Схема вакуумно-термічної установки для очищення катодних осадів:
1 – реторта; 2 – електропіч; 3 – конденсатор; 4 – стакан; 5 – дифузійний вакуумний насос; 6 – система завантаження тигля – катода; 7 – тигель–катод
Таблиця 5.7
Умови отримання порошків деяких металів електролізом розплавлених середовищ
| Метал | Склад електроліту, % | Густина струму, кА/м2 | Температура, °С | Вихід за струмом, % | Анод | |
| Джерело металу | Розчинник | |||||
| Титан | TiCl2 (TiCl3) | NaCl, NaCl + KCl, NaCl + KCl + MgCl2 | а к = 5...15 а а = 1...3 | 809...880 | Титановий скрап | |
| Цирконій | K2ZrF6 (25…30) | KCl, NaCl (75…70) | а к= 3,5...4,5 | 750...800 | 88...90 | Графіт |
| Залізо | FeCl2 (11…12) | NaCl + KCl (96…88) | а к = 50 а а = 2...4 | 750...900 | 80...90 | Губчасте залізо |
| Тантал | Ta2O5 (3…3,5) K2TaF7 (25…30) | NaCl + KCl (60…70) | а к = 5 а а = 12...16 | 680...720 | Скрап, сполуки | |
| Ніобій | NbCl2, (Nb) (5…8) | NaCl + KCl + NaF | а к =10... 20 | 680...720 | 88...90 | Скрап, сполуки |
|
|
|
|
|
Дата добавления: 2014-11-20; Просмотров: 567; Нарушение авторских прав?; Мы поможем в написании вашей работы!