
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Радиоактивность. Для того чтобы разобраться в явлении радиоактивности, необходимы знания о строении атома, из которых состоят молекулы веществ
|
|
|
|
Для того чтобы разобраться в явлении радиоактивности, необходимы знания о строении атома, из которых состоят молекулы веществ. Коротко вспомним сведения о структуре атома. Атом представляет собой систему взаимодействующих между собой элементарных частиц - протонов, нейтронов, электронов. Атом состоит из положительно заряженного ядра и оболочки из отрицательно заряженных электронов, которые двигаются на определенных, «разрешенных» орбитах: К (ближайшая к ядру орбита), L, M, N, O, P, Q. Электроны на внутренних орбитах связаны с ядром наиболее прочно, на внешней (валентной) орбите прочность связи наименьшая. Емкость каждой из орбит ограничена; структура орбит и количество электронов на внешней оболочке определяет индивидуальные химические свойства элемента – его валентность, степень окисления и др. Один электрон несет элементарный (единичный) отрицательный электрический заряд, а общий отрицательный заряд электронной оболочки атома равен числу электронов. Носителем элементарного положительного заряда в ядре является протон. В целом атом электронейтрален, т.е. число электронов в оболочке равно числу протонов в ядре атома. В ядре кроме протонов содержатся нейтроны, частицы с массой протона, но не имеющие электрического заряда. Протоны и нейтроны имеют общее название - нуклоны. Число нейтронов в ядре может быть не равным числу протонов. Это не отражается на химических свойствах элемента. Следовательно, в природе существуют разновидности атомов одного элемента, которые имеют одинаковое количество протонов и электронов, но разное число нейтронов. Такие разновидности атомов называются изотопами. Ядра изотопов элементов называют нуклидами. Для конкретного изотопа (нуклида) Х принято следующее обозначение: AX, где А – массовое число (число протонов+нейтронов), Z – зарядовое число, равное числу протонов в ядре = числу электронов (атомный номер элемента в периодической системе Менделеева). Например, изотопы водорода протий, дейтерий и тритий обозначаются, 1H, 2H, 3H. Два изотопа фосфора, стабильный изотоп, 31P и радиоактивный изотоп 32P, имеет по 15 протонов и электронов, число нейтронов определяется по разнице A-Z, т.е. у стабильного изотопа оно составляет 16, у радиоактивного 32P число нейтронов будет равно 17. Термины нуклид и изотоп почти равнозначны, но рекомендуется использовать первый, когда речь идет о разновидностях одного атома, и второй, если это атомы разных химических элементов, например, изотопы водорода 1H, 2H, 3H, радионуклиды 32P, 90Sr, 137Cs. Масса электрона в 2000 раз меньше массы протона или нейтрона, и поэтому суммарная масса атома почти целиком сосредоточена в ядре (на 99, 98 %). Все что касается явления радиоактивности, относится только к атомному ядру.
Радиоактивность - явление самопроизвольного распада ядер радиоактивных атомов с испусканием ионизирующих излучений. В основе радиоактивности лежит способность ядер атомов к самопроизвольным перестройкам своей структуры и даже к расщеплению ядра на отдельные фрагменты. Считается, что нуклоны в ядрах могут взаимодействовать друг с другом и участвовать так называемых ядерных реакциях. Протоны и нейтроны в ядерных реакциях могут превращаться друг в друга, что сопровождается испусканием за пределы атома ряда элементарных частиц: электрона, позитрона, нейтрино, антинейтрино. Кроме элементарных частиц, при ядерных реакциях выделяется большое количество энергии в виде электромагнитного излучения (гамма -излучение, УФ, видимое и инфракрасное излучение). В природе каждый химический элемент существует в виде устойчивых(относительно устойчивы) ядерных структур –стабильных изотопов, и неустойчивых – радиоактивных изотопов. Устойчивость (стабильность) ядра определяется соотношением протонов и нейтронов. У большей части стабильных легких элементов это соотношение составляет 1:1., у элементов с большими массовыми числами оно выше, например, у урана 1:1,6. При недостатке или избытке нейтронов (относительно некого оптимального для этого элемента соотношения) ядра элементов становятся неустойчивыми, что приводит к возможности радиоактивного распада того или иного типа. Например, один из избыточных нейтронов может превратиться в протон с испусканием электрона и антинейтрино. Избыток нейтронов при
радиоактивном распаде снижается и обычно образуется стабильный изотоп нового элемента. Но при распаде некоторых элементов дочерний изотоп тоже оказывается нестабильным и цепочка ядерных превращений может продолжиться до появления нового стабильного химического элемента. Например, при распаде 238U, 232Th имеет место последовательная цепь радиоактивных превращений, включающих несколько радиоактивных изотопов (радиоактивные семейства).
Радиоактивный распад может происходить по нескольким типам: α-распад, β- распад, изомерный переход, внутренняя конверсия, осколочное деление тяжелых ядер.
α-распад- это отщепление от ядра атома фрагмента, состоящего из двух протонов и двух нейтронов. Эту частицу называют α-частицей и по сути она является ядром атома гелия 4Н. Этот тип распад характерен для тяжелых элементов- U, Th, Ra, Rn и др.
β- распад - связан с превращением нейтрона в протон и наоборот. Эти реакции сопровождаются вылетом из ядра электрона, позитрона, нейтрино. β- распад характерен как для легких таки для тяжелых элементов.
Изомерный переход- тип радиоактивного превращения, сопровождающийся только с испусканием γ –излучения. Изомерные переходы могут происходить отдельно или одновременно с другими типами распада как у легких так и у тяжелых атомов.
Внутренняя конверсия. Энергия возбуждения ядра передается орбитальному электрону и сопровождается испусканием атомом характеристического рентгеновского излучения.
Осколочное деление тяжелых ядер. Самые тяжелые ядра с Z ≥ 90 имеют очень большой избыток нейтронов. Так, в ядре 238U на 92 протона приходится 146 нейтронов. Кроме α-распада такие ядра могут самопроизвольно расщепляется на 2 крупных фрагмента, называемых осколками деления с испусканием 2-3 нейтронов. При этом процессе выделяется огромное количество энергии (до 200 МэВ за один распад). Вероятность спонтанного распада природных нуклидов небольшая, например, 1 распад в сутки на 1 кг 238U. Однако, скорость распада можно увеличить на несколько порядков путем облучения ядер нейтронами. Попадание одного нейтрона в «перегруженное» нейтронами ядро приводит к мгновенному делению возбужденного ядра. Некоторые ядра, например, 235U и 239Pu весьма эффективно распадаются на осколки в цепных реакциях деления даже от захватов медленных (тепловых) нейтронов. Расщепление ядер при осколочном делении происходит случайным образом, но чаще всего два образующихся дочерних ядра соотносятся по массе 3: 2.. Первичные осколки деления обычно нестабильны и претерпевают несколько последовательных β- распадов, образуя цепочки вторичных продуктов.
Распад ядер изотопов происходит самопроизвольно, непрерывно и является статистическим процессом. Количество ядер атомов исходного изотопа непрерывно уменьшается, а количество продуктов распада непрерывно накапливается. При радиоактивном распаде проявляется некоторая общая закономерность, которая заключается в том, что количество атомов данного радиоактивного изотопа, распадающихся в единицу времени, всегда составляет определенную, характерную для данного изотопа долю от полного числа еще не распавшихся атомов. Это связано с тем, что вероятность распада отдельного атома за промежуток времени Dt не зависит от условий, в которых находился и находится этот атом, а зависит только от времени. Поэтому число атомов DN, распавшихся за время Dt, пропорционально общему числу не распавшихся атомов. Эта закономерность называют законом радиоактивного распада. Этот закон математически можно выразить так:
-DN = lNDt
где DN - число распавшихся ядер за промежуток времени Dt, N - число не распавшихся ядер, l - величина, пропорциональная вероятности распада одного ядра, называется постоянной распада и является константой, характерной для данного изотопа. Закон радиоактивного распада записывается в виде дифференциальных уравнений
-dN/dt = lNdt/dt = lN [1]
Величина -dN/dt есть абсолютная скорость распада ядер радиоактивного изотопа, называется активностью изотопа (А).
Из уравнения [1] следует, что l = dN/dtN, т.е. l есть уменьшение числа не распавшихся ядер или доля ядер, распадающихся в единицу времени. Постоянная распада имеет размерность с-1. Чем выше l, тем быстрее происходит радиоактивный распад. Величина t = 1/l называется средней продолжительностью жизни атомов данного изотопа. Закон радиоактивного распада можно сформулировать и так: средняя продолжительность жизни атомов есть величина постоянная для данного изотопа. На практике удобно пользоваться интегральной формой этого закона.
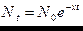
где N0 - число атомов изотопа при t = 0, Nt - число атомов изотопа к моменту времени t.
Для характеристики радиоактивного распада вместо l используют величину, называемую периодом полураспада Т1/2. Период полураспада - это время, в течение которого в среднем распадается половина начального количества радиоактивных ядер.
При регистрации ионизирующих излучений определяют число распадов в единицу времени. Как было отмечено, мера количества радиоактивного вещества, выражаемая числом радиоактивных превращений в единицу времени называется активностью этого вещества и обозначается А.
A = - dN/dt =lN
Единицей измерения активности в системе СИ является 1 распад/с = 1 Беккерель (Бк). Широко используются внесистемная единица измерения активности - Кюри (Ки).
1 Ки = 3,7×1010 Бк. В практической работе применяют производные от Кюри единицы измерения активности: милликюри (1 мКи = 1 ·10 -3 Ки), микрокюри (мкКи = 1 ·10 -6 ), нанокюри (1 нКи = 1· 10 -9 Ки).
|
|
|
|
|
Дата добавления: 2014-11-08; Просмотров: 769; Нарушение авторских прав?; Мы поможем в написании вашей работы!