
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Метод электронного баланса
|
|
|
|
Здесь подсчет числа присоединяемых и теряемых электронов производится на основании значений степеней окисления элементов до и после реакции. Обратимся к простейшему примеру:
Na0 + Cl 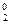 ® Na+ Cl
® Na+ Cl 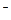


1 Cl2 + 2eˉ ® 2 Cl 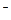 – восстановление
– восстановление
 2 Na + Cl2 = 2Na+ + 2Cl
2 Na + Cl2 = 2Na+ + 2Cl 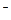
2 Na + Cl2 = 2NaCl
Данный метод используют в том случае, если реакция протекает не в растворе (в газовой фазе, реакции термического разложения и т.д.).
Алгоритм подбора коэффициентов в уравнениях ОВР методом электронного баланса:
1. Записать молекулярную схему реакции.
2. Определить с.о. элементов.
3. Отметить символы элементов, изменивших с.о. в ходе реакции.
4. На основании сравнения с.о. элементов, определить окислитель и продукт восстановления, восстановитель и продукт окисления.
5. Составить электронные уравнения процессов восстановления, окисления, соблюдая при этом баланс по элементам и зарядам.
6. Найти наименьшее общее кратное (НОК) для числа принятых и отданных электронов.
7. Найти основные коэффициенты при каждом электронном уравнении. Для этого полученное в пункте 6 число НОК разделить на число электронов, фигурирующих в данном электронном уравнении.
8. Умножить электронные уравнения на основные коэффициенты, полученные в п.7, и просуммировать их между собой (т.е. получить суммарное электронное уравнение). В суммарном уравнении электроны отсутствуют, т.к. сокращаются.
9. Подставить коэффициенты из суммарного электронного уравнения в молекулярное уравнение. Остальные коэффициенты подбираем в последовательности: соль, кислота или основание, вода.
10. Осуществить проверку числа атомов кислорода в правой и левой частях уравнения.
Примеры:
1. Молекулярная схема реакции:
+3 +2 0 +4
Bi Cl3 + Na2 Sn O2 + NaOH → Bi + NaCl + Na2 Sn O3 +H2O
ок-ль восст-ль продукт продукт
восст-ия ок-ия
Электронные уравнения:
| осн. коэффициенты | НОК | ||
| Bi+3 +3℮ = Bi | процесс восстановления | ||
| Sn+2 - 2℮ = Sn+4 | процесс окисления | ||
| 2 Bi+3 + 3Sn+2 = 2 Bi +3Sn+4 | Суммарная схема электронного баланса |
Молекулярное уравнение реакции:
2BiCl3 + 3Na2SnO2 + 6 NaOH → 2Bi + 6 NaCl + 3Na2SnO3 + 3 H2O
Проверка: O: 12 = 12.
|
|
|
|
|
Дата добавления: 2014-11-20; Просмотров: 644; Нарушение авторских прав?; Мы поможем в написании вашей работы!