
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тепловые двигатели и холодильные машины. Цикл Карно и его к.п.д. для идеального газа
|
|
|
|
Второе начало термодинамики
Первое начало термодинамики, выражая закон сохранения и превращения энергии, не позволяет установить направление протекания термодинамических процессов. Появление второго начала термодинамики связано с необходимостью дать ответ на вопрос, какие процессы в природе возможны,а какие нет. Второе начало термодинамики определяет направление протекания термодинамических процессов.
Используя понятие энтропии и неравенство Клаузиуса ΔS≥0, второе начало термодинамики можно сформулировать как закон возрастания энтропии замкнутой системы при необратимых процессах: любой необратимый процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает.
Формула Больцмана S = k ln W позволяет объяснить постулируемое вторым началом термодинамики возрастание энтропии в замкнутой системе при необратимых процессах: возрастание энтропии означает переход системы из менее вероятных в более вероятные состояния. Таким образом, формула Больцмана позволяет дать статистическое толкование второго начала термодинамики. Оно, являясь статистическим законом, описывает закономерности хаотического движения большого числа частиц, составляющих замкнутую систему.
Укажем еще две формулировки второго начала термодинамики:
1) по Кельвину: невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу;
2) по Клаузиусу: невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому.
Первые два начала термодинамики дают недостаточно сведений о поведении термодинамических систем при нуле Кельвина. Они дополняются третьим началом термодинамики, или теоремой Нернста — Планка: энтропия всех тел в состоянии равновесия стремится к нулю по мере приближения температуры к нулю Кельвина:
S → 0 при Т →0. (8.13)
Из теоремы Нернста — Планка следует, что теплоемкости Ср и СV при 0 К равны нулю.
Из формулировки второго начала термодинамики по Кельвину следует, что вечный двигатель второго вода – периодически действующий двигатель, совершающий работу за счет охлаждения одного источника теплоты, – невозможен.
Для иллюстрации этого положения рассмотрим работу теплового двигателя.
Принцип действия теплового двигателя приведен на рис.8.2.
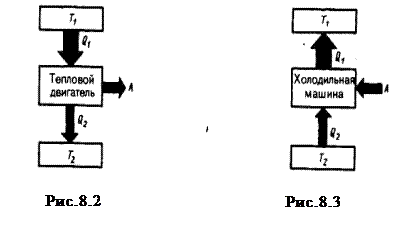
От термостата с более высокой температурой T1 называемого нагревателем, за цикл отнимается количество теплоты Q 1, а термостату с более низкой температурой T 2, называемому холодильником, за цикл передается количество теплоты Q 2, при этом совершается работа
А=Q 1 –Q 2.
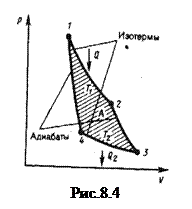
Процесс, обратный происходящему в тепловом двигателе, используется в холодильной машине, принцип действия которой представлен на рис.9.3. Системой за цикл от термостата с более низкой температурой Т 2отнимается количество теплоты Q 2 и отдается термостату с более высокой температурой Т 1 количество теплоты Q 1. Для кругового процесса Q=A, но, по условию, Q=Q 2 -Q 1<0, поэтому А <0 и Q 2 -Q 1 = -А, или Q 1 =Q 2 +A, т. е. количество теплоты Q 1, отданное системой источнику теплоты при более ысокой температуре T 1 больше количества теплоты Q 2, полученного от источника теплоты при более низкой температуре Т2, на величину работы, совершенной над системой. Следовательно, без совершения работы нельзя отбирать теплоту от менее нагретого тела и отдавать ее более нагретому. Это утверждение есть не что иное, как второе начало термодинамики в формулировке Клаузиуса.
Основываясь на втором начале термодинамики, Карно вывел теорему: из всех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей (Т 1) и холодильников (Т 2) наибольшим к. п. д. обладают обратимые машины; при этом к. п. д. обратимых машин, работающих при одинаковых температурах нагревателей (Т 1) и холодильников (Т 2), равны друг другу и не зависят от природы рабочего тела (тела, совершающего круговой процесс и обменивающегося энергией с другими телами), а определяются только температурами нагревателя и холодильника.
Цикл Карно – наиболее экономичный цикл, состоящий из двух изотерм и двух адиабат. Рассмотрим прямой цикл Карно, в котором в качестве рабочего тела используется идеальный газ,заключенный в сосуд с подвижным поршнем.
Цикл Карно изображен на рис. 8.4, где изотермические расширение и сжатие заданы соответственно кривыми 1–2 и 3–4, а адиабатические расширение и сжатие – кривыми 2–3 и 4–1.
 При изотермическом процессе U = const, поэтому количество теплоты Q1 полученное газом от нагревателя, равно работе расширения А 12, совершаемой газом при переходе из состояния 1 в состояние 2:
При изотермическом процессе U = const, поэтому количество теплоты Q1 полученное газом от нагревателя, равно работе расширения А 12, совершаемой газом при переходе из состояния 1 в состояние 2:
A 12 = νRT 1 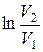 = Q 1 (8.13)
= Q 1 (8.13)
При адиабатическом расширении 2-3 теплообмен с окружающей средой отсутствует и работа расширения A 23 совершается за счет изменения внутренней энергии A 23 =–νCV (T 2 -T 1). Количество теплоты Q 2, отданное газом холодильнику при изотермическом сжатии, равно работе сжатия A 34:
A 34= νRT 2 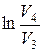 =– Q 2. (8.14)
=– Q 2. (8.14)
Работа адиабатического сжатия
A 41 =–νCV (T 1 –T 2) =–A 23.
Работа, совершаемая в результате кругового процесса,
A=A 12 + A 23 + A 34 + A 41 =Q 1 + A23– Q 2 – A 23 = Q 1 – Q 2
определяется площадью, заштрихованной на рис.8.4.
Термический к. п. д. для цикла Карно равен: η = A/Q 1 = (Q 1 –Q 2) /Q 1.
Применив уравнение Пуассона для адиабат 2–3 и 4–1, получим
T 1 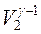 = T 2
= T 2 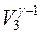 ,
, 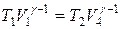 .
.
Откуда
V 2 /V 1 = V 3 /V 4. (8.15)
Подставляя (9.13) и (9.14) в формулу (9.2) и учитывая (9.15), получаем
η = 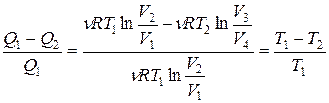 , (8.16)
, (8.16)
т. е. для цикла Карно к. п. д. действительно определяется только температурами нагревателя и холодильника. Для его повышения необходимо увеличивать разность температур нагревателя и холодильника. Например, при Т 1=400 К и Т 2=300 К η =0,25. Если же температуру нагревателя повысить на 100 К, а температуру холодильника понизить на 50 К, то η =0,5. К. п. д. всякого реального теплового двигателя из-за трения и неизбежных тепловых потерь гораздо меньше вычисленного для цикла Карно.
Обратный цикл Карно положен в основу действия тепловых насосов. В отличие от холодильных машин тепловые насосы должны как можно больше тепловой энергии отдавать горячему телу, например системе отопления. Часть этой энергии отбирается от окружающей среды с более низкой температурой, а часть – получается за счет механической работы, производимой, например, компрессором.
Теорема Карно послужила основанием для установления термодинамической шкалы температур. Сравнив левую и правую части формулы (8.16), получим
Τ 2 /T 1 =Q 2 /Q 1,(8.17)
т. е. для сравнения температур T 1 и T 2 двух тел необходимо осуществить обратимый цикл Карно, в котором одно тело используется в качестве нагревателя, а другое – холодильника. Из равенства (8.17) видно, что отношение температур тел равно отношению отданного в этом цикле количества теплоты к полученному.
|
|
|
|
|
Дата добавления: 2014-12-08; Просмотров: 1605; Нарушение авторских прав?; Мы поможем в написании вашей работы!