
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Десульфурация
|
|
|
|
Дефосфорация
Фосфор в углеродистой стали вызывает ее повышенную хрупкость на холоде, хладноломкость или синеломкость, ухудшает механические свойства стали. Допустимое содержание фосфора в стали менее 0,02…0,05%.
Фосфор обладает большим химическим сродством к кислороду, чем железо, и его можно удалять из расплава методом окислительного рафинирования.
Окисление фосфора происходит в два этапа. На первом этапе фосфор окисляется в ванне по уравнению:
2 [ Р ] + 5 [ FeO ] = (Р2O5) + 5 [ Fe ]; ∆ H = - 200,97 кДж/моль.
Образовавшийся оксид фосфора Р2O5 образует с избыточным FeO фазу, имеющую состав, близкий к фосфату железа:
(Р2O5) + 3 (FeO) = (FeO)3· Р2O5; ∆ H = - 128,5 кДж/моль.
Так как реакция экзотермическая, она протекает при относительно низких температурах. При высоких температурах фосфат железа нестабилен и появляется опасность восстановления фосфора и перехода его в ванну. Чтобы предупредить обратную реакцию, необходимо перевести Р2O5 в стабильное соединение, из которого фосфор восстанавливаться не будет.
Второй этап окисления фосфора осуществляется при помощи извести. При этом образуется фосфорно-кальциевая соль по уравнению:
(FeO)3· Р2O5 + 4 СаО = (СаО)4· Р2O5 + 3 FeO; ∆ H = - 546,41 кДж/моль.
Если в шлаке мало СаО, то в первую очередь он будет соединяться с оксидом кремния и его не хватит для связывания фосфора. Считают, что извести в шлаке должно быть по массе в четыре раза больше, чем кремния и фосфора в шихте.
Из кинетических факторов, обеспечивающих успешную дефосфорацию в реальных условиях плавки, большое значение имеет перемешивание шлака, поскольку лимитирующим является процесс диффузии.
Восстановлению фосфора из шлака при высоких температурах могут способствовать элементы, которые при данных условиях имеют большее сродство к кислороду, чем железо, то есть все раскисляющие элементы. В период окончания плавки это главным образом марганец, кремний, алюминий.
Шлак, содержащий фосфор, который извлечен из расплава, перед раскислением удаляют (полностью или частично).
При отвердевании стали в результате избирательной кристаллизации сера, растворенная в расплавленном металле, концентрируется в остающейся жидкости. Обладая очень малой растворимостью в железе, сера выделяется на границах зёрен металла в виде легкоплавких соединений в смеси с оксидами железа. Сталь с повышенным содержанием серы становится красноломкой – хрупкой при температурах горячей обработки (800-1000°С) а в холодном состоянии сталь имеет низкую механическую прочность.
При производстве литейных сплавов сера может находиться в газовой фазе (SO2), в топливе (FeS), в металлическом и шлаковом расплавах. Удалить серу из металла методом окислительного рафинирования невозможно, так как сера обладает меньшим сродством к кислороду, чем железо.
Десульфурация расплавленного металла производится переводом серы в шлак при помощи реагентов, способных давать более прочные и существенно менее растворимые в железе сульфиды, чем FeS, например CaS, MgS, MnS, Na 2 S и др. В качестве такого реагента чаще всего используют оксид кальция CaO.
В плавильных агрегатах процесс сводится к взаимодействию шлака, содержащего CaO, с металлом по реакции
[ FeS ] + (CaO) = (FeО) + (CaS),
которая является частным случаем взаимодействия серы, растворенной в железе, с основными оксидами шлака
[ FeS ] + (МеO) = (FeО) + (МеS).
Константа равновесия
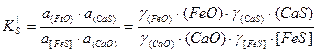 .
.
Концентрации (CaS) и [ FeS ] можно заменить общим содержанием серы в шлаке (S) и расплаве [ S ] с введением коэффициентов активности серы в шлаке γ ( S ) и расплаве γ [ S ], учитывающих в суммарном виде степень связанности серы в соответствующих фазах. Тогда
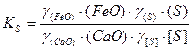 .
.
Коэффициент распределения 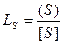 .
.
Эта величина служит для оценки обессеривающей способности шлака.
Из уравнения константы равновесия
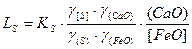 .
.
Отсюда следует, что константа распределения серы LS возрастает с увеличением активности СаО, то есть основности шлака, и со снижением активности FeO, то есть его окислительной способности.
Таким образом, для обессеривания наиболее пригодны основные восстановительные процессы.
В электросталеплавильном процессе после завершения окислительного рафинирования наводят раскислительный шлак с низким содержанием FeO (менее 1%) путём введения восстановителей (C и Si). Это обеспечивает и раскисление и десульфурацию стали.
Обессеривающая способность шлака зависит от его химического состава. Из всех компонентов шлака наиболее существенно влияют на обессеривающую способность оксиды кальция и кремния. CaO ее увеличивает; SiO 2 уменьшает. Поэтому обессеривающую способность шлака оценивают отношением: 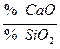 . Чем больше отношение, тем выше константа распределения
. Чем больше отношение, тем выше константа распределения 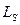 . Температура влияет на
. Температура влияет на 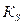 и
и 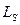 незначительно.
незначительно.
Процесс десульфурации определяется в значительной степени кинетикой взаимодействия. Чем быстрее идёт процесс, тем ближе система к состоянию равновесия и полнее используется обессеривающая способность шлака.
Большое значение имеют интенсивность перемешивания и вязкость шлака. Скорость процесса десульфурации возрастает по мере увеличения интенсивности перемешивания металла и шлака, а также понижения вязкости шлака, что может быть достигнуто повышением температуры и введением разжижающих добавок. Такой эффект связан с тем, что десульфурация расплавов железа протекает в диффузионной области и основным лимитирующим звеном процесса является переход серы из металлического расплава в шлак.
Раскисление
Раскисление - это заключительная технологическая операция плавильного процесса. Она проводится для того, чтобы снизить до минимума содержание кислорода, остающегося в расплаве после окислительного рафинирования. Кислород необходимо перевести в соединения, которые должны быть удалены из расплава.
Критерием раскислительной способности того или иного элемента является активность кислорода в металле, которая находится в равновесии с определенной концентрацией (активностью) элемента раскислителя и с продуктами раскисления, образуемыми раскислителем с кислородом.
При одновременном использовании нескольких раскислителей раскислительная способность каждого из них может увеличваться. Известно, что марганец и кремний взаимно усиливают раскислительную способность друг друга.
При выборе раскислителей необходимо отдавать предпочтение тем элементам, которые образуют оксиды, взаимодействующие между собой с образованием соединений с невысокой температурой плавления, желательно ниже температуры раскисляемого сплава, и плотностью намного меньше плотности сплава.
Требования, предъявляемые к раскислителям:
- при возможно малых концентрациях они должны обладать в условиях раскисления большим сродством к кислороду, чем раскисляемый Ме;
- остающиеся в расплаве раскислители не должны оказывать вредного влияния на свойства сплава;
- оксиды, образованные раскислителем, должны в минимальной степени растворяться в раскисляемом металле;
- нерациональные потери раскислителя должны быть минимальны;
- раскислители должны быть дешевыми и недифицитными.
Для раскисления железоуглеродистых сплавов используют C, Mn, Si, Al, Ti, Ca и др.
Процесс удаления продуктов раскисления связан не только с их природой, но и со многими побочными факторами: глубина ванны, высота ковша и др.
Эффективным средством раскисления сплавов является использование вакуума. В вакууме усиливается раскислительная способность элементов и создаются благоприятные условия для дегазации и удаления неметаллических включений. Но в вакууме возникает опасность взаимодействия жидкого металла с оксидами огнеупорных материалов футеровки.
|
|
|
|
|
Дата добавления: 2014-12-08; Просмотров: 833; Нарушение авторских прав?; Мы поможем в написании вашей работы!