
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Корпускулярные ионизирующие излучения
|
|
|
|
Е) Тормозное излучение высоких энергий
Е) Альфа-частицы
3) Какие из перечисленных видов излучения относятся к фотонным?
а) Пи-мезонное
б) Рентгеновское
в) Электронное
г) Гамма-излучение
д) Протонное
4) Какой термин выражает среднее количество пар ионов, образованных заряженной частицей, на единицу длины пробега?
а) Линейная плотность ионизации (ЛПИ)
б) Линейная передача энергии (ЛПЭ)
в) Средняя длина свободного пробега
Положительно заряженные частицы
a -излучение представляет собой поток ядер гелия, несущих двойной положительный элементарный заряд. Так как масса a-частиц значительна по сравнению с массой электронов атомов, с которыми они соударяются (соотношение примерно 2700:1), траектория a-частиц прямолинейна. Вследствие большого заряда и малой скорости a-частицы весьма интенсивно взаимодействуют с электронами поглощающего материала; быстро расходуя свою энергию. При этом они успевают пройти очень малое расстояние.
Эти частицы производят самое большое ионизирующее действие (3000 – 4000 пар ионов на 1 мкм пути). Альфа-частицы примерно в 100 раз сильнее ионизируют воздух, чем бета – излучение. В ткани человека a-частицы проникают на глубину не более 50 мкм, в воздухе их пробег равен 7-12 см. Это определяет относительно малую радиационную опасность a-частиц при наружном облучении.
Протонные пучки. Как и a-частицы, характеризуются наибольшими массой и зарядом по сравнению с другими видами ИИ. Их траектории также прямолинейны.
Линейная плотность ионизации, создаваемая положительно заряженными частицами, неравномерна вдоль трека частицы, образует в конце пробега так называемый «пик Брегга», т. е. тяжелые частицы в конце пути дают ЛПИ, в сотни раз превышающую ЛПИ в начале пути (рис.1). Наличие пика Брегга и возможность управления его локализацией на глубине создают благоприятные условия для лучевой терапии протонными пучками высоких энергий.
Основными преимуществами использования протонных пучков в лучевой терапии являются формирование нерасходящихся пучков и возможность подведения необходимого количества энергии на заданную глубину, соответствующую пику Брегга. При этом ткани, расположенные за пределами пучка, практически не повреждаются, поэтому можно использовать пучок с различными энергиями и таким образом разрушить весь очаг поражения.
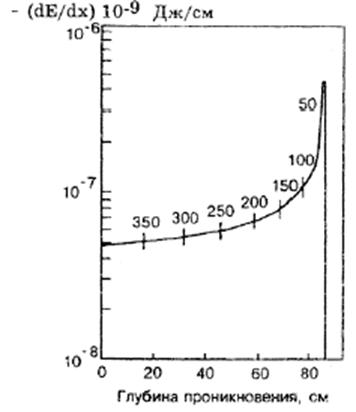
Рис. 2.1. Зависимость ЛПИ протонов с начальной энергией 400 МэВ от глубины проникновения в биологической ткани. В конце пробега находится пик Брегга.
Отрицательно заряженные частицы
b-излучение представляет собой поток электронов и позитронов (β- или β+), возникающий в результате внутриядерных превращений нейтронов и протонов.
При электронном (β-) распаде массовое число элемента не меняется, а заряд ядра увеличивается на единицу. Схема (β-) распада искусственного радионуклида 60Со, который широко используется для наружного и контактного облучения, показана ниже (Рис. 2.2.).
При позитронном (β+) распаде массовое число нового элемента также не меняется но заряд ядра уменьшается на единицу.

Рис. 2.2. Схема (β-) распада радионуклида 60Со.
В отличие от a-частиц, b-частицы характеризуются непрерывным энергетическим спектром. Путь электрона в веществе извилист, поскольку он обладает малой массой и легко изменяет направление вследствие соударения с электронами атомов. Поэтому начальный пучок электронов в тканях имеет тенденцию к расхождению (так называемый, эффект рассеяния электронов). При торможении быстрых электронов в поле ядра атомов возникает тормозное фотонное излучение.
Вследствие большой скорости проникающая способность b-частиц выше, чем у a-частиц. В воздухе она составляет около 10 м, в мышечных тканях - 10 мм. b-активные источники используются при лечении злокачественных опухолей, локализация которых позволяет обеспечить непосредственный контакт с этими препаратами. Избирательное накопление органами и тканями некоторых химических соединений послужило основанием для применения радионуклидов этих элементов с лечебной целью. Например, внутривенное введение раствора 131I (период полураспада 8,06 дня) используют для лечения метастатического рака щитовидной железы.
С помощью современных ускорителей создаются пучки ускоренных электронов высоких энергий (от 4 до 20 МэВ), обладающие относительно большой проникающей способностью. Средняя длина свободного пробега таких электронов может достигать в тканях человеческого организма 10 см. Электронный пучок, поглощаясь в тканях, создает дозное поле, отличающее этот вид излучения от других. Максимум ионизации при этом образуется вблизи поверхности тела. Размеры зоны максимума ионизации находятся в прямой зависимости от величины энергии излучения. За пределами максимума происходит довольно быстрый спад дозы.
Электронный пучок с энергией до 6 МэВ используется при лечении поверхностных злокачественных новообразований, с энергией до 20 МэВ - более глубоко расположенных. Современные ускорители дают возможность плавно регулировать энергию пучка электронов и тем самым создавать требуемую дозу на любой глубине.
p-мезоны - бесспиновые элементарные частицы с массой, величина которой занимает промежуточное место между массами электрона и протона.
Отрицательные p-мезоны при "входе" в вещество в начале пути ведут себя подобно протонам, затем основная часть мезонов останавливается на определенной глубине и со 100%-й вероятностью захватывается атомами (кислородом и азотом тканей), а затем поглощается их ядрами. При этом в ядро вносится очень большая энергия (больше 100 МэВ), в результате чего ядро сильно возбуждается и распадается с испусканием нейтронов, протонов, дейтронов и a-частиц, которые и вызывают сильную ионизацию вещества.
Таким образом, все заряженные частицы в результате их электростатического взаимодействия с электронами облучаемого вещества приводят к непосредственной прямой ионизации его атомов и молекул. Это взаимодействие тем эффективнее, чем выше порядковый номер вещества - поглотителя. Поэтому защитные устройства, экранирующие взаимодействие ИИ на биологические объекты, выполняются из веществ с высоким атомным номером.
Нейтронные излучения
Процессы взаимодействия нейтронов с веществом определяются как энергией нейтронов, так и атомным составом поглощающей среды. Отсутствие у нейтронов электрического заряда позволяет ему проникать через электронные оболочки атомов и свободно приближаться к ядру.
Источники нейтронов:
o бомбардировка дейтерия;
o смеси a-излучателей с бериллием или бором:
§ Не + Ве = 13С ® 12С + n.
При воздействии на ткани нейтроны захватываются ядрами атомов, что приводит к нарушению их структуры и сопровождается испусканием a- или b-частиц и g-квантов. Кроме того, при ядерных превращениях освобождаются ядра отдачи, которые обладают большой энергией, производят высокую ионизацию среды. Их ионизирующая способность близка к ионизирующей способности a-частиц. Однако поражающее действие нейтронов значительно выше вследствие их большой проникающей способности.
При облучении нейтронами в клетке возникает одномоментный разрыв ДНК, что приводит к ее гибели. Так как гибнут не только опухолевые, но и здоровые клетки, для нейтронов характерна высокая частота лучевых повреждений. Из всех видов ИИ быстрые нейтроны обладают наибольшей радиационной опасностью. Быстрые нейтроны лучше замедляются на ядрах легких элементов (вода, парафин, жировая ткань). Следовательно, поглощенная доза оказывается большей в жировой ткани, что приводит к лучевым повреждениям.
В то же время высокая проникающая способность быстрых нейтронов открывает перспективы для их использования в лучевой терапии злокачественных новообразований.
При решении вопросов защиты от нейтронного излучения необходимо учитывать специфику его взаимодействия с веществом. Быстрые нейтроны необходимо их замедлить. Для этого используются легкие среды (вода, парафин). Медленные нейтроны затем поглощаются в результате радиационного захвата в материалах, изготовленных из бора или кадмия. Поскольку процесс захвата сопровождается излучением g-квантов, в качестве защитного материала используют свинцовые барьеры. Таким образом, для защиты от нейтронов используются довольно сложные конструкции.
Нейтронозахватная терапия. Впервые метод предложен Locher в 1936 г. При этом методе используется поток медленных нейтронов, получаемых от ядерных реакторов. Для дифференцированного облучения с максимальным эффектом в опухоли и минимальным в нормальных тканях необходимо насыщение опухоли элементами, характеризующимися большим поперечным сечением захвата медленных нейтронов.
Такими элементами являются бор (10В) и литий (6Li). Однако туморотропностью эти элементы не обладают. Для обогащения ими опухоли использована различная скорость диффузии их из кровеносной системы в ткани (т. е. эти элементы медленно переходят из крови в головной мозг, а в опухолевую ткань поступают значительно быстрее).
Установлено, что через 30 минут после внутривенного введения соединений бора его концентрация в опухоли мозга в 4-5 раз выше, чем в нормальной ткани. И именно в это время должно проводиться облучение.
Концентрация бора и лития в мышечной ткани очень велика, и поэтому нейтронозахватывающую терапию нельзя применять при опухолях туловища и конечностей. Этот метод применим только при опухолях головного мозга.
|
|
|
|
|
Дата добавления: 2014-12-16; Просмотров: 1597; Нарушение авторских прав?; Мы поможем в написании вашей работы!