
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Изменение скорости реакции во времени
|
|
|
|
Число прореагировавших молей в единице объема за время 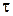 обозначим сB. Тогда, в соответствии с законом действующих масс, для рассматриваемо-
обозначим сB. Тогда, в соответствии с законом действующих масс, для рассматриваемо-
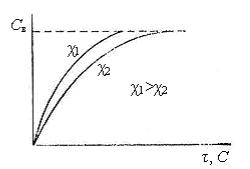
Рис. 5. Зависимость скорости реакции от порядка реакции
го момента времени скорость реакции можно записать в виде
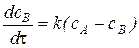 , (79)
, (79)
где сА — начальная концентрация реагирующего вещества. Решение уравнения (79) при постоянной температуре имеет вид
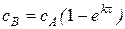 . (80)
. (80)
Графическая иллюстрация зависимости (80) приведена на рис. 5. Экспоненциальный закон расходования исходного вещества показывает, что в начальный момент количество продуктов реакции (или расхода исходного вещества) увеличивается, затем этот процесс замедляется. С повышением порядка реакции 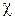 скорость реакции падает.
скорость реакции падает.
Организация процесса горения предусматривает обеспечение многих факторов. Например:
- к горючему необходим подвод окислителя;
- составы горючего и окислителя должны соответствовать условиям воспламенения;
- необходимо обеспечить воспламенение топливоокислительной смеси;
- необходимо создать условия для стабилизации воспламенения и горения.
Удовлетворение этих условий зависит от протекания кинетических и диффузионных процессов. Рассмотрим некоторые из них.
В соответствии с современным представлением, основанном на работах Н. Н. Семенова, горение протекает по цепному принципу. В процессе цепной реакции на начальном этапе образуются промежуточные продукты (радикалы, свободные атомы), обладающие повышенной реакционной активностью. Последние вступают в химические взаимодействия между собой и исходными реагентами, в результате появляются конечные продукты и одновременно регенерируются активные промежуточные продукты, количество которых с течением времени при определенных условиях увеличивается. Скорость такого цепного процесса лавинообразно возрастает (цепной взрыв).
Начальный процесс образования активных продуктов из исходных веществ называется зарождением цепи. Этот процесс идет с поглощением энергии, т. е. является эндотермическим, так как для разрыва внутримолекулярных связей необходима энергия.
Разветвление цепи происходит в результате реагирования одной молекулы активного вещества с исходным веществом, вследствие чего образуются две или несколько молекул активного продукта.
Под обрывом цепи понимается процесс, при котором активный продукт исчезает. Если скорость разветвления больше скорости обрыва, то происходит развитие цепной реакции, если скорость обрыва больше скорости разветвления, то реакция не происходит. К обрыву цепи может привести столкновение активных центров между собой, с молекулами инертного газа или со стенкой сосуда.
Схема реакции горения водорода, протекающей по цепному принципу, приведена на рис. 6. Итоговый результат одной цепочки горения водорода можно представить следующим равенством:
Н + 3Н2+О2 = 3Н + 2Н2О. (81)
Из этого уравнения видно, что вступление одного атома водорода в реакцию привело к появлению конечного продукта (2Н2О) итрех новых активных центров — атомов водорода, т. е. имеется процесс разветвления цепи.
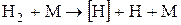
+
O2
OH O
+ +
H2 H2
H2O [H] [H] OH
+
H2 H2O
[H]
Рис. 6. Цепной принцип горения водорода
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 785; Нарушение авторских прав?; Мы поможем в написании вашей работы!