
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Методические указания к выполнению. контрольного задания
|
|
|
|
контрольного задания
Выполнение расчетов горения различных топлив, составление материальных и тепловых балансов является основой инженерных расчетов, связанных с сжиганием топлива.
Схема процесса горения топлива и последующего разбавления продуктов сгорания воздухом с целью получения энергоносителя в виде горячего газа в заданном количестве и с заданной температурой показана на рис. 38.
В камеру сгорания подаются топливо и окислитель, продукты сгорания поступают в камеру смешения, где смешиваются с воздухом, полученный энергоноситель поступает к потребителю.
Для упрощения расчетов составляющие тепловых потерь заданы в процентах, потери теплоты вследствие термической диссоциации не учитываются.
 Таблица исходных данных
Таблица исходных данных
| Параметр | Вариант | |||||||||||||||||||||||||
| Последняя цифра шрифта | ||||||||||||||||||||||||||
| Расход энергоносителя Vэ, м3/с | 3,0 | 2,5 | 2,0 | 0,75 | 4,0 | 4,5 | 3,5 | 5,0 | 1,0 | 1,5 | ||||||||||||||||
| Предпоследняя цифра шрифта | ||||||||||||||||||||||||||
| Температура энергоносителя Тэ, К | ||||||||||||||||||||||||||
| Топливо | Уголь ирша-бородинский Б2 | Уголь кузнецкий | Уголь донецкий | Сланец | Мазут малосернистый | Мазут высокосернистый | Газ природный Серпухово-Ленинский | Газ природный Саратов-Москва | Газ промышленный доменный | Газ генераторный водяной | ||||||||||||||||
| Тепловые потери |  , % , %
| 0,0 | 1,0 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | ||||||||||||||||
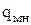 , % , %
| 0,5 | 2,0 | 3,0 | 0,5 | ||||||||||||||||||||||
 , % , %
| 0,5 | 1,0 | 1,5 | 2,0 | ||||||||||||||||||||||
| через наружные ограждения | ||||||||||||||||||||||||||
а) камеры сгорания 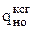 , % , %
| 0,4 | 0,5 | 1,0 | 1,5 | 2,0 | 2,5 | 3,0 | 3,5 | 4,0 | 5,0 | ||||||||||||||||
б) камеры смешания 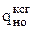 , % , %
| 1,5 | 0,5 | 1,0 | 0,4 | 9,0 | 1,0 | 0,5 | 7,0 | 8,0 | |||||||||||||||||
| Третья от конца цифра | ||||||||||||||||||||||||||
| Коэффициент расхода окислителя, α | 1,03 | 1,05 | 1,08 | 1,10 | 1,12 | 1,20 | 1,05 | 1,10 | 1,12 | 1,15 | ||||||||||||||||
Рекомендуется следующий порядок выполнения расчета:
1) определить и выбрать необходимые для последующих расчетов характеристики топлива (состав топлива, теплота сгорания, теплоемкость);
2) рассчитать теоретический расход окислителя и теоретический выход продуктов полного сгорания топлива;
3) определить температуру газов после камеры сгорания Тк сг, К;
4) составить уравнение теплового баланса всего процесса и определить на его основе объем воздуха, необходимый для разбавления продуктов сгорания vВ, м3/кг (м3/м3) топлива;
5) составить материальный баланс процесса и определить на его основе расход топлива В, кг/с (м3/с), окислителя Vок, м3/с, и воздуха VВ, м3/с;
6) рассчитать состав продуктов сгорания (после камеры сгорания) и энергоносителя (после камеры смешения), % об.
Состав топлива, теплота сгорания, теплоемкость выбирается по справочникам. При отсутствии опытных данных для расчета приближенного значения теплоты сгорания топлива может быть использована эмпирическая формула Д.И. Менделеева:
 ,
,
где 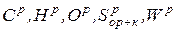 − элементы состава рабочей массы, %.
− элементы состава рабочей массы, %.
Низшая теплота сгорания 1 м3 газового топлива, МДж/м3, определяется при нормальных условиях по его составу и теплотам сгорания индивидуальных горючих газов по формуле:
 ,
,
где QCO, QH2, QCH4, QCmHn, QH2S − теплота сгорания соответствующих газов, МДж/м3;
СО, Н2, СН4, СmHn, H2S − содержание соответствующих газов в сухом газовом топливе, % об.
Теоретический расход окислителя для всех видов топлива, м3/кг (м3/м3), определяется исходя из концентрации кислорода в окислителе,
 ,
,
где О  − концентрация кислорода в окислителе, % об.;
− концентрация кислорода в окислителе, % об.;
v 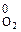 − теоретический расход кислорода, необходимый для полного сгорания 1 кг твердого (жидкого) или 1 м3 газообразного топлива, м3/кг (м3/м3).
− теоретический расход кислорода, необходимый для полного сгорания 1 кг твердого (жидкого) или 1 м3 газообразного топлива, м3/кг (м3/м3).
Для твердого (жидкого) топлива конкретного состава, м3/кг,
 ,
,
где  кг/м3 − плотность кислорода при нормальных условиях.
кг/м3 − плотность кислорода при нормальных условиях.
Для газового топлива известного состава, м3/м3,
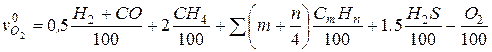 ,
,
где Н2, СО, СН4, СmHn, Н2S, О2 − концентрация составляющих газового топлива, % об.
При использовании воздуха в качестве окислителя его теоретический расход, необходимый для полного сгорания кг (м3) топлива, м3/кг (м3/м3), составляет:
 .
.
Коэффициент расхода окислителя:
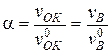 .
.
В общем случае для всех видов топлива суммарный выход продуктов полного сгорания, м3/кг (м3/м3), имеет вид
 .
.
Для твердого и жидкого топлива объемный выход:
СО2 при сгорании 1 кг углерода, м3/кг,
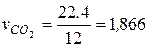 ;
;
SO2 при сжигании 1 кг серы, м3/кг,
 .
.
В практике технологических расчетов принимается

и
 .
.
Выход азота при сжигании твердых (жидких) топлив, м3/кг, определяется в зависимости от содержания азота в топливе и окислителе
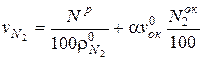 ,
,
где 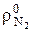 =1,251 − плотность азота при нормальных условиях, кг/м3;
=1,251 − плотность азота при нормальных условиях, кг/м3;
N  − содержание азота в окислителе, % об.
− содержание азота в окислителе, % об.
Объемное содержание кислорода в продуктах сгорания, м3/кг,
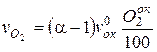 . (*)
. (*)
Выход водяных паров, м3/кг, определяется из материального баланса реакции горения водорода с учетом влажности рабочей массы топлива и влагосодержания окислителя
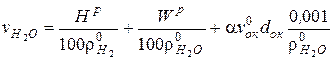 ,
,
где  = 0,089 и
= 0,089 и 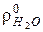 = 0,804 − соответственно плотность водорода и водяного пара при нормальных условиях, кг/м3;
= 0,804 − соответственно плотность водорода и водяного пара при нормальных условиях, кг/м3;
dок − влагосодержание окислителя, кг/м3, сухого окислителя.
При сжигании газового топлива выход сухих трехатомных продуктов сгорания (с учетом СО2, содержащегося в исходном газовом топливе), м3/м3, составляет
 .
.
Выход азота, м3/м3, определяется в зависимости от содержания азота в газовом топливе и окисляется с учетом коэффициента расхода окислителя
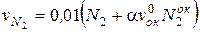 .
.
Объемное содержание кислорода в продуктах сгорания газового топлива, м3/м3, находится из выражения (*).
Выход водяных паров, м3/м3, определяется на основе химических реакций горения водородосодержащих компонентов газового топлива с учетом перехода в продукты сгорания влаги, содержащейся в топливе и окислителе
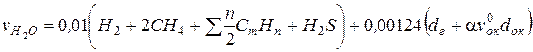 ,
,
где dг − влагосодержание газового топлива, г/м3 сухого газа.
Если в вышеприведенных формулах принять a=1, то определяются теоретические значения выхода продуктов полного сгорания топлива, при этом в продуктах сгорания отсутствует кислород, а объем продуктов сгорания, м3/кг (м3/м3), равен
 .
.
Выход сухих трехатомных продуктов полного сгорания топлива не зависит от численного значения a.
Температура газов после камеры сгорания определяется из уравнения теплового баланса камеры сгорания, МДж/кг (МДж/м3),
 ,
,
где 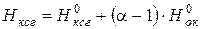 .
.
В явном виде уравнение баланса камеры сгорания не решается, так как входящие в это уравнение теплоемкости продуктов сгорания сами являются функцией температуры Тксг. Определить Тксг можно, используя метод последовательных приближений или графоаналитический метод. В последнем случае Тксг определяется следующим образом.
Из уравнения теплового баланса находят
 ,
,
иначе
 .
.
Запишем эту зависимость в виде системы двух функций:
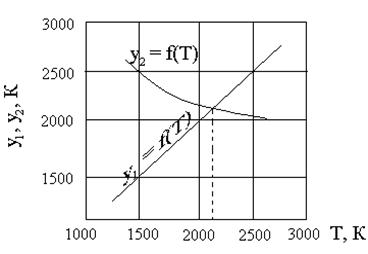 |
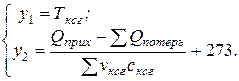
Рис. 39. Графоаналитический метод определения Тксг
Решение задачи относительно Тксг сводится к нахождению условия, при котором у1 = у2. Значения у1 и у2 рассчитываются не менее чем по трем значениям Тксг, близким к ожидаемому. Пример графического решения задачи по определению Тксг приведен на рис. 39.
В уравнении теплового баланса всего процесса учитываются тепловые потери в камерах сгорания и смешения. Оно имеет вид (на 1 кг или м3 топлива)
 ,
,
где Qрасп, Qв − соответственно количество теплоты, внесенное в процесс паром, используемым для распыления мазута, МДж/кг, и воздухом, используемым для разбавления продуктов сгорания, МДж/кг или МДж/м3 топлива.
Количество теплоты, внесенное в процесс воздухом, складывается из теплоты сухого воздуха и водяных паров, содержащихся в воздухе,
 ,
,
где 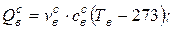
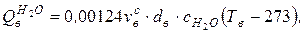
vвс − количество сухого воздуха, необходимое для разбавления продуктов сгорания, м3/кг (м3/м3) топлива;
свс, сН2О − средние в интервале температур от 273 до Тв теплоемкости сухого воздуха и водяных паров, МДж/(м3×К).
Энергоноситель в данном случае представляет собой смесь продуктов полного сгорания топлива, полученных при a=1, избыточного количества сухого окислителя, воздуха, вводимого в процесс при разбавлении продуктов сгорания топлива, и водяных паров, содержащихся в избыточном окислителе и воздухе. Поэтому его энтальпия, МДж/кг (МДж/м3),
 .
.
Энтальпия теоретического количества продуктов сгорания топлива в энергоносителе 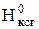 , МДж/кг (МДж/м3), рассчитывается по формуле
, МДж/кг (МДж/м3), рассчитывается по формуле
 ,
,
где с  допускается принять равной с
допускается принять равной с  .
.
Величина (a-1) Н  − энтальпия избыточного (сверх теоретически необходимого) количества окислителя, поступающего с дымовыми газами из камеры сгорания в камеру смешения
− энтальпия избыточного (сверх теоретически необходимого) количества окислителя, поступающего с дымовыми газами из камеры сгорания в камеру смешения
 ,
,
где сок, с 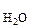 − средние в интервале температур от 273 до Тэ, К, объемные теплоемкости соответственно сухого окислителя и водяных паров, МДж/(м3×К).
− средние в интервале температур от 273 до Тэ, К, объемные теплоемкости соответственно сухого окислителя и водяных паров, МДж/(м3×К).
Энтальпия воздуха в камере смешения Нв, МДж/м3, рассчитывается при Тэ, К,
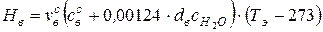 .
.
Подставив в уравнение теплового баланса найденные и заданные значения параметров, следует определить v 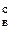 и удельный расход воздуха, необходимый для разбавления продуктов сгорания, м3/кг (м3/м3),
и удельный расход воздуха, необходимый для разбавления продуктов сгорания, м3/кг (м3/м3),
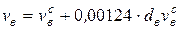 .
.
Определение расхода топлива В производится путем решения уравнения материального баланса процесса получения заданного количества энергоносителя после камеры смешения, выраженного через объемные расходы составляющих отходящих газов.
Секундный расход энергоносителя, м3/с, определяется по формуле
 ,
,
где V  − секундный расход продуктов сгорания, м3/с, образующихся при сжигании В с коэффициентом расхода окислителя a=1;
− секундный расход продуктов сгорания, м3/с, образующихся при сжигании В с коэффициентом расхода окислителя a=1;
Vок изб, Vв − секундные расходы соответственно избыточного окислителя и воздуха, м3/с.
Все указанные расходы могут быть выражены через расход топлива:
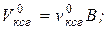
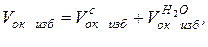
где V  − расход избыточного сухого окислителя, м3/с;
− расход избыточного сухого окислителя, м3/с;
V  − объем водяных паров в избыточном окислителе, м3/с,
− объем водяных паров в избыточном окислителе, м3/с,

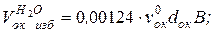
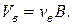
При известном (по заданию) Vэ и найденных Vкгс, Vок изб и Vв определяется секундный расход топлива, необходимый для получения заданного количества энергоносителя.
Секундный расход окислителя, м3/с, определяется по найденному В

Суммарный объем продуктов сгорания равен 100 %, тогда процентный состав продуктов сгорания, % об., равен
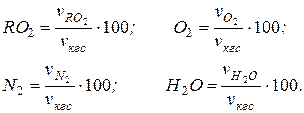
В результате разбавления продуктов сгорания воздухом в энергоносителе увеличивается количество азота, кислорода и водяных паров. Их определяют по формулам, м3/кг (м3/м3) топлива.

Общий выход энергоносителя
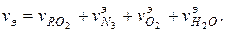
Состав энергоносителя, % об., определяется по формулам
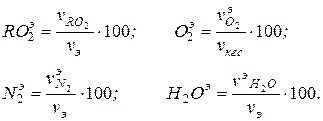
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 864; Нарушение авторских прав?; Мы поможем в написании вашей работы!