
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Особенности микромира
|
|
|
|
Открытие сложного строения атома - важнейший этап становления современной физики. В процессе создания количественной теории строения атома, позволившей объяснить атомные системы, были сформированы новые представления о свойствах микрочастиц, которые описываются квантовой механикой.
Существование закономерной связи между всеми химическими элементами, ярко выраженной в периодической системе Менделеева, наталкивает на мысль о том, что в основе строения всех атомов лежит общее свойство.
Различные предположения о строении атома долгое время не подтверждались какими-либо экспериментальными данными. Лишь в конце XIX в. были сделаны открытия, показавшие сложность строения атома и возможность превращения при определенных условиях одних атомов в другие. На основе этих открытий стало быстро развиваться учение о строении атома.
Первый толчок был дан Дж. Томсоном (1895), который открыл электрон - отрицательно заряженную частицу, входящую в состав всех атомов. Поскольку электрон имеет отрицательный заряд, а атом в целом нейтрален, то было сделано предположение о наличии и положительного заряда в атоме.
Стр. 37
Затем последовало открытие А. Беккерелем явления радиоактивности, которое заключалось в самопроизвольном превращении атомов одних элементов в атомы других элементов. Именно исследование радиоактивности позволило получить первые представления о строении атома.
В 1911 г. Э. Резерфорд предлагает ядерную модель атома. Исследования по рассеянию 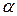 -частиц хорошо объясняли планетарную модель атома, состоявшую из положительно заряженного ядра, заключавшего в себе почти всю массу атома, и «планетарной системы» электронов.
-частиц хорошо объясняли планетарную модель атома, состоявшую из положительно заряженного ядра, заключавшего в себе почти всю массу атома, и «планетарной системы» электронов.
В 1913 г. Н. Бор впервые при решении вопроса о строении атома применил принцип квантования. Его гипотеза строения атома основывалась на двух постулатах, совершенно несовместимых с классической физикой: 1) существуют стационарные состояния (орбиты) электронов; 2) при переходе из одного стационарного состояния в другое атом излучает или поглощает порцию энергии.
Теория Бора занимает пограничное положение между классической физикой и квантовой механикой.
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 810; Нарушение авторских прав?; Мы поможем в написании вашей работы!