
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные определения. Химическое равновесие
|
|
|
|
Химическое равновесие
Теория химического равновесия рассматривается на основе второго закона термодинамики и закона действующих масс, открытого в начале 60 –х годов прошлого столетия. Одним из первых идею закона действующих масс предложил Н.Н.Бекетов (1827 – 1911 гг.).
Под объемно –мольной концентрацией подразумевается число молей вещества в единице объема (1 м3), т.е. 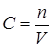 , где С –концентрация вещества; n –число молей и V –объем в м3.
, где С –концентрация вещества; n –число молей и V –объем в м3.
Скорость химической реакции. Под скоростью химической реакции подразумевается количество вещества в молях, прореагировавшее в единице объема за единицу времени.
При химическом равновесии обе реакции –прямая и обратная осуществляются с одинаковыми скоростями.
Закон действующих масс. Скорость химической реакции пропорциональна произведению концентрации реагирующих веществ. Для реакции 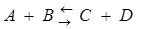 скорость прямой и обратной реакций w1 и w2 равны
скорость прямой и обратной реакций w1 и w2 равны
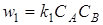 и
и 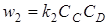 , (6.10)
, (6.10)
где СА, СВ, СС и СD –концентрации веществ A, B, C, D; k1 и k2 –коэффициенты пропорциональности –так называемые константы прямой и обратной реакций.
|
|
|
|
|
Дата добавления: 2014-12-07; Просмотров: 315; Нарушение авторских прав?; Мы поможем в написании вашей работы!