
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основні класи органічних сполук
|
|
|
|
Таблиця 2.1 – Вуглеводні
| Ознаки порівняння | Алкани (насичені) | Алкени (етиленові) | Алкіни (ацетиленові) | Арени (ароматичні) |
| Загальна формула | СnН2n+2 | СnН2n | СnН2n–2 | СnН2n–6 (похідні бензену) |
| Номенклатура міжнародна IUPAC -суфікс | -ан | -ен | -ин чи -ін | -ен |
| Функціональна група | 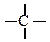
| 
| 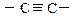
| 
|
| Ізомерія | Карбонового ланцюга. | Карбонового ланцюга, положення положення кратного зв’язку та для алкенів – геометрична. | Положення замісників (якщо їх більше одного). | |
| Гомологічні ряди | СН4 – метан С2Н6 – етан С3Н8 – пропан С4Н10 – бутани С5Н12 – пентани | С2Н4 – етилен С3Н6 – пропілен С4Н8 – бутени С5Н10– пентени | С2Н2 – ацетилен С3Н4 – пропін С4Н6 – бутини С5Н8 – пентини | С6Н6 – бензен С6Н5СН3 – толуен |
| Фізичні властивості | С1-С4 – гази; С5-С16 –рідини; решта – тверді речовини. | С2-С4 – гази; С5-С17 – рідини; решта – тверді речовини. | С2-С4 – гази4 С5-С16 –рідини; решта – тверді речовини. | Безбарвні рідини, що мають характерний запах. |
| У сполук лінійної будови Тпл. і Ткип. зростають зі збільшенням атомів С у молекулах. Газоподібні та тверді не мають запаху, рідкі мають специфічний запах бензину і гасу. Нерозчинні у воді, розчиняються в органічних розчинниках. Густина менша за одиницю. | ||||
| Небезпечність | Газоподібні, у суміші з киснем вибухонебезпечні. | Сильно токсичні. | ||
| Знаходження в природі | Головна складова природного газу і нафти. | Досить рідко у деяких родовищах нафти. |  
| У деяких видах нафти. |
| Застосування | Паливо, пальне для двигунів внутрішнього згорання. Для добування ненасичених вуглеводнів, водню, галогено-похідних та ін. | Виробництво пластмас, етанолу, етиленгліколю та ін. | Виробництво оцтового аль-дегіду і оцтової кислоти. | Виробництво барвників, медикаментів, пластмас, вибухових речовин, інсектицидів і гербіцидів. |
Найбільш характерні властивості вуглеводнів
Алкани
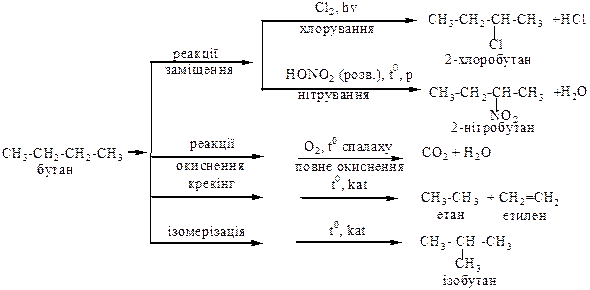
Алкени

Алкіни
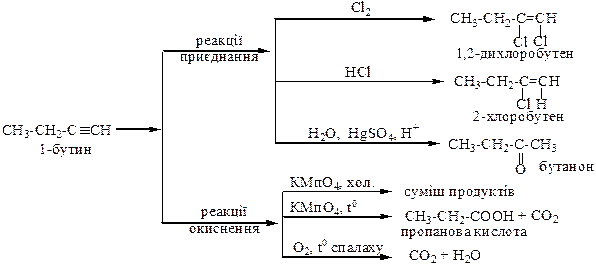
Арени
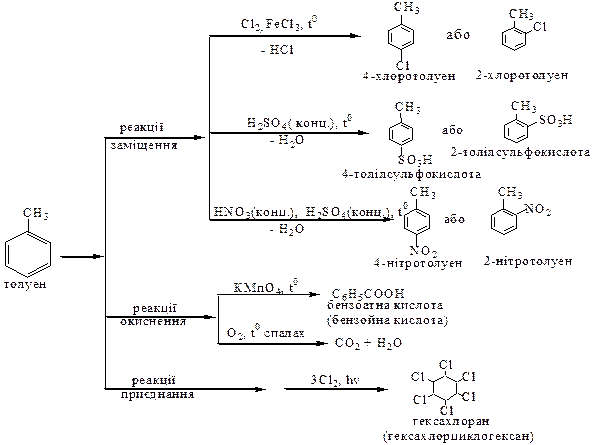
Таблиця 2.2 – Оксигеновмісні органічні речовини
| Ознаки порівняння | Спирти (одноатомні насичені) | Феноли одноатомні | Етери |
| Загальна формула | 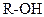
| Ar-OH | R1-O-R2, R-O-Ar, Ar1-O-Ar2 |
| Характеристична група | -ОН – гідроксигрупа біля насиченого атому С | -ОН –гідроксигрупа зв’язана з ароматичним кільцем | -О – зв’язані з однаковими чи різними замісниками |
| Номенклатура - тривіальна - IUPAC | СН3ОН – деревинний; С2Н5ОН – винний. суфікс -ол СН3ОН – метанол; С2Н5ОН – метанол. |
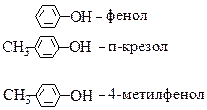
| C2H5-O-C2H5 – дієтиловий етер назва замісників + “етер” диетиловий етер |
| Фізичні властивості | С1-С10 – рідини, з С11 – тверді речовини, легші за воду, безбарвні. С1-С6 – різкий запах. Тверді – без запаху. С1-С3 – добре розчинні у воді. Молекули асоційовані між собою, тому Ткип. вищі за Ткип. сполук інших класів. | Феноли – кристалічні безбарвні речовини, погано розчиняються у воді, окиснюються на повітрі. Розчин фенолу у воді називають карболовою кислотою. | Безбарвні рідини з приємним запахом. У воді не розчиняються. |
| Небезпечність | СН3ОН – 10-20 см3 - сліпота, більша доза смертельна. Надзвичайно токсичний!!! С2Н5ОН – наркотична речовина, великі кількості (0,5-1 дм3) – смертельні! | При попаданні на шкіру чи слизову оболонку – опіки. Вражається кишечник, печінка, жовчний міхур. | С2Н5ОС2Н5 – наркотична речовина. Суміш з киснем – вибухонебезпечна. |
| Застосування | Розчинники. Широко використовують в органічному синтезі (альдегіди, кислоти, естери, етери). | Фенол використовують для одержання фенолформальдегідних смол і інших органічних речовин. | Розчинники |
Продовження таблиці 2.2
| Ознаки порівняння | Оксосполуки | Кислоти (одноосновні насичені) | Естери |
| Загальна формула | 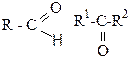
|
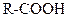
| 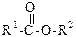
|
| Характеристична група |
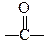 -- оксогрупа -- оксогрупа
|
-СООН – карбоксильна
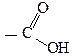
|
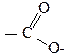
|
| Номенклатура - тривіальна - систематична | 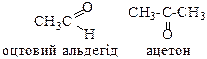 суфікси –аль (альдегіди) чи –он (кетон)
етаналь пропанон
суфікси –аль (альдегіди) чи –он (кетон)
етаналь пропанон
| НСООН – мурашина; СН3СООН – оцтова. суфікс –ова кислота НСООН – метанова кислота; СН3СООН – етанова кислота. |  назва замісників суфікс –оат
етилетаноат
назва замісників суфікс –оат
етилетаноат
|
| Фізичні властивості | С1 – газ, інші оксосполуки – рідини чи тверді речовини з специфічним запахом. Запах альдегідів більш різкий. Оксосполуки легші за воду, нижчі добре розчиняються у воді. | С 1-С3 – безбарвні рідини зз різким запахом. С4-С9 – олієподібні рідини з неприємним запахом. З С11 – тверді речовини, безбарвні. Низькомолекулярні кислоти добре розчинні у воді. | Безбарвні рідини з приємним запахом. У воді не розчиняються. |
| Продовження таблиці 2.2 | |||
| Небезпечність | Токсичні речовини, подразнюють слизову оболонку. | НСООН – при 0,75 мг/дм3 сильне подразнення, сльозоточивість, біль у грудях, кашель, катари шлунка. ГДК (НСООН) – 1 мг/м3. С(СН3СООН) – 2-3 мг/дм3 переносима не більше 3 хвилин. Викликає гострі і хронічні рініти, коньюктивіт. ГДК(СН3СООН) – 5 мг/м3. | Етилетаноат викликає подразнення слизових оболонок (1,44 г/дм3), дерматити, екземи. ГДК – 200 мг/м3. |
| Застосування | Ацетальдегід використовують для одержання пластмас, оцтової кислоти, винного спирту і інших речовин. Ацетон – розчинник. Синтез. | Мурашина кислота – у текстильній і шкіряній промисловості, оцтова – розчинник, виробництво штучних волокон, барвників та ін. | Розчинники |
Найбільш характерні реакції оксигеновмісних
похідних вуглеводнів
Спирти (алканоли)

Феноли

Етери
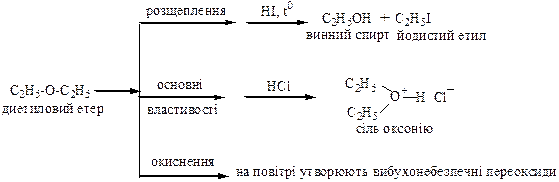
Таблиця 2.3 – Хімічні властивості альдегіів і кетонів
| Представники Реакції | 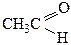 альдегіди
альдегіди
| 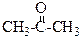 кетони
кетони
|
| 1. Реакції приєднання водню (відновлення) + Н2, Kat 2. Окиснення КМnО4 хол. КМnО4 нагр. | → C2H5OH етанол → СН3СООН оцтова кислота → СН3СООН | → СН3 – СН – СН3 | OH 2-пропанол не окиснюються з розривом ланцюга |
Карбонові кислоти

Естери

Таблиця 2.4 – Нітрогеновмісні органічні сполуки
| Аміни | Гетероциклічні сполуки | ||
| Представники | CH3NH2 – метиламін C6H5NH2 – анілін |
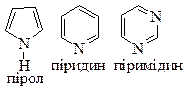
| |
| Фізичні властивості | СН3NH2 – газ з запахом амоніаку C6H5NH2 – рідина з неприємним запахом Нижчі аміни розчиняються у воді. | Рідини безбарвні з неприємним запахом! Розчинні у воді піридини та піримідини. | |
| Хімічні властивості | І Основні властивості
 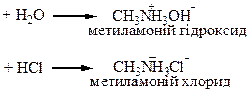 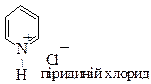
| ||
ІІ Кислотні властивості
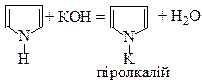
| |||
ІІІ Окиснення
 горять СО2 + Н2О + N2 горять СО2 + Н2О + N2
| |||
| Використання | Для виготовлення ліків, барвників, поверхневоактивних речовин. | Для виготовлення барвників та kіків. | |
| Небезпечність | Дуже токсичні речовини. Канцерогени. Токсичність зростає з ростом карбонового ланцюга. Навіть у малих концентраціях вражають нервову систему, впливають на кровотворненя, порушують функції печінки. Рідкий анілін всмоктується крізь шкіру зі швидкістю 0,2-0,7 г/см2/год. ГДК метиламіну – 1 мг/м3. ГДК аніліну – 0,1 мг/см3. | Пара піридину – сильний подразник, викликає сильно токсичну дію. В першу чергу вражає нервову систему, викликає дегенеративні зміни у печінці і нирках. ГДК піридину – 5 мг/м3. | |
Таблиця 2.5 – Галогеновмісні органічні сполуки
| Склад | СНСl3 хлороформ | ССl4 чотирихлористий карбон | CF2Cl2 дифлуоро-дихлоро- метан | СН2=СНСl хлористий вініл |
| Фізичні властивості | Безбарвна рідина, солодкуватий запах. | Негорюча безбарвна рдина, солодкуватий запах. | Газ, без кольору та запаху. | Безбарвний газ. |
| Густина більша за одиницю. Нерозчинні у воді. | ||||
| Хімічні властивості моногалогено похідних |
І. Реакції заміщення:
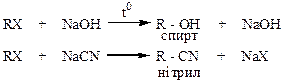 ІІ. Реакції відновлення:
ІІ. Реакції відновлення:
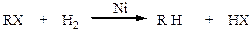
| |||
| Небезпечність | У присутності кисню розкла- дається з утво-ренням СОСl2 – фосгену (отруй-ний газ). Раніше використовував- ся як дихальний загальнонаркотич ний засіб, але виявлена побічна дія на серце і печінку. | При температурі вище за 5000С утворюється фосген. | Нетоксичний, вибухо-небезпечний. | ГДК = 0,1мг/м3 Канцерогенна речовина – пухлини печінки, системи крові та лімфи. |
| Застосування | Добрі розчинники | |||
| Одержання фреонів, тефлону. | Одержання фреонів. Негорючий розчин- ник. | Фреон (фреон-12) – хладоагент у холодильниках. Розчинник інсектицидів. | Одержання полівінілхлориду з якого виготовляють електро-ізоляційні матеріали, замінник шкіри, лінолеум тощо. |
Високомолекулярні сполуки (ВМС)
ВМС поділяють на природні (білки, нуклеїнові кислоти, полісахариди) та синтетичні.
Макромолекула полімеру побудована з однакових фрагментів (мономерних одиниць). Структурний елемент – найменша група атомів полімерного ланцюга, що повторюється (табл. 2.6).
Таблиця 2.6 – Будова ВМС
| Полімер | Мономер | Структурний фрагмент (ланка) | Структурний елемент |
| Поліетилен | 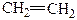
| 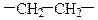
| 
|
| Полістирен | 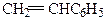
| 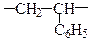
| 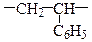
|
Число структурних фрагментів в макромолекулі називається ступінню полімеризації (n): [– СН2 – СН2 – ]n.
Більшість синтетичних полімерів утворена одним чи двома видами структурних фрагментів.
Найважливіші синтетичні полімери – це поліетилен, поліпропілен, полістирен, поліізобутилен, полібутадієни, полівінілхлорид, тефлон, поліакрілонітрил, поліметилметакрилат, епоксидні смоли, силікони, фенолформальдегідні смоли, сечовинформальдегідні смоли тощо.
Каучуки можуть бути натуральними і синтетичними (натрійбутадієновий, ізопреновий, хлоропреновий).
Натрійбутадієновий каучук відноситься до каучуків загального призначення і одержується полімерізацією бутадієну:
п СН2 = СН – СН = СН2 → [– СН2 – СН = СН – СН2–] п
Умови реакції: підвищений тиск та температура, натрій.
Ізопреновий каучук одержують з ізопрену:
п СН2 = С(СН3) – СН = СН2 → [– СН2 – С(СН3) = СН – СН2–] п
Хлоропреновий каучук одержують з хлоропрену:
п СН2 = С(Сl) – СН = СН2 → [– СН2 – С(Сl) = СН – СН2–] п
Цей каучук дуже стійкий до впливу світла, розчинників. Використовують для виробництва деталей та апаратури.
У теперішній час синтетичні полімери перестали бути замінниками природних речовин і є матеріалами, що за властивостями перевершують природні аналоги. У той же час, синтетичні полімери – це дуже інертні матеріали. Вони стійкі до впливу зовнішнього середовища і є біологічно жорсткими, що призводить до забруднення ними навколишнього середовища.
Поверхнево-активні речовини (ПАР)
До ПАР відносять речовини, які здатні знижувати поверхневе напруження рідин, особливо, води. Вони містять гідрофобний вуглеводневий залишок і гідрофільну группу атомів.
Щорічно майже половина ПАР використовується для виробництва миючих засобів, засобів для чистки, інша половина – це емульгатори, деемульгатори, інгібітори корозії, флотаційні засоби.
В залежності від заряду гідрофільної групи ПАР поділяють на:
- аніоноактивні (мило, синтетичні миючі засоби);
- катіоноактивні (флотаційні агенти, дезінфікуючі засоби);
- неіоногенні (компоненти різних миючих засобів);
- амфолітні (шампуні для волосся, дитячі шампуні).
До біологічно жорстких ПАР відносять алкілбензенсульфонати з розгалуженим алкільним замісником. ПАР такої будови у стічних водах дуже повільно руйнуються мікроорганізмами і довго забруднюють воду. Тому у більшості країн їх використання заборонено.
Сучасні миючі засоби містять поліфосфати, які підсилюють миючу дію ПАР. Однак, наявність фосфатів у миючих засобах призводить до збагачення фосфором природних вод і, як наслідок, – надмірному росту водоростей і водних рослин.
Література
1. Бобровник Л.Д., Руденко В.М., Лезенко Г.О. Органічна хімія. – К.: Ірпінь: ВТФ “Перун”. – 2005. – 544 с.
2. Жиряков В.Г. Органическая химия. – М.: Химия. – 1972. – 408 с.
3. Мітрясова О.П. Вступ до органічної хімії. – К.: ВД “Професіонал”. – 2007. – 400 с.
4. Нечаев А.П. Органическая химия. – М.: Высш. шк. – 1988. – 319 с.
5. Тейлор Г. Основы органической химии для студентов нехимических специальностей. – М.: Мир. – 1989. – 384 с.
6. Цвєткова Л.Б., Романюк О.П. Неорганічна і органічна хімія. – Львів: “Магнолія – 2006”. – 2007. – 358 с.
|
|
|
|
|
Дата добавления: 2014-12-07; Просмотров: 1081; Нарушение авторских прав?; Мы поможем в написании вашей работы!