
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Фотохимические реакции
|
|
|
|
Реакции, протекающие под воздействием светового излучения, называются фотохимическими, а раздел, изучающий фотохимические превращения, – фотохимией.
Основной закон фотохимии – закон квантовой эквивалентности (А. Эйнштейн, 1912 г): каждый поглощенный квант света hν вызывает изменение одной молекулы.
Важнейшим параметром фотохимической реакции служит квантовый выход γ:
|
В зависимости от типа фотохимической реакции квантовый выход может меняться в широких пределах. Это связано с возможностью потери поглощенной энергии до фотопревращения. Если время существования фотовозбужденной молекулы и скорость фотодиссоциации совпадают, то γ ~ 1. При γ >> 1 фотореакция идет по цепному механизму. В частности для реакции H2 + Cl2 = 2HCl γ = 105.
Типы фотохимических реакций:
1. Фотодиссоциация (фотолиз) приводит к разложению исходного вещества, поглотившего световую энергию. Примерами реакции фоторазложения служат такие: разложение галогенидов серебра (основа серебряной фотографии), фотолиз паров ацетона CH3CO CH3 → CO + другие продукты.
2. Фотосинтез приводит к образованию более сложных соединений. Примерами реакций фотосинтеза служат:
· фотосинтез озона в верхних слоях атмосферы, создающий защитный озоновый слой:

| фотодиссоциация |

| фотосинтез; |

|
| Рисунок 5.7. Кислород, которым зеленые растения обогащают атмосферу, образуется в процессе фотосинтеза. |
· фотосинтез органических соединений из углекислого газа, воды, минеральных веществ зелеными растениями. В частности, синтез глюкозы может быть описан уравнением:
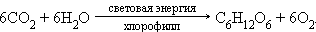
|
3. Фотохромизм – явление обратимого изменения пространственного или электронного строения молекул под действием света, сопровождающееся изменением окраски вещества. На основе фотохромных материалов изготовляются линзы с переменным светопропусканием, оконные стекла, фотохромные системы на основе некоторых органических и координационных соединений.

Тема 6: Растворы.
Цели:
1. Ознакомиться с определениями электролит и неэлектролит.
2. Знать способы выражения концентрации.
3. Уметь вычислять моляльность вещества, если известна его массовая доля.
4. Уметь определите молярную концентрацию, если известна массовая доля растворенного вещества и плотность этого раствора.
5. Знать концентрации, не меняющие свою величину при изменении температуры.
6. Знать какие растворы называют идеальными.
7. Уметь формулировать законы идеальных растворов (Рауля и Вант-Гоффа).
8. Узнать в чем состоит явление осмоса, и привести примеры, где осмос и осмотическое давление проявляется наиболее ярко.
9. Понимать в чем преимущество осмометрического метода определения молекулярных масс растворенных соединений.
10. Узнать какое из веществ: неэлектролит глюкоза (C6H12O6) и два электролита NaCl и BaCl2 при эквимолекулярной концентрации способно к наибольшему понижению температуры замерзания водного раствора.
11. Знать чем активность отличается от концентрации, и от каких факторов зависит коэффициент активности электролитов.
12. Узнать что такое ионная сила раствора электролита.
13. Узнать к каким соединениям применимо понятие произведение растворимости.
Классификация растворов.
Растворы – это гомогенные (однофазные) системы переменного состава, состоящие из двух или более веществ (компонентов).
По характеру агрегатного состояния растворы могут быть газообразными, жидкими и твердыми. Обычно компонент, который в данных условиях находится в том же агрегатном состоянии, что и образующийся раствор, считают растворителем, остальные составляющие раствора – растворенными веществами. В случае одинакового агрегатного состояния компонентов растворителем считают тот компонент, который преобладает в растворе.
В зависимости от размеров частиц растворы делятся на истинные и коллоидные. В истинных растворах (часто называемых просто растворами) растворенное вещество диспергировано до атомного или молекулярного уровня, частицы растворенного вещества не видимы ни визуально, ни под микроскопом, свободно передвигаются в среде растворителя. Истинные растворы – термодинамически устойчивые системы, неограниченно стабильные во времени.
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 443; Нарушение авторских прав?; Мы поможем в написании вашей работы!
