
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
ЗWake UpИ 39 страница
|
|
|
|
CaC2 + 2H2O = Ca(OH)2 + H2C2
H2C2 + 2HCl = CH3CHCl2
Задача 2.
Из бинарных соединений натрия при взаимодействии с водой газ будут образовывать гидрид, карбид, нитрид, фосфид. Соответственно, продуктами взаимодействия с водой могут быть водород, ацетилен, аммиак и фосфин. Поскольку относительная плотность выделяющегося при взаимодействии с водой газа равна 1,30, молярная масса этого газа составляет М = 1,30 · 20 = 26 г/моль. Данному условию отвечает ацетилен, С2Н2.
По-видимому, второй газ поглощается кислотой. Из указанных выше вариантов основные свойства проявляет только аммиак. Следовательно, исходная смесь состояла из карбида и нитрида натрия.
Na3N + 3H2O = 3NaOH + NH3
Na2C2 + 2H2O = 2NaOH + C2H2
2Na3N + 4H3PO3 = 3Na2HPO3 + (NH4)2HPO3
Na2C2 + H3PO3 = Na2HPO3 + C2H2
Определим мольное соотношение нитрида и карбида натрия. Пусть мольная доля аммиака в смеси газообразных продуктов составляет х. Тогда:
17х +26 · (1-х) = 1,00 · 20 = 20
Х = 2/3, т.е., на 2/3 моль нитрида натрия приходится 1/3 моль карбида.
Тогда массовая доля нитрида натрия составит
2/3 · 83: (2/3 · 83 + 1/3 · 70) = 70,3%
Массовая доля карбида натрия – 29,7%.
Задача 3.
При электролизе будет протекать процесс:
2HBr = H2 + Br2
Полученный бром будет взаимодействовать с раствором поташа:
3K2CO3 + Br2 = 5KBr + KBrO3 + 3CO2
В исходном растворе хлороводорода присутствовало 200 · 1,15 · 0,15: 81 = 0,426 моль HBr. Для получения 1 моль брома требуется 96500 · 2 = 193000 Кл. По условию задачи через раствор пропустили 7 000 Кл электричества, следовательно, бромоводород в недостатке. В результате электролиза получилось 7000: 193000 = 0,036 моль брома.
В растворе поташа присутствовало 200 · 0,08: 138 = 0,116 моль карбоната калия. По-видимому, бром взят в недостатке. Тогда в результате реакции получится 0,18 моль бромида калия и 0,036 моль бромата калия, а также останется 0,01 моль карбоната калия.
Масса сухого остатка составит
m = 0,18 · 110 + 0,036 · 167 + 0,01 · 138 = 27,192 г
Задача 4.
Запишем кинетическое уравнение реакции.
V = k[CH3CHO]2
Понижение давления равнозначно уменьшению концентрации газообразных веществ. Следовательно, концентрация стала равна (0,72:1,5)[CH3CHO] = 0,48[CH3CHO].
V’ = k[CH3CHO]’2 = k∙0,482[CH3CHO]2 = 0,2304V
По условию также увеличили температуру на 20 oС. По правилу Вант-Гоффа:
V’ = V∙gDT/10 = V∙2,22 = 4,84V
В результате скорость реакции увеличится в 0,2304∙4,84 = 1,12 раза.
Схема катализа:
СН3СНО + I2 → СН3I + НI + СО
СН3I + НI → СН4 + I2
Ответ: скорость реакции увеличится в 1,12 раза.
Задача 5.
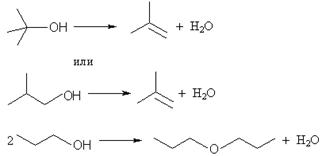
Кислотная дегидратация спиртов приводит к образованию алкенов или простых эфиров (только в случае первичных спиртов). Рассмотрим возможные случаи образования продуктов в температурном интервале нагревания до 140 oС (тогда исключается возможность образования алкенов из первичных спиртов):
1) первичный (1)/первичный (2) – эфир (1), эфир(2), эфир (3) – продукт перекрестной дегидратации: образуется 3 продукта, противоречит условию;
2) вторичный (1)/ вторичный (2) – алкен (1), алкен (2); для случаев третичный (1)/третичный (2) и вторичный/третичный аналогично: массовая доля углерода 12n: 14n = 6/7 есть величина постоянная для любого алкена (CnH2n), противоречит условию;
3) первичный/ вторичный – эфир, алкен; для случая первичный/третичный аналогично – удовлетворяет условию.
Легко показать, что массовая доля углерода в любом эфире всегда меньше, чем в алкене. Общая формула эфира CnH2n+2O, ω(C) = 12n: (14n + 18) = 6/7 – 0,151. Решая это уравнение, получим n = 6. В спирте число атомов углерода в 2 раза меньше. Таким образом, один из спиртов н-C3H7OH.
ω(C в н-C3H7OH) = 100∙12∙3: 60 = 60%, тогда ω(C в CmH2m + 2O) = (60 ± 4,9)% = 100∙12m: (14m + 18). Решая два уравнения, получим, m = 2,3 и m = 4. m должно быть натуральным числом, т.е. m = 4. Второй спирт – t-C4H9OH или i-C4H9OH.
Задача 6.
Пусть Х – доля минорного компонента. По выражению для константы равновесия: 0,11=Х: (1-Х), Х=0,099, т.е 9,9% и 90,1%. Наиболее термодинамически стабилен 2-бромпропан, он будет в избытке.
Одним из удобных способов синтеза является следующий:
CaC2 + 2H2O = HC≡CH + Ca(OH)2
Al4C3 + 12HCl = 3CH4 + 4AlCl3
CH4 + Br2 = CH3Br
HC≡CH + NaNH2 = HC≡CNa + NH3 (вместо NaNH2 можно использовать Na)
HC≡CNa + CH3Br = HC≡CCH3 + NaBr
HC≡CCH3 + H2 = H2C=CHCH3 (реакция идет в присутствии каталитически активного Pd)
H2C=CHCH3 + HBr = H3CCHBrCH3
Однако возможны и другие пути синтеза.
o Мастер-класс ЗФантазийная игрушкаИ,
Катерина Мисюра
10:00 Р 12.00
o Мастер-класс ЗЖивописьИ,
Мария Покровская
12:00 Р 12:45
o Мастер-класс ЗТехника Поп-апИ,
Лидия Пожидаева
13:00Р 16:00
o Мастер-класс ЗЖивописьИ,
Мария Покровская
16:00 Р 16:45
o Мастер-класс ЗСоздание КалейдоскопаИ,
Янина Черных
17:00 Р 19:00
Площадка ЗЖелезный ПятакИ
o Мастер-класс "Граффити",
Группа 310
16:00 - 19:00
Павильон ЗКольца Города-СадаИ
o Открытие ЗБалансирующей выставкиИ,
Государственного Центра Современного Искусства (ГЦСИ),
16:00 Р 16:15
o ЗБалансирующая выставкаИ,
Государственный Центр Современного Искусства (ГЦСИ)
16:15 Р 23.00
ДК ЗМеталлургИ
o Мастер-класс
ЗМастерская Стомп / Stomp workshopИ
13:00 -14:30; 14:45 -16:15; 17:15 Р 18:45; 19:15 Р 21:45
ДК ЗМеталлургИ, малый зал
o Лекция по граффити,
Группа 310
12:00 Р 13:00
o Лекция архитектора,
Хавьер Понсе / Javier Ponce (Испания)
(победитель архитектурного конкурса ЗБалансирующий ПавильонИ)
14:00 - 15:30
Художественная школа
o Мастер-класс по фотополимерным технологиям,
Андрей Булгаков
12:00 Р 14:00
o Мастер-класс ТИзготовление рельефов из гипсаУ,
Михаил Ефименко
14:00-18:00
Дом-музей Баташевых
o Открытие выставки ЗТень зеленого городаИ,
Государственный музей архитектуры (Москва),
куратор И.В.Чепкунова
13:00 - 13:30
o Выставка ЗТень зеленого городаИ,
Государственный музей архитектуры (Москва),
куратор И.В.Чепкунова
14:00-19:00
Скульптура ЗЭнтазис Данс IVИ:
o ЗЭнтазис Данс IV / Entasis Dance IVИ,
перформанс Р скульптура,
автор Ив Бэйлей / Eve Bailey (Нью-Йорк, США)
15:00 Р 15:30; 16:30 Р 17:00; 18:00 Р 18:30; 19:30 Р 20:00; 20:30 Р 21:00
Аллея Молодёжи
o Выставка ЗИскусство в пейзаже: Лэнд-арт и скульптураИ
круглосуточно
Город
o Флеш-моб ЗСуперГнездоИ (в рамках открытия скульптуры),
Дмитрий Алексеев,
(М-н Жуковского, 7 Р 7а)
12:00 - 14:30
o Открытие пандуса. Посадка деревьев,
Фонд ЗОмк-УчастиеИ,
Детская Поликлиника (ул. Красные Зори, д. 16, стр. 2)
13:00 - 15:00
o Завершение коллективной работы по граффити,
(ул. Братьев Баташевых д.1)
12:00 Р 17:00
o ЗВыставка стрит-арта под открытым небомИ,
Работы стрит-арт по всему городу (см. карту фестиваля)
круглосуточно
01 июня
Основная сцена:
o Чемпионат по брейкингу 1х1,
конкурсная программа
17:00 Р 20.30
o Показательное выступление BMX FlatLand,
Алексей Прошин + Константин Чернов
20:30 Р 21:00
o Театр ЗАльтерумИ,
современный танец / брейкданс
21:00 Р 21:15
o Театр ЗГартнерплац / The GЉrtnerplatz TheatreИ (Мюнхен),
современный балет
21:45 Р 22:00
o Саша Пушкин (Берлин), клавишные, голос;
Миметик (Швейцария), электроника;
Юрий Элик (Санкт-Петербург), виджеинг;
музыкально-визуальный перформанс
22:00 Р 23:30
Скейт-парк:
o Riding non-stop: велотриал
13:00 Р 16:00
o Показательные выступления
Велотриал,
Михаил Суханов
16:00 -16:30
Паркур-парк / ворк-аут / триал:
o Соревнования по Work Out
12:00 Р 14:00
o Соревнования по Parkour
14:00 Р 16:00
Центральная поляна:
o Мастер-класс ЗЛэнд-арт для детейИ,
Павел Дудка
11:00 Р 12:00
o Акция / мастер-класс ЗЧудо-ЛавкаИ,
Георгий Попов и Андрей Салак, художники, ведущие мастер-классов, организаторы фестиваля
12:00 Р 15:00
o Мастер-класс по современному танцу,
Театр ЗАльтерумИ
15:30 Р 17:00
Музыкальная поляна
o Мастер-класс ЗСоздание шумящих музыкальных инструментовИ
Арт-группа ЗУХТОИ
11:00-17:00
Сфера ЗЭкранИ
o Мастер-класс художника,
Роб Малхолланд / Rob Mulholland (Шотландия)
11:00 Р14:00
o Мастер-класс ЗМузыка сегодня и музыка завтраИ, сессия 2
Арсений Трофим
14:30 Р 17:00
o Ансамбль Детских Музыкальных Инструментов (АДМИ),
музыкальный перформанс
18:00 Р 19:30
Арт-павильон ЗАтом 49И
o ЗПлощадка Свободного ТворчестваИ
Выставка по итогам мастер-классов межфестивальной программы
11:00 Р 18:00
Арт-павильон ЗНаправляй энергиюИ
o Мастер-класс ЗСоздание арт-объектовИ
Георгий Попов и Андрей Салак
10:00Р12:30
o Мастер-класс ЗКаллиграфияИ,
Каори Исидзима / Kaori Ishijima (Япония)
13:00 Р 14:30
o Мастер-класс ЗКаллиграфияИ,
Каори Исидзима / Kaori Ishijima (Япония)
15:00 Р 16:30
o Мастер-класс ЗВолшебная лампаИ
Студия ЗДети и домаИ
17:00-19:00
|
|
|
|
|
Дата добавления: 2015-01-03; Просмотров: 292; Нарушение авторских прав?; Мы поможем в написании вашей работы!